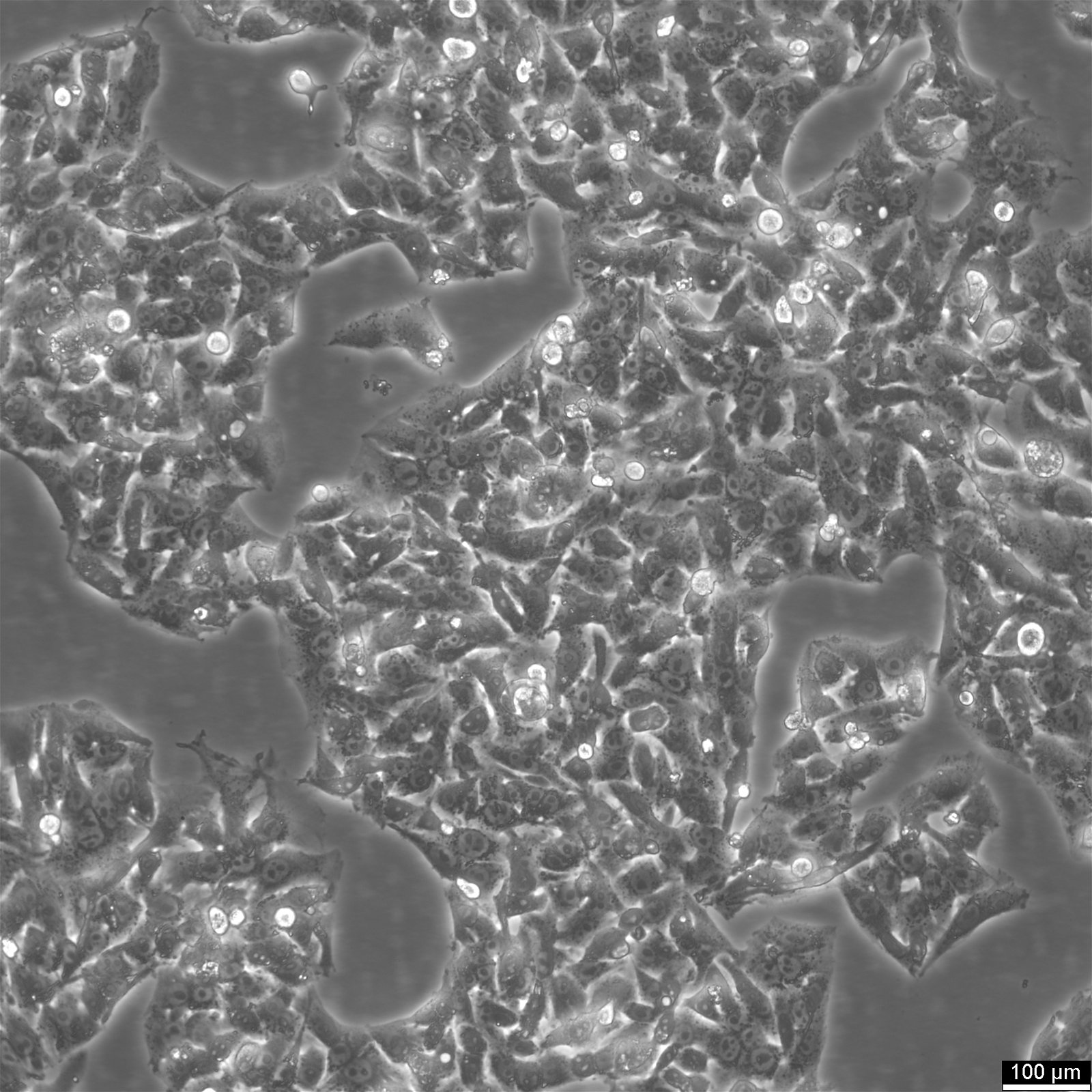
Buňky HepG2 - zdroj pro výzkum rakoviny jater
Hep-G2 je lidská buněčná linie jaterního karcinomu pocházející z jaterní tkáně 15letého bělocha s hepatocelulárním karcinomem. Tyto buňky se často využívají ve studiích metabolismu léčiv a hepatotoxicity. Přestože buňky HepG2 mají vysokou míru proliferace a vzhled podobný epitelu, nejsou nádorové a plní různé diferencované jaterní funkce. V roce 1975 vědci odvodili buňky HepG2 z hepatocelulárního karcinomu, čímž se staly první jaterní buněčnou linií, která vykazovala kritické vlastnosti hepatocytů. Na rozdíl od dříve zavedené buněčné linie SK-Hep1, která postrádá základní markery jaterních buněk, mohou buňky HepG2 vylučovat různé plazmatické proteiny a poskytují cenný model pro studium intracelulární dynamiky povrchových domén lidských hepatocytů. Tyto buňky vykazují morfologii podobnou epitelu, mají modální počet chromozomů 55 a lze je stimulovat lidským růstovým hormonem
Charakteristika HepG2
Primární hepatocyty mají typický kubický tvar a obvykle obsahují dvě jádra. Naproti tomu buňky HepG2 mají epiteliální morfologii s jedním jádrem a počtem chromozomů v rozmezí 48 až 54 na buňku. Ačkoli buňky HepG2 mohou tvořit až 25 % celkového buněčného proteinu, jejich velikost je větší než u normálních hepatocytů a tvoří asi 10 % kompletního proteinu v buňce. Buněčné proteiny jsou rozhodujícími aktéry v buňce, kteří vykonávají funkce určené geny.
Nádorové buňky, včetně těch s abnormálním počtem chromozomů, často vykazují zvýšený počet jader, a to až na sedm na buňku. Vzhledem k vysokému stupni diferenciace in vitro představují buňky HepG2 ideální model pro studium vnitrobuněčného obchodu a dynamiky žlučových kanálků, sinusoidálních membránových proteinů a lipidů v lidských hepatocytech.
Průměrný průměr buňky HepG2 je přibližně 10-20 µm, což je menší než průměr hepatocytu 15 µm, ale podobný jako u nádorových buněk hepatoblastomu (HB), které se pohybují v rozmezí 10-20 µm.
Genetika HepG2
Buněčná linie Hep-G2 vykazuje několik translokací, včetně translokací mezi krátkými raménky chromozomů 1 a 21, trizomií chromozomů 2, 16 a 17 a tetrasomií chromozomu 20. V buněčné linii Hep-G2 se vyskytuje několik translokací. Pozorována je také ztráta oblasti chromozomu 4q3, která souvisí s translokací t(1;4) často pozorovanou u hepatoblastomu (HB) a dalšími chromozomálními abnormalitami, jako jsou trizomie 2 a 20. Počet chromozomů v buňkách HepG2 se pohybuje mezi 50 a 60, což svědčí o hyperdiploidním karyotypu, zatímco některé případy vykazují více než 100 chromozomů a vyznačují se tetraploidním rozšířením. Buňky HepG2 obsahují přibližně 7,5 pg DNA, což je o 15 % více než průměrná somatická buňka. Pro srovnání, primární hepatocyty mají kubický tvar buňky a obvykle obsahují dvě jádra [1].
Mutační profil buněk HepG2
Buněčná linie HepG2 nese mutaci C228T v promotorové oblasti TERT, která se vyskytuje také u hepatocelulárního karcinomu (HCC) a hepatoblastomu (HB). Tato mutace přispívá k imortalizaci tím, že chrání telomery v nádorových buňkách. Buňky HepG2 navíc vykazují divoký typ genu TP53, který je kritický pro potlačení lidského nádorového onemocnění, protože hraje roli při zastavení buněčného cyklu, apoptóze a stárnutí. Mutace v tomto genu mohou podporovat proliferaci buněk.
Buňky HepG2 se účastní několika drah, včetně dysregulace buněčného růstu, drah přežití, jako je fetální a embryonální HB, a dráhy Wnt/β-katenin. Tato buněčná linie má navíc charakteristickou deleci třetího exonu genu CTNNB1, která je shodná s delecí pozorovanou u epiteliálního typu HB [2,3].
Přehled buněk hepatocelulárního karcinomu HepG2 ve výzkumu jater
Buňky HepG2 pocházející z lidského hepatomu se staly neocenitelným nástrojem pro výzkum jaterních funkcí a onemocnění, včetně hepatocelulárního karcinomu. Tyto jaterní buněčné linie umožňují nahlédnout do buněčných reakcí lidských hepatocytů za různých experimentálních podmínek. Použití luciferázových reportérových plazmidů v buňkách HepG2 je zvláště účinné pro sledování genové exprese a buněčných transfekcí, které jsou zásadní pro metabolický výzkum, například pro studium účinků ethanolu na jaterní buňky
Studie virových infekcí a jaterních onemocnění s použitím buněk HepG2
Imortalizované jaterní nádorové buněčné linie, jako jsou HepG2 a Huh7, mají zásadní význam při studiu virových infekcí, neboť prokazují kompletní buněčný cyklus replikace viru hepatitidy D (HDV) a expresi viru hepatitidy B (HBV) [5,6]. Současně hrají buněčné linie HepaRG zásadní roli při objasňování mechanismů vstupu HBV [7]. Buňky HepG2 se rovněž využívají ke zkoumání různých onemocnění lidských jater, od genetických stavů, jako je progresivní familiární intrahepatální cholestáza (PFIC) a Dubin-Johnsonův syndrom, až po environmentální a dietní studie související s cytotoxickými a genotoxickými látkami, jakož i při výzkumu cílení léčiv a hepatokarcinogeneze [8,9]. Jejich využití se rozšiřuje i na studie s bio-umělými jaterními zařízeními
Interakce buněk HepG2 s biomateriály v tkáňovém inženýrství
Interakce buněk HepG2 s různými biomateriály je v tkáňovém inženýrství klíčová. Techniky, jako je technika koloidní sondy, pomáhají porozumět těmto interakcím měřením adhezních vlastností buněk, které jsou zásadní pro určení životaschopnosti buněk pro vývoj scaffoldů a přesných modelů jaterní tkáně
Chování buněk a inovace v modelech založených na HepG2
Studium chování buněk v modelech založených na HepG2 je pro výzkum jaterních onemocnění zásadní. Pokroky v oblasti trojrozměrných sféroidních buněčných kultur vedly k vytvoření buněčných sféroidů HepG2, které nabízejí fyziologicky relevantnější model, jenž věrně odráží normální hepatocyty. Tyto trojrozměrné modely se zvýšenou metabolickou aktivitou naznačují potenciál buněk HepG2 sloužit jako model hepatoblastomu a mají význam ve výzkumu léčby rakoviny, zejména pro simulaci jaterních nádorů a testování nových terapeutických přístupů [10-12]
Srovnání a charakteristiky HepG2 mezi ostatními nádorovými buněčnými liniemi
HepG2 je jednou z nejpoužívanějších buněčných linií jaterních nádorů, která byla vybrána pro své široké využití ve vědeckém výzkumu mezi přibližně 40 dostupnými buněčnými liniemi jaterních nádorů [13]. Navzdory slabé nebo chybějící expresi některých enzymů cytochromu P450 ve srovnání s normálními hepatocyty vedl metabolický profil HepG2 ke snahám o modifikaci buněčné linie pro lepší studie metabolismu léčiv [13]. Ve srovnání s nádorovými buněčnými liniemi, jako jsou MCF7, PC3, 143B a HEK293, vykazují buňky HepG2 jedinečné profily obsahu aminokyselin, které významně ovlivňují syntézu a sekreci proteinů, což poukazuje na jejich jedinečné metabolické dráhy [14]
Výzkum onemocnění jater pomocí HepG2
Subkultivace buněk HepG2
Zde je uvedeno pět kroků pro odstranění adherentních buněk z baněk s buněčnou kulturou pomocí Accutase:
- Odstraňte médium z baňky a opláchněte adherované buňky pomocí PBS bez vápníku a hořčíku. Použijte 3-5 ml PBS pro baňky T25 a 5-10 ml pro baňky T75.
- Do baňky s buněčnou kulturou přidejte akutázu, a to 1-2 ml na baňku T25 a 2,5 ml na baňku T75. Zajistěte, aby Accutase pokryla celý buněčný list.
- Inkubujte baňku při pokojové teplotě po dobu 8-10 minut.
- Opatrně resuspendujte buňky s médiem s použitím 10 ml čerstvého média.
- Resuspendované buňky odstřeďujte 5 minut při 300xg, znovu je rozpusťte v čerstvém médiu a rozdělte je do nových baněk obsahujících čerstvé médium.
Budoucí perspektivy buněk HepG2
Snaha o odhalení plného potenciálu buněčné linie HepG2 pokračuje díky průlomovému pokroku ve zvyšování exprese cytochromů. Výzkumníci také zkoumají možnost trojrozměrných kultivací sféroidních buněk, které nabízejí fyziologicky relevantnější systém. Metabolická aktivita, včetně cytochromů, je ve 3D sféroidních modelech HepG2 pozoruhodně vyšší než ve 2D buňkách, což nás přibližuje k vytvoření modelu, který odráží normální hepatocyty. Zkoumání dynamických procesů, které jsou základem nesprávné distribuce povrchových buněčných proteinů, může navíc otevřít cestu k lepšímu pochopení jaterních onemocnění
Buňky HepG2: Pochopení jejich úlohy a rozdílů v biomedicínském výzkumu - nejčastější dotazy
Odkazy
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiation-induced chromosomal breakage and rejoining in interphase-metaphase chromosomes of human lymphocytes, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4 Inhibition: Nová terapeutická strategie reaktivace P53 u hepatoblastomu. Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53 Mutations and hepatocellular Carcinoma: Insights into the Etiology and Pathogenesis of Liver Cancer. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Critical Investigation of the Usability of Hepatoma Cell Lines HepG2 and Huh7 as Models for the Metabolic Representation of Resectable Hepatocellular Carcinoma (Kritické zkoumání použitelnosti hepatomových buněčných linií HepG2 a Huh7 jako modelů pro metabolické zobrazení resekabilního hepatocelulárního karcinomu). Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Cell Culture Models for the Investigation of Hepatitis B and D Virus Infection. Viruses 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Viruses. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Infection of a Human Hepatoma Cell Line by Hepatitis B Virus. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. Use of a human-derived liver cell line for the detection of cytoprotective, antigenotoxic and cogenotoxic agents. Toxikologie. 2004; 198(1-3): 329-340.
- Fanelli, A. HepG2 (jaterní hepatocelulární karcinom): buněčná kultura. HepG2. Získáno 3. prosince 2017.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Development of HepG2-Derived Cells Expressing Cytochrome P450s for Assessing Metabolism-Associated Drug-Induced Liver Toxicity (Vývoj buněk odvozených od HepG2 exprimujících cytochrom P450 pro hodnocení toxicity jater vyvolané léky související s metabolismem). Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. Application of in Vitro Metabolism Activation in High-Throughput Screening (Použití aktivace metabolismu in vitro při vysokokapacitním screeningu). Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. Down-Regulation of Dehydroepiandrosterone Sulfotransferase Gene in Human Hepatocellular Carcinoma [Snížená regulace genu pro dehydroepiandrosteron sulfotransferázu u lidského hepatocelulárního karcinomu]. Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Cancer stem/progenitor cells are highly enriched in CD133 + CD44 + population in hepatocellular carcinoma. Int J Cancer. 2010; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. Characterization of human cytochrome P450 enzymes involved in the metabolism of cyamemazine. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.