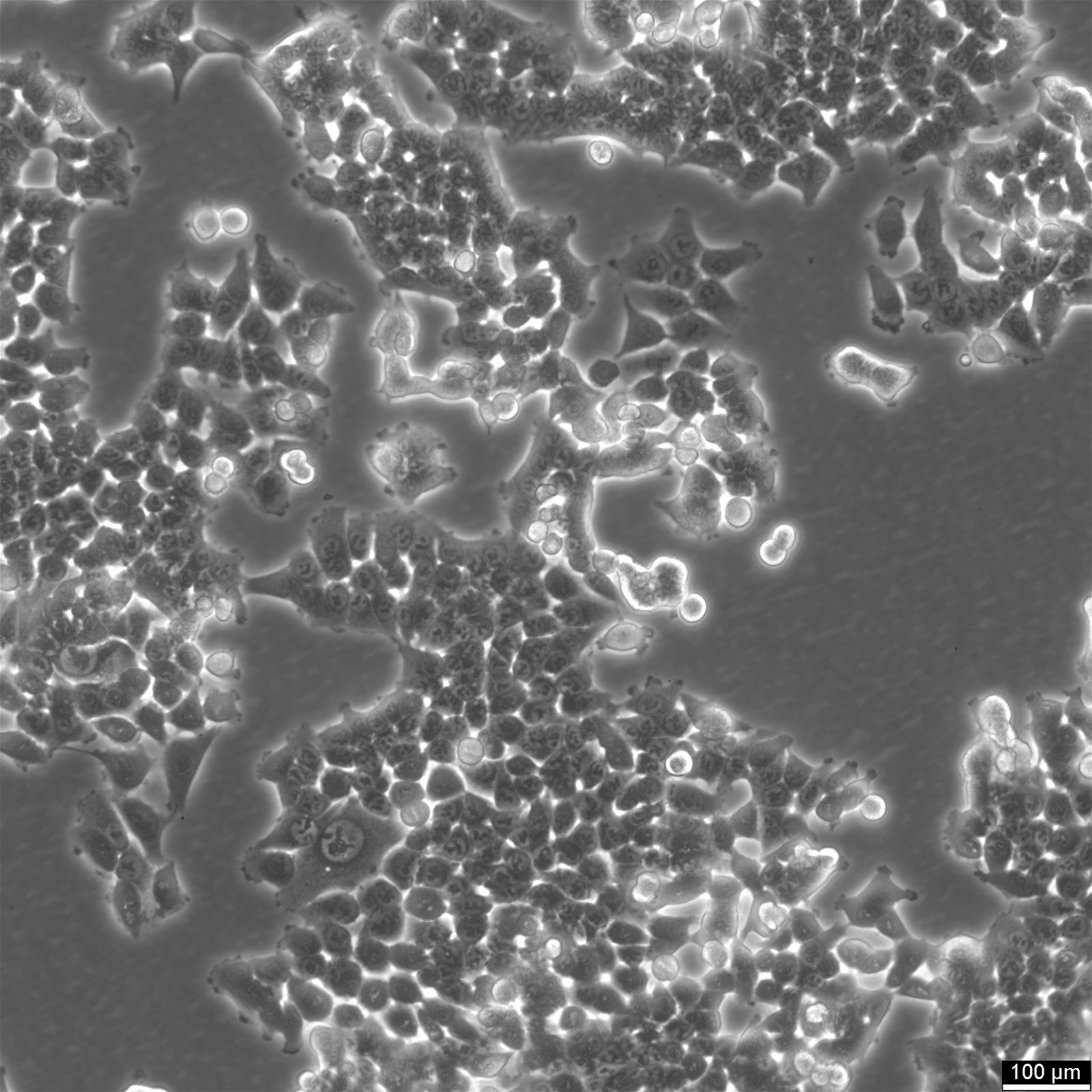
Buněčná linie HCT116: Pilíř ve výzkumu kolorektálního karcinomu
Buněčná linie HCT116 je základním kamenem výzkumu kolorektálního karcinomu a nabízí neocenitelné poznatky o patogenezi tohoto onemocnění a potenciálních terapeutických možnostech. HCT116 je známá svou užitečností ve výzkumu rakoviny a farmakologickém hodnocení a usnadňuje klíčové studie chování nádorů a účinnosti léků.
Původ a základní charakteristiky buněk HCT116
Pochopení kořenů a základních vlastností buněk HCT116, jako jsou jejich morfologické rysy, genetická výbava a buněčné rozměry, je pro výzkumné pracovníky, kteří se pouštějí do studií využívajících tuto buněčnou linii, zásadní.
Původ a genetické prostředí: Buňky HCT116 pocházejí z tlustého střeva 48letého muže bělošské rasy s diagnózou kolorektálního karcinomu a vyznačují se mutací v kodonu 13 (G13D) genu KRAS, který je součástí signální dráhy RAS/RAF/MEK/ERK. Tato konkrétní mutace je klíčová pro onkogenní transformaci těchto buněk, což podtrhuje jejich význam ve výzkumu rakoviny.
Morfologie a růstové charakteristiky: Buňky HCT116 vykazují morfologii podobnou epitelu a obvykle rostou v jednovrstvých kulturách, ale mohou také vytvářet sféroidy o průměru 150-400 µm. Tato přizpůsobivost růstových vzorců podtrhuje jejich univerzálnost v různých experimentálních sestavách.
Chromozomální profil: Chromozomální složení buněk HCT116 je téměř diploidní, přibližně 70 % buněčné populace nese 45 chromozomů. Pozoruhodná je opakovaná amplifikace dlouhých ramen chromozomů 8, 10, 16 a 17, zatímco chromozom Y chybí, což přispívá k jejich jedinečnému genomickému podpisu.
Srovnávací analýza: buněčné linie HCT116 vs. HT29
Při porovnání buněčné linie HCT116 s HT29, další buněčnou linií lidského kolorektálního karcinomu, se objevují výrazné rozdíly v jejich onkogenním potenciálu a diferenciačních schopnostech:
Onkogenní agresivita a diferenciace: Buňky HCT116 se vyznačují vysokou onkogenní agresivitou a omezeným diferenciačním potenciálem, což z nich činí model pro studium agresivních nádorových fenotypů. Naproti tomu buňky HT29 vykazují schopnost diferenciace do linií podobných enterocytům a produkujících mucin, což představuje kontrastní model, který napodobuje různé aspekty biologie kolorektálního karcinomu.
Toto srovnávací poznání buněčných linií HCT116 a HT29 obohacuje soubor nástrojů, které mají výzkumní pracovníci k dispozici, a umožňuje jemnější zkoumání mnohostranné povahy kolorektálního karcinomu.
Manipulace s buňkami HCT116
|
Doba zdvojení: |
Doba zdvojení nádorových buněk HCT116 se pohybuje od 25 do 35 hodin. |
|
Adherentní nebo v suspenzi: |
Buněčná linie rakoviny tlustého střeva HCT116 je adherentní, buňky rostou v monovrstvách. |
|
Hustota výsevu: |
Pro buněčnou kulturu HCT116 se doporučuje hustota výsevu 2 x104 buněk/cm2. Pro subkultivaci by měly být buňky odděleny pomocí roztoku Accutase po promytí 1x PBS. Po odstředění se buněčná peleta resuspenduje v čerstvém růstovém médiu a přenese se do nové baňky. |
|
Růstové médium: |
Pro kultivaci buněk HCT116 je optimální médium McCoys 5a doplněné 3,0 g/l L-glukózy, 1,5 mM L-glutaminu, 3,0 g/l NaHCO3 a 10% fetálního hovězího séra. Doporučuje se obnovovat médium 1 až 2krát týdně. |
|
Růstové podmínky (teplota,CO2): |
Kultivace probíhá ve zvlhčeném inkubátoru při teplotě 37 °C s 5% koncentracíCO2. |
|
Skladování: |
Buňky HCT116 lze skladovat při teplotách nižších než -150 °C v parní nebo kapalné fázi tekutého dusíku. |
|
Postup zmrazování a médium: |
Pro kryokonzervaci použijte médium CM-1 nebo CM-ACF. Doporučuje se metoda mrazení s řízenou rychlostí, která umožňuje postupné snižování teploty o 1 °C za minutu, což pomáhá zachovat životaschopnost buněk. |
|
Postup rozmrazování: |
Rozmrazování buněk HCT116 ve vodní lázni o teplotě 37 °C. Po přidání růstového média odstřeďte, abyste odstranili zbytky zmrazovacího média. Resuspendujte buněčné pelety v čerstvém médiu a kultivujte v nových baňkách. |
|
Úroveň biologické bezpečnosti: |
Úroveň bezpečnosti: 1 |
Výhody buněčné linie HCT116
Tento oddíl se zabývá buněčnou linií HCT116, zdůrazňuje její klíčovou roli ve výzkumu rakoviny, zejména ve studiu kolorektálního karcinomu, a diskutuje o jejích inherentních výhodách.
Buněčná linie HCT116 vyniká ve výzkumu rakoviny několika klíčovými výhodami:
Model kolorektálního karcinomu: Slouží jako široce uznávaný in vitro model kolorektálního karcinomu, třetího nejčastějšího nádorového onemocnění na světě. Díky svému významu pro napodobení lidského kolorektálního karcinomu je neocenitelná pro pochopení biologie rakoviny a testování terapeutických strategií.
Homogenita: Pozoruhodné je, že přibližně 70 % buněk HCT116 vykazuje konzistentní genetické profily, což představuje relativně homogenní populaci. Tato homogenita má zásadní význam pro studie zaměřené na genovou expresi, buněčné signální dráhy a hodnocení účinnosti léčby léky, protože zajišťuje konzistenci a spolehlivost výsledků experimentů.
Účinnost transfekce: Jedním z charakteristických rysů buněk HCT116 je jejich vysoká schopnost transfekce, zejména virovými vektory. Tato vlastnost je zvláště výhodná ve výzkumu genové terapie, protože umožňuje účinné a přesné vnášení genetického materiálu, a tím usnadňuje pokročilé genetické manipulace a funkční studie.
Pokračujte ve svých objevech s naší ověřenou buněčnou linií HCT116
Výzkumné využití buněčné linie HCT116
Buněčná linie HCT116 má širokou škálu využití ve výzkumu rakoviny. Některé významné aplikace jsou:
Biologie rakoviny
Buněčná linie HCT116 se používá ke studiu progrese a vývoje rakoviny tlustého střeva. Kromě toho pomáhá objasnit základní mechanismy a signální dráhy, které se podílejí na proliferaci, migraci a invazi rakoviny. Studie použila buňky HCT116 ke studiu genů podílejících se na vývoji rezistence vůči lékům. Výzkumníci nadměrně exprimovali gen MDR1 v buňkách rakoviny tlustého střeva a pozorovali expresi izoforem NOX (NADPH oxid) a Nrf2. Studie odhalila, že zvýšená regulace NOX2 a Nrf2 způsobuje chemorezistenci rakovinných buněk; tyto geny tedy mohou být cíleny k překonání rozvoje rezistence během léčby rakoviny [1]. Podobně výzkum provedený v roce 2021 uvádí, že signální dráha NF-κB se podílí na regulaci proliferace a migrace rakoviny tlustého střeva. Lze ji tedy zacílit k vývoji nových a účinných terapeutik proti kolorektálnímu karcinomu [2].
V oblasti onkologie má zásadní význam pochopení složitých procesů buněčného cyklu, proliferace a růstu a apoptózy. Tyto biologické funkce jsou stěžejní při studiu lidských buněčných linií, zejména těch odvozených z maligních buněk, jako jsou buňky lidského karcinomu tlustého střeva a modely karcinomu pankreatu. Například buněčné linie HCT116 a SW620 mají zásadní význam pro zkoumání mechanismů, které jsou základem rakoviny tlustého střeva a slinivky břišní. Pomocí technik, jako je průtoková cytometrie a klonogenní testy, mohou vědci objasnit profily genové exprese a chování nezávislých buněk v nádorech, což vrhá světlo na to, jak rakovina komunikuje v extracelulární matrix.
Úloha apoptózy v progresi rakoviny
Apoptóza neboli programovaná buněčná smrt hraje klíčovou roli při udržování buněčné homeostázy a je klíčovou oblastí studia ve výzkumu rakoviny. Zásadní je rozlišení mezi nepříbuznou apoptózou a apoptózou specificky vyvolanou v kontextu rakoviny, jako je například buněčná smrt rakoviny tlustého střeva. Tento proces nespočívá pouze v eliminaci buněk, ale zahrnuje komplexní souhru signálů, které mohou ovlivnit růst nádoru a metastazování. Zkoumáním apoptózy a buněčné smrti ve spojení se supresory metastáz a aktivitou nádorových supresorů mohou vědci získat přehled o cestách, které regulují progresi rakoviny a její metastatický potenciál.
Metastázy a molekulární markery u rakoviny
Metastázy zůstávají jedním z nejhrozivějších aspektů rakoviny, přičemž hematogenní metastázy představují významný problém při šíření zhoubných buněk. Zkoumání metastáz zahrnuje studium pohybových a invazivních schopností nádorových buněk neboli buněčné lokomoce a způsobu interakce buněk s jejich okolím, včetně extracelulární matrix. Molekulární markery, jako je exprese CD133 a receptoru pro epidermální růstový faktor, mají zásadní význam pro identifikaci a pochopení chování pozitivních buněk karcinomu tlustého střeva a dalších typů rakoviny. Například dráha SIRT6 se stala předmětem zájmu kvůli své potenciální roli v modulaci růstu nádorů a metastazování rakoviny tlustého střeva.
Toxikologie/vývoj léčiv
Buněčná linie HCT116 se používá jako model pro screening nových léků proti rakovině. Bylo provedeno několik studií k posouzení účinnosti a toxicity protinádorových léčiv, včetně přírodních produktů a chemicky syntetizovaných nanočástic. Výzkum jako takový hodnotil cytotoxicitu syntetizovaných nanočástic stříbra z výtažků rostlinné drogy Caesalpinia pulcherrima v buňkách HCT116 [3]. Ve studii vědci použili rakovinnou buněčnou linii HCT116 k hodnocení protinádorového potenciálu vodného extraktu kakaového čaje. Zjistili, že extrakt z kakaového čaje snižuje proliferaci rakoviny tlustého střeva a vyvolává buněčnou smrt [4]. V další studii byly použity rakovinné buňky HCT116 a bylo zjištěno, že extrakty zbramboříku vzdušného, Dioscorea bulbifera, vykazují proapoptotickou aktivitu u buněk kolorektálního karcinomu prostřednictvím aktivace signální kaskády JNK a potlačení genu ERK1/2 [5].
Účinky metforminu na nádorové buňky, zejména v souvislosti s rakovinou tlustého střeva a slinivky břišní, jsou příkladem toho, jak může pochopení biologických funkcí nádorových buněk vést k potenciálním terapeutickým strategiím. Výzkum klonogenního přežívání neboli schopnosti rakovinných buněk vytvářet klony při léčbě látkami, jako je metformin, nebo při cílení na specifické dráhy, jako je receptor pro epidermální růstový faktor, může poskytnout cenné poznatky o účinné léčbě rakoviny. Použití klonů HCT116 a buněčných populací HCT116 v těchto studiích navíc umožňuje lépe pochopit, jak nádorové buňky reagují na různé terapeutické zásahy, což otevírá cestu k personalizovanějším přístupům k léčbě rakoviny.
Buňky HCT116: Výzkumné publikace
V tomto oddíle bude rozebráno několik významných a nejcitovanějších publikací z poslední doby, které se týkají buněčné linie HCT116.
Tato studie byla publikována v časopise Journal of Photochemistry and Photobiology B: Biology (2017). Výzkumníci použili buněčné linie rakoviny tlustého střeva HCT116 a rakoviny plic A549 k hodnocení cytotoxických účinků nanočástic oxidu cíničitého syntetizovaných ze semen piperu nigrum.
Tento výzkum v časopise Cancer Letters (2018) navrhuje, že lncRNA SNHG15 podporuje migraci buněk rakoviny tlustého střeva v buněčných liniích kolorektálního karcinomu, včetně HCT116.
Nadměrná exprese dlouhé nekódující RNA TUG1 podporuje progresi rakoviny tlustého střeva
Tento článek byl publikován v časopise Medical Science Monitor v roce 2016. Studie zjistila, že onkogenní LncRNA TUG1 podporuje proliferaci a migraci buněk rakoviny tlustého střeva HCT116.
Tento výzkum v časopise Biochemical Pharmacology (2018) navrhuje, že rozvoj lékové rezistence zvyšuje hladinu enzymů produkujících H2S v buňkách rakoviny tlustého střeva HCT116.
Tento výzkumný článek v časopise International Journal of Environmental Health Research (2023) navrhuje, že extrakt z Inula viscosa L. působí protinádorově na buňky kolorektálního karcinomu HCT116 prostřednictvím regulace mikroRNA.
Zdroje pro buňky HCT116
Níže je uvedeno několik zdrojů o buňkách HCT116.
- Transfekce buněk HCT116: Toto video je průvodcem krok za krokem pro transfekci nádorových buněk HCT116.
- Kultivace buněčné linie HCT116: Toto video ukazuje protokol subkultivace buněčné linie rakoviny tlustého střeva HCT116.
- Subkultivace buněčné linie HCT116: Tato webová stránka obsahuje mnoho užitečných informací o kultivačním médiu HCT116. Kromě toho poskytuje postupy pro zmrazení, rozmrazení a subkultivaci buněk.
Často kladené otázky o buňkách HCT116
odkazy
- Waghela, B.N., F.U. Vaidya a C. Pathak: Upregulace NOX-2 a Nrf-2 podporuje rezistenci vůči 5-fluorouracilu u buněk lidského karcinomu tlustého střeva (HCT-116 ). Biochemie (Moskva), 2021, 86, s. 262-274.
- Yang, M., a další, Astragalin inhibuje proliferaci a migraci buněk lidského karcinomu tlustého střeva HCT116 regulací signální dráhy NF-κB. Frontiers in Pharmacology, 2021, 12: s. 639256.
- Deepika, S., C.I. Selvaraj a S.M. Roopan, Screening bioaktivity Caesalpinia pulcherrima L. swartz a cytotoxicity extraktu syntetizovaných nanočástic stříbra na buněčné linii HCT116. Materials Science and Engineering, C, 2020, 106, s. 110279.
- Gao, X., et al., Kakaový čaj (Camellia ptilophylla) indukuje mitochondriálně závislou apoptózu v buňkách HCT116 prostřednictvím tvorby ROS a signální dráhy PI3K/Akt. Food Research International, 2020, 129, s. 108854.
- Hidayat, A.F.A., et al., Dioscorea bulbifera indukovala apoptózu prostřednictvím inhibice ERK 1/2 a aktivace signální dráhy JNK v buňkách lidského kolorektálního karcinomu HCT116. Biomedicine & Pharmacotherapy, 2018. 104: p. 806-816.