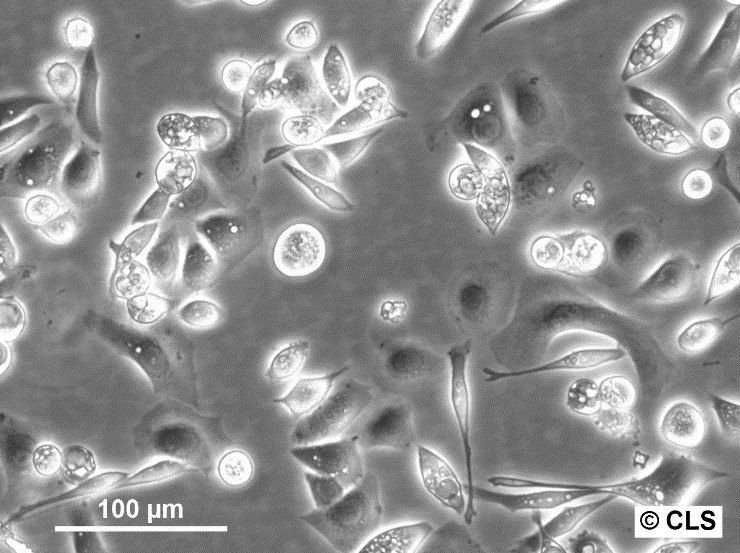
Buňky AGS - Výzkum buněk AGS žaludečního adenokarcinomu ve studiích rakoviny
BuňkyAGS představují buněčnou linii lidského adenokarcinomu žaludku, která se široce používá v biomedicínském výzkumu. Využívá se zejména ke studiu biologie rakoviny žaludku, včetně růstu, vývoje, progrese a terapeutických zásahů. Kromě toho se používá ke zkoumání interakcí mezi hostitelem a patogenem.
Tento článek pojednává o základech žaludečních epiteliálních buněk AGS. Zejména se bude zabývat:
- Obecnou charakteristiku a původ AGS buněk
- Informace o kultivaci buněčné linie AGS
- Buněčné linie AGS: Výhody a omezení
- Aplikace buněk AGS
- Výzkumné publikace o buněčné linii AGS
- Zdroje pro buněčnou linii AGS: Protokoly, videa a další zdroje pro AGS
1.obecná charakteristika a původ buněk AGS
Než začnete s buněčnou linií pracovat, je nutné znát její původ a obecné vlastnosti. V této části se budeme zabývat následujícími informacemi: Co jsou buňky AGS? Jaký je původ buněk AGS? Jaká je morfologie nádorové buněčné linie AGS?
- Buněčná linie AGS byla odvozena ze žaludeční tkáně 54leté bělošky s adenokarcinomem žaludku. Byla izolována v roce 1979 [1].
- Buňky AGS mají morfologii podobnou epitelu.
- Žaludeční epiteliální buňky AGS jsou hyperdiploidní. Modální počet chromozomů pro buňky AGS je 49, což se vyskytuje téměř u 60 % buněk. Polyploidie se vyskytuje také přibližně u 3,6 % buněk.
2.informace o kultivaci buněčné linie AGS
Pro správnou manipulaci a správu buněčné linie je třeba znát její základní kultivační koncepty. Zejména byste se měli naučit: Jaká je doba zdvojení buněk AGS? Co je to buněčné médium AGS? Jak se provádí subkultivace buněk AGS? Jaká mrazicí média se používají pro žaludeční epiteliální buňky AGS?
Klíčové body pro kultivaci buněk AGS
|
Doba zdvojení: |
Doba zdvojení buněk AGS se pohybuje mezi 24 a 48 hodinami. |
|
Adherentní nebo v suspenzi: |
AGS buňky jsou adherentní. Rostou do monovrstev. |
|
Hustota výsevu: |
Hustota výsevu buněk AGS je 1 x104 buněk/cm2. Při této hustotě vytvoří buňky splývající monovrstvu za 3 až 5 dní. Po odstranění starého média se buňky propláchnou 1 x PBS a inkubují se s disociačním roztokem Accutase. Oddělené buňky byly resuspendovány v kultivačním médiu a odstředěny. Buněčná peleta byla opět resuspendována a po spočítání AGS buněk se dávkuje do nové baňky k růstu. |
|
Růstové médium: |
Ke kultivaci buněk AGS se používá médium DMEM obsahující 10 % FBS, 4 mM L-Glutamin, 4,5 g/l glukózy, 1,5 g/l NaHCO3 a 1,0 mM pyruvát sodný. Médium by se mělo vyměňovat 2 až 3krát týdně. |
|
Růstové podmínky: |
AGS buňky se uchovávají ve zvlhčeném inkubátoru (při teplotě 37 °C) s 5% přívodem CO2. |
|
Skladování: |
Zmrazené buňky AGS se uchovávají v elektrických mrazničkách při teplotě nižší než -150 °C nebo delší dobu v plynné fázi tekutého dusíku. |
|
Postup zmrazování a médium: |
Ke zmrazení buněk AGS se používá médium CM-1 nebo CM-ACF. Zmrazování buněk se provádí pomalým zmrazovacím procesem, který umožňuje pokles teploty pouze o 1 °C za minutu a chrání životaschopnost buněk. |
|
Proces rozmrazování: |
Zmrazené žaludeční epiteliální buňky se rychle míchají ve vodní lázni o teplotě 37 °C po dobu 40 až 60 sekund. Rozmražené buňky se resuspendují v čerstvém kultivačním médiu a přelijí se do nových baněk pro růst. Po 24hodinové inkubaci se médium obnoví, aby se odstranily složky zmrazovacího média. Na rozdíl od toho se rozmražené buňky odstředí a prvky mrazicího média se odstraní. Poté se sklizené buňky opět resuspendují a dávkují do baňky obsahující kultivační médium. |
|
Úroveň biologické bezpečnosti: |
Pro kultivaci buněk AGS je nezbytné laboratorní prostředí úrovně biologické bezpečnosti 2. |
3.buněčná linie AGS: Výhody a omezení
V této části článku se dozvíte o některých klíčových výhodách a omezeních spojených s buňkami AGS.
Výhody
Hlavní výhody žaludečních epiteliálních buněk AGS jsou:
|
Snadná kultivace |
Buněčnou linii AGS pro karcinom žaludku lze snadno udržovat v laboratořích pro kultivaci buněk. Nemá žádné složité a náročné požadavky na kultivaci buněk. Navíc vykazuje dobré růstové vlastnosti, což z ní činí ideální volbu pro studium biologie karcinomu žaludku. |
|
Význam pro karcinom žaludku |
Buňky AGS byly odvozeny z lidského adenokarcinomu žaludku, díky čemuž jsou široce využívány ke studiu biologie karcinomu žaludku a terapeutických zásahů. |
Omezení
S buněčnou linií AGS jsou spojena následující omezení:
|
Buněčný model in vitro |
Buňky AGS jsou kultivovány v laboratořích biomedicínského výzkumu za umělých podmínek. Proto nemusí plně kopírovat mikroprostředí karcinomu žaludku in vivo a další buněčné a molekulární interakce. |
4.aplikace buněk AGS
Buňky AGS se používají speciálně ke studiu biologie rakoviny žaludku. Mají mnoho dalších slibných aplikací v biomedicíně. Některé ze zajímavých výzkumných aplikací AGS buněk jsou:
- Studium rakoviny žaludku: AGS buňky jsou vynikajícím výzkumným nástrojem pro zkoumání buněčných a molekulárních mechanismů, které jsou základem růstu, metastazování a invaze rakoviny žaludku. Vědci také využívají žaludeční epiteliální AGS buňky ke studiu různých buněčných procesů, genetických mutací a signálních drah při vývoji rakoviny žaludku. Studie Oncology Reports (2019) zjistila, že mikroRNA-183-5p.1 podporuje proliferaci, migraci a invazi nádorových buněk tím, že inhibuje signální kaskádu Bcl 2/P53. Kromě toho také snižuje regulaci genu TPM1, čímž tyto účinky uplatňuje. MikroRNA i TPM1 jsou tedy navrhovány jako účinné molekulární cíle pro vývoj cílené terapie proti rakovině žaludku [2].
- Screening léčiv: AGS buňky se běžně používají ke screeningu nových a účinných léčiv proti rakovině žaludku. Výzkumníci hodnotí cytotoxicitu a účinnost potenciálních léčiv pomocí buněčné linie AGS. Byly také provedeny studie zaměřené na identifikaci nových molekulárních cílů a vývoj nových cílených terapií pro boj s karcinomy žaludku. Výzkum prováděný v roce 2021 využíval buňky AGS karcinomu žaludku a studoval terapeutický účinek léčiva paklitaxel. Výsledky odhalily, že paklitaxel vyvolává mitotickou katastrofu, což je nedílný mechanismus apoptózy neboli buněčné smrti v buňkách AGS. Kromě toho také podporoval autofagii v buňkách karcinomu žaludku [3].
- Interakce mezi hostitelem a patogenem: Na nádorové buněčné linii AGS se také studují interakce mezi hostitelem a patogenem. To pomáhá vědcům pochopit buněčné mechanismy a reakce, které se podílejí na infekci. Například studie provedená v roce 2020 pozorovala, že malé nekódující RNA přítomné ve vezikulech vnější membrány Helicobacter pylori snižují sekreci interleukinu 8 v lidských AGS buňkách [4].
5.výzkumné publikace o buněčné linii AGS
V této části článku se budeme věnovat několika zajímavým a nejcitovanějším výzkumným publikacím, které se týkají buněk AGS.
Tato studie v časopise Biomedicine & Pharmacotherapy (2020) navrhla, že salidrosid, přírodní sloučenina, indukuje ochrannou autofagii a buněčnou smrt v buňkách žaludečního epitelu AGS prostřednictvím modulace signální dráhy PI3K/AKT/mTOR.
Tato studie byla publikována v časopise Biomedicine & Pharmacotherapy (2018). Zkoumala synergické protinádorové účinky polysacharidu astragalu a léčiva apatinibu v buňkách AGS. Výsledky studie odhalily, že astragalus zvyšuje protinádorové účinky apatinibu prostřednictvím potlačení signalizace AKT.
Tento výzkum v časopise Journal of Ethnopharmacology (2018) navrhl, že kurkuzedoalid, přírodní sloučenina z rostliny Curcuma zedoaria Roscoe, přispívá k jejímu cytotoxickému potenciálu vůči buňkám AGS.
Nadměrná exprese FOXA1 inhibuje buněčnou proliferaci a EMT buněk lidského karcinomu žaludku AGS
Tato publikace v časopise Gene (2018) navrhla, že upregulace FOXA1 potlačuje proliferaci buněk žaludečního adenokarcinomu AGS a přechod z epitelu na mezenchym (EMT) a invazi.
Tento výzkumný článek byl publikován v časopise International Journal of Medical Microbiology v roce 2020. V této studii byly ke studiu interakcí mezi hostitelem a patogenem použity buňky AGS. Výsledky odhalily, že Helicobacter pylori obsahuje ve svých vezikulech vnější membrány některé nekódující RNA, které ovlivňují hladiny IL-8 v buňkách AGS.
6.zdroje pro buněčnou linii AGS: Protokoly, videa a další zdroje pro AGS
Níže je uvedeno několik zdrojů, které se týkají buněk AGS.
- Protokol transfekce buněk AGS: Toto video je postupným průvodcem při výuce protokolu transfekce žaludečních epiteliálních buněk AGS.
Následující odkaz obsahuje protokol kultivace buněk AGS.
- Protokol kultivace buněk AGS: Tato webová stránka obsahuje užitečné informace o médiích a protokolech kultivace buněk AGS. Stručně řečeno, poskytuje protokol pro subkultivaci žaludečních epiteliálních AGS buněk a manipulaci s proliferujícími a kryokonzervovanými AGS kulturami.
- Subkultivace buněk AGS: Tato stránka podrobně vysvětluje postup subkultivace buněk AGS.
Odkazy
- Phuc, B.H., et al., Comparative genomics of two Vietnamese Helicobacter pylori strains, CHC155 from a non-cardia gastric cancer patient and VN1291 from a duodenal ulcer patient. Scientific Reports, 2023. 13(1): p. 8869.
- Lin, J., et al., miRNA-183-5p. 1 podporuje migraci a invazi buněk karcinomu žaludku AGS tím, že se zaměřuje na TPM1 Corrigendum in/10.3892/or. 2020.7902. Oncology reports, 2019. 42(6): p. 2371-2381.
- Khing, T.M., a další, Vliv paklitaxelu na apoptózu, autofagii a mitotickou katastrofu u buněk AGS. Scientific Reports, 2021. 11(1): p. 23490.
- Zhang, H., et al., sncRNA zabalené vezikuly vnější membrány Helicobacter pylori tlumí sekreci IL-8 v lidských buňkách. International Journal of Medical Microbiology, 2020. 310(1): p. 151356.