Cellule U2OS-CRISPR-SNAPf-SEH1
800,00 €*
I prodotti vengono spediti congelati in ghiaccio secco in criotubi. Ogni criotubo contiene in genere 3 × 10 6 cellule per le linee aderenti o 5 × 106 cellule per le linee in sospensione (per ulteriori dettagli, consultare il certificato di analisi del lotto).
Informazioni generali
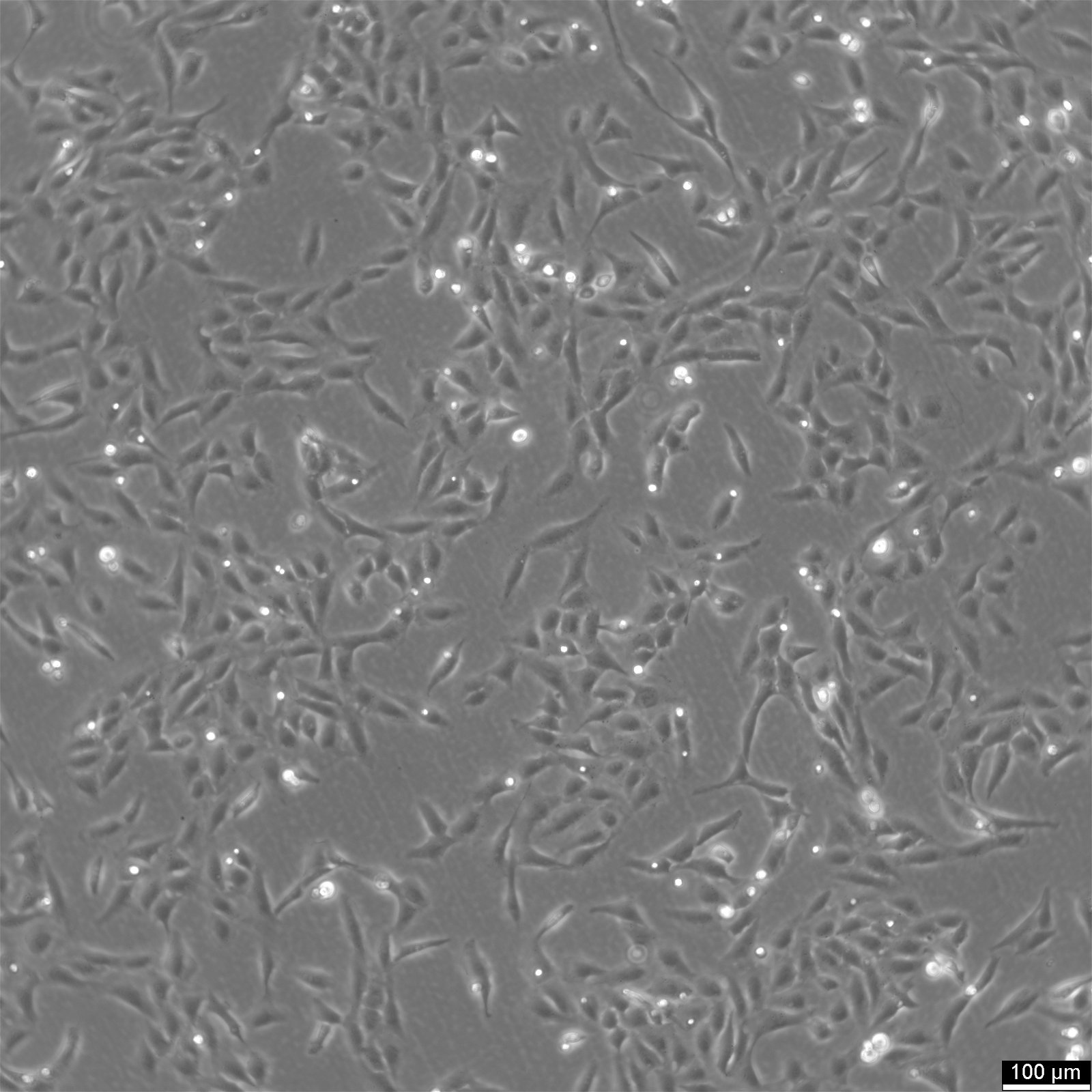
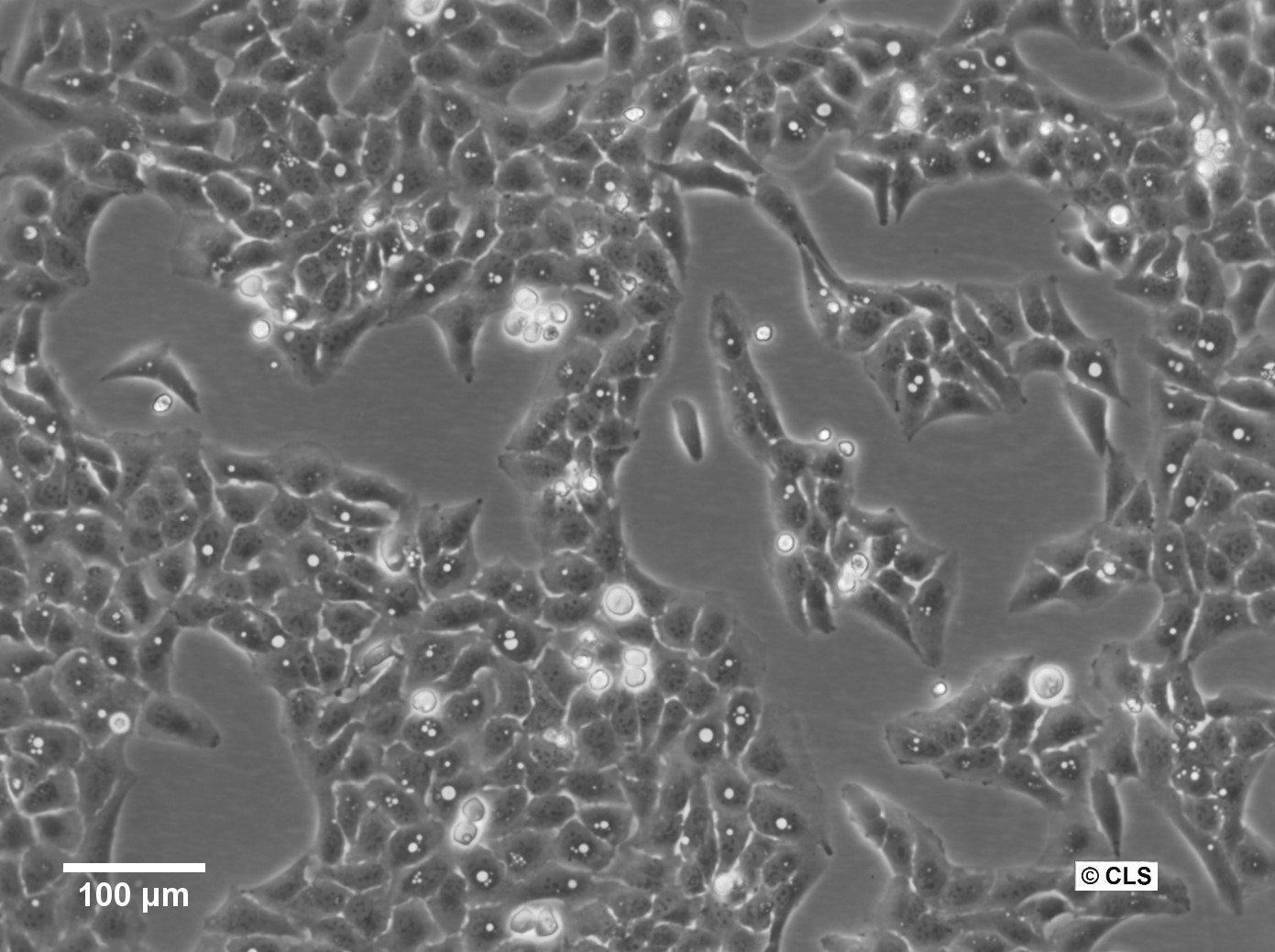
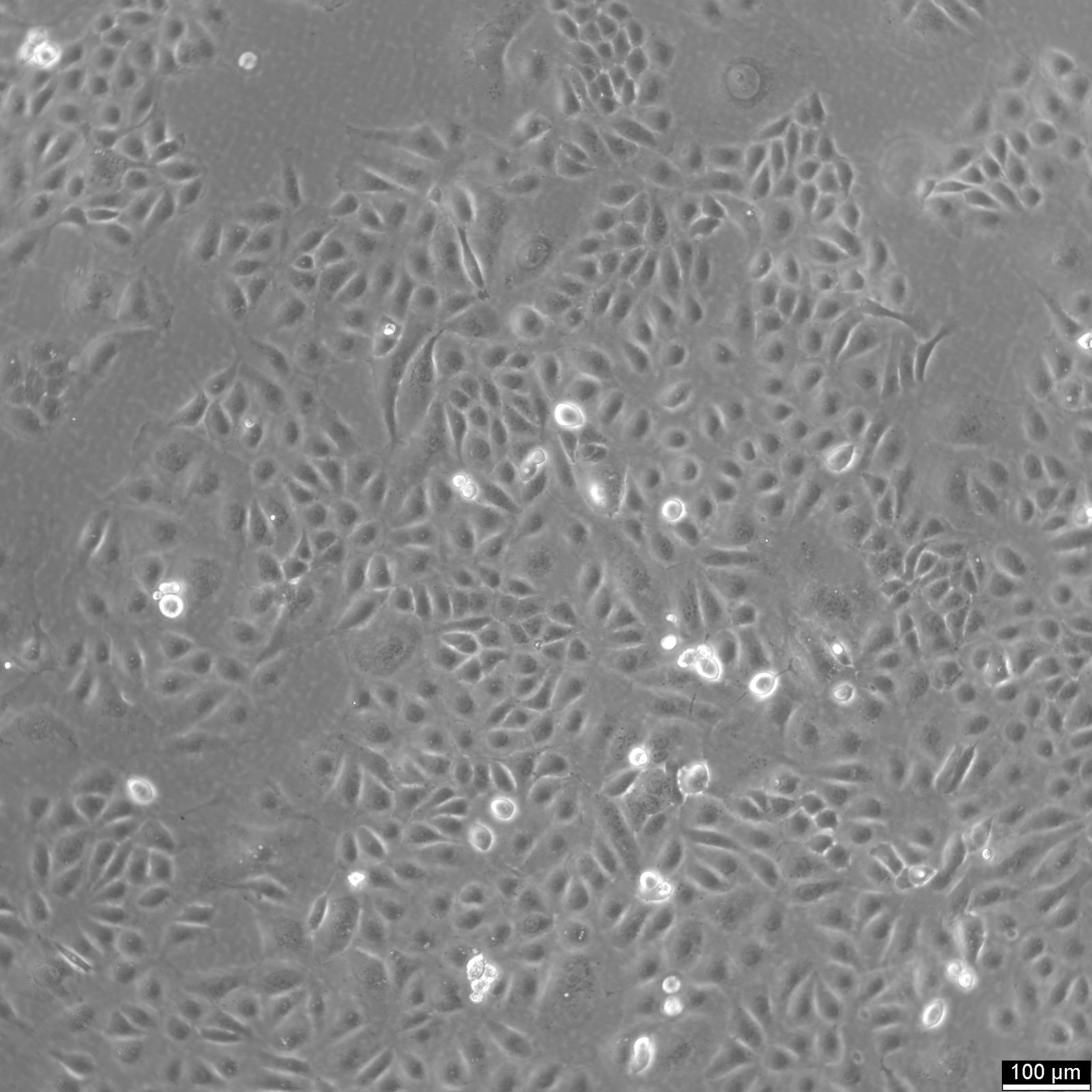
| Descrizione | U2OS-CRISPR-SNAPf-SEH1 è una linea cellulare di osteosarcoma umano modificata genomicamente derivata dalle cellule U2OS in cui il gene endogeno SEH1L (SEH1) è stato modificato utilizzando la tecnologia CRISPR/Cas9 per codificare un tag SNAPf in-frame. SEH1 è un componente del complesso Y (noto anche come complesso NUP107-160), un modulo strutturale centrale del complesso dei pori nucleari (NPC) che contribuisce all'assemblaggio e alla stabilità dell'impalcatura dei pori. Inserendo la sequenza codificante SNAPf nel locus endogeno, la proteina SEH1 marcata viene espressa sotto il controllo regolatorio nativo, preservando i livelli di espressione fisiologica e riducendo al minimo le perturbazioni della composizione dei pori nucleari. Il tag SNAPf è una variante ingegnerizzata e a reazione rapida del tag SNAP che si lega in modo covalente ai substrati coniugati con benzilguanina, consentendo una marcatura fluorescente selettiva e stabile in cellule vive o fissate. Nelle cellule U2OS-CRISPR-SNAPf-SEH1, la proteina di fusione si localizza nell'involucro nucleare con un pattern puntiforme caratteristico della distribuzione dell'NPC. Poiché l'etichettatura avviene a livelli proteici endogeni, questo sistema è particolarmente adatto per la microscopia a fluorescenza quantitativa, l'imaging a super risoluzione e le analisi di tracciamento di singole particelle volte a sezionare l'organizzazione e la stechiometria degli NPC. La morfologia piatta e i nuclei grandi delle cellule U2OS facilitano ulteriormente la visualizzazione ad alta risoluzione delle strutture dell'involucro nucleare. SEH1 partecipa alla biogenesi NPC ed è stato anche implicato nei processi associati al cinetocoro durante la mitosi. Di conseguenza, questa linea cellulare fornisce una solida piattaforma per lo studio dell'assemblaggio e del disassemblaggio NPC dipendente dal ciclo cellulare, dell'organizzazione spaziale del complesso Y all'interno dello scaffold poroso e dei potenziali ruoli duali di SEH1 nell'involucro nucleare e nei cinetocori mitotici. U2OS-CRISPR-SNAPf-SEH1 consente studi meccanicistici dell'architettura e della dinamica dei pori nucleari in condizioni di espressione fisiologicamente rilevanti. |
|---|---|
| Organismo | Umano |
| Tessuto | Osso |
| Malattia | Osteosarcoma |
Caratteristiche
| Età | 15 anni |
|---|---|
| Genere | Donna |
| Etnia | Caucasico |
| Morfologia | Simile all'epitelio |
| Proprietà di crescita | Aderente |
Dati normativi
| Citazione | U2OS-CRISPR-SNAPf-SEH1 (numero di catalogo Cytion 300664) |
|---|---|
| Livello di biosicurezza | 1 |
| NCBI_TaxID | 9606 |
| Depositante | Il laboratorio Ellenberg (EMBL) |
| Stato degli OGM | GMO-S1: questa linea cellulare di osteosarcoma umano (U2OS-CRISPR-SNAPf-SEH1) contiene una fusione SNAPf-SEH1 mediata da CRISPR che consente l'etichettatura selettiva della nucleoporina SEH1. La modifica è presente in modo stabile. Questa classificazione si applica solo in Germania e può differire altrove. |
Dati biomolecolari
| Espressione proteica | SEH1, tag SNAPf |
|---|
Manipolazione
| Terreno di coltura | McCoys 5a, w: 3,0 g/L Glucosio, w: Glutammina stabile, w: 2,0 mM Sodio piruvato, w: 2,2 g/L NaHCO3 (articolo Cytion numero 820200a) |
|---|---|
| Integratori | Integrare il terreno di coltura con 10% FBS, 3,0 g/L di glucosio, Glutammina stabile, 2,0 mM di piruvato di sodio, 2,2 g/L di NaHCO3, 1% di NEAA |
| Reagente di dissociazione | Accutase |
| Sottocoltura | Rimuovere il vecchio terreno dalle cellule aderenti e lavarle con PBS privo di calcio e magnesio. Per le fiasche T25, utilizzare 3-5 ml di PBS e per le fiasche T75, 5-10 ml. Quindi, coprire completamente le cellule con Accutase, utilizzando 1-2 ml per le fiasche T25 e 2,5 ml per le fiasche T75. Lasciare incubare le cellule a temperatura ambiente per 8-10 minuti per staccarle. Dopo l'incubazione, mescolare delicatamente le cellule con 10 ml di terreno per risospenderle, quindi centrifugare a 300xg per 3 minuti. Scartare il surnatante, risospendere le cellule in terreno fresco e trasferirle in nuove fiasche contenenti terreno fresco. |
| Prodotto da congelare | Come terreno di crioconservazione, utilizziamo un terreno di crescita completo (incluso FBS) + 10% DMSO per un'adeguata vitalità post-scongelamento, o CM-1 (numero di catalogo Cytion 800100), che include osmoprotettori e stabilizzatori metabolici ottimizzati per migliorare il recupero e ridurre lo stress crio-indotto. |
| Scongelamento e coltura delle cellule |
|
| Atmosfera di incubazione | 37°C, 5%CO2, atmosfera umidificata. |
| Rivestimento del pallone | Nessuno |
| Procedura di congelamento | Le linee cellulari crioconservate vengono spedite su ghiaccio secco in confezioni isolate e convalidate, con una quantità di refrigerante sufficiente a mantenere circa -78 °C durante il trasporto. Al ricevimento, ispezionare immediatamente il contenitore e trasferire immediatamente le fiale in un luogo di conservazione appropriato. |
| Condizioni di spedizione | Le linee cellulari crioconservate vengono spedite su ghiaccio secco in confezioni isolate e convalidate, con una quantità di refrigerante sufficiente a mantenere circa -78 °C durante il trasporto. Al ricevimento, ispezionare immediatamente il contenitore e trasferire immediatamente le fiale in un luogo di conservazione appropriato. |
| Condizioni di conservazione | Per la conservazione a lungo termine, porre le fiale in azoto liquido in fase vapore a una temperatura compresa tra -150 e -196 °C circa. La conservazione a -80 °C è accettabile solo come breve fase intermedia prima del trasferimento in azoto liquido. |
Controllo di qualità / Profilo genetico / HLA
| Sterilità | La contaminazione da micoplasma viene esclusa utilizzando sia saggi basati sulla PCR sia metodi di rilevamento del micoplasma basati sulla luminescenza. Per garantire l'assenza di contaminazione batterica, fungina o da lieviti, le colture cellulari sono sottoposte a ispezioni visive quotidiane. |
|---|
Accordo con terzi
Si prega di notare che questa linea cellulare non è disponibile con un MTA standard di Cytion, in quanto richiede un accordo di terze parti e/o è soggetta a negoziazione con il licenziante originale.-
Prodotti richiesti
Prodotti richiesti
Terreno di congelamento CM-1 - 50 mlVarianti dei mezzi di crioconservazione: 50 mlIl Freeze Medium CM-1 di Cytion è un mezzo di crioconservazione all'avanguardia, progettato per garantire il massimo livello di vitalità e funzionalità delle cellule dopo il disgelo. Questo terreno versatile è adatto a un ampio spettro di tipi di cellule, comprese quelle umane e animali, ed è quindi uno strumento essenziale per diverse applicazioni di ricerca. Formulato con una combinazione meticolosamente bilanciata di crioprotettori e nutrienti essenziali, Freeze Medium CM-1 riduce al minimo la formazione di cristalli di ghiaccio e lo stress cellulare durante il processo di congelamento, preservando così l'integrità cellulare.
Le caratteristiche principali del Freeze Medium CM-1 includono:
Ampia compatibilità: Efficace per un'ampia gamma di tipi di cellule, tra cui cellule primarie, cellule staminali e linee cellulari consolidate.
Alta vitalità: Ottimizzato per massimizzare il recupero e la vitalità delle cellule dopo lo scongelamento, garantendo risultati sperimentali affidabili.
Pronto all'uso: Comodamente preparato e sterilizzato per l'applicazione immediata, riducendo i tempi di preparazione e il rischio di contaminazione.
Maggiore stabilità: Mantiene prestazioni costanti in condizioni di crioconservazione standard, garantendo risultati riproducibili.
Lunga durata di conservazione: CM-1 è un terreno di crioconservazione contenente siero, pronto all'uso, che può essere conservato in frigorifero fino a un anno.
Uso del CM-1 per il congelamento delle cellule
Per utilizzare CM-1 per il congelamento di cellule aderenti e in sospensione, procedere come segue
Per le cellule aderenti, lavarle e dissociarle dal substrato di coltura. Per le cellule in sospensione, passare direttamente alla fase successiva.
Contare le cellule per assicurarsi che siano alla giusta concentrazione.
Centrifugare le cellule per pellettizzarle, quindi risospenderle nel terreno di coltura CM-1.
Trasferire le cellule risospese in crioviali.
Utilizzare un metodo di congelamento lento prima di trasferire le cellule alla conservazione a lungo termine
Metodo
Descrizione
Passi
❄️
Congelamento manuale
Un metodo graduale che prevede una riduzione graduale della temperatura per garantire la vitalità delle cellule
1️⃣ Mettere le cellule nel terreno di coltura in un congelatore a 4°C per 40 minuti.
2️⃣ Trasferire in un congelatore a -80°C per 24 ore.
3️⃣ Conservare le cellule in azoto liquido per la conservazione a lungo termine
❄️
Utilizzo di Mr. Frosty
Un comodo dispositivo che consente di controllare la velocità di congelamento senza l'uso di energia elettrica
1️⃣ Preparare le cellule in crioviali con terreno di congelamento.
2️⃣ Collocare le crioviali nel contenitore Mr. Frosty.
3️⃣ Conservare a -80°C per 24 ore prima di trasferire in azoto liquido
❄️
Congelatore a velocità controllata
Un congelatore di alta precisione di Thermo Fisher o di altri produttori progettato per la riduzione controllata della temperatura
1️⃣ Programmare il dispositivo per ridurre gradualmente la temperatura.
2️⃣ Collocare le cellule preparate nel congelatore.
3️⃣ Dopo il ciclo di congelamento, trasferire le cellule in azoto liquido
Conservare le crioviali a temperature inferiori a -130°C o in azoto liquido per la conservazione a lungo termine.
Ingredienti
Contiene FBS, DMSO, Glucosio, Sali
Capacità tampone: pH = 7,2
- 7,6
Il terreno di congelamento CM-1 di Cytion offre una soluzione affidabile per la crioconservazione, garantendo un'elevata vitalità cellulare e funzionalità dopo il disgelo per un'ampia gamma di applicazioni di ricerca.59,00 €*Terreno McCoys 5A (modificato), w: 3,0 g/L Glucosio, w: Glutammina stabile, w: 2,0 mM Sodio piruvato, w: 2,2 g/L NaHCO3Il McCoy's 5A Medium è un terreno di coltura altamente raccomandato e specializzato, progettato per facilitare la crescita e la replicazione dei virus nelle colture cellulari primarie. Ha ottenuto un riconoscimento significativo per le sue eccezionali prestazioni in varie applicazioni di ricerca biologica. Un'applicazione di rilievo del McCoy's 5A Medium è il suo utilizzo nella coltura di linee cellulari di carcinoma del colon umano. Nello specifico, è stato impiegato nello studio del recettore accoppiato alla proteina G contenente ripetizioni ricche di leucina (LGR5) e del suo ruolo nella metastasi del cancro al colon. Questo terreno è stato efficacemente impiegato nella coltivazione di diverse linee cellulari di carcinoma del colon, tra cui HCT116, RKO, FET, CBS, HCT116b e TENN, consentendo ai ricercatori di approfondire i meccanismi alla base delle metastasi del cancro del colon. Oltre alla sua applicazione nella ricerca sul cancro, il McCoy's 5A Medium si è dimostrato indispensabile nello studio degli osteoblasti. I ricercatori che studiano la reattività ionica dell'idrossiapatite carente di calcio nei terreni di coltura cellulare standard hanno utilizzato questo terreno per coltivare gli osteoblasti. Questa applicazione ha facilitato una migliore comprensione delle interazioni tra gli osteoblasti e l'idrossiapatite carente di calcio, contribuendo ai progressi nel campo della ricerca sulle ossa. Il McCoy's 5A Medium è stato meticolosamente formulato modificando gli aminoacidi presenti nel Basal Medium Eagle per fornire un supporto ottimale alle cellule tumorali del fegato. Questa formulazione arricchita lo rende adatto a una vasta gamma di linee cellulari consolidate, nonché alle cellule primarie, migliorandone ulteriormente la versatilità e l'applicabilità in vari contesti di ricerca. Il McCoy's 5A Medium estende i suoi effetti biochimici e fisiologici oltre le cellule tumorali del fegato. È stato impiegato con successo per sostenere la crescita in colture primarie di midollo osseo, pelle, gengiva, rene, omento, surrene, polmone, milza, embrione di ratto e altri tipi di cellule. Questa ampia gamma di applicazioni attesta la grande utilità del McCoy's 5A Medium nel sostenere la crescita e il mantenimento di vari tipi di cellule per una ricerca biologica completa. Formulazione Questo McCoy's 5A medium (modificato) contiene 3,0 g/L di glucosio, glutammina stabile, 2,0 mM di piruvato di sodio e 2,2 g/L di NaHCO3. Controllo qualità pH = 7,2 +/
- 0,02 a 20-25 °C. Ogni lotto è stato testato per verificarne la sterilità e l'assenza di micoplasmi e batteri. Conservazione Conservare in frigorifero a una temperatura compresa tra +2 °C e +8 °C al riparo dalla luce. Il congelamento e il riscaldamento fino a +37 °C compromettono la qualità del prodotto. Non riscaldare il terreno a temperature superiori a 37 °C né utilizzare fonti di calore incontrollabili (ad es. forni a microonde). Se si intende utilizzare solo una parte del terreno, prelevare la quantità necessaria dalla bottiglia e riscaldarla a temperatura ambiente. La durata di conservazione di qualsiasi terreno, ad eccezione del terreno di base, è di 6-8 settimane dalla data di apertura. Composizione Componenti mg/L Sali inorganiciCloruro di calcio x 2H2O132,00 Solfato di magnesio97,67 Cloruro di potassio400,00 Cloruro di sodio6.460,00 Idrogeno fosfato disodico (anidro)504,00 Altri componentiD(+)-Glucosio (anidro)3.000,00 Glutatione (ridotto)0,50 Peptone di carne600,00 Sale sodico del rosso fenolo11 AminoacidiL-alanina13,36 L-arginina x HCl42,14 L-asparagina x H2O45,03 Acido L-aspartico19,97 L-Cisteina x HCl x H2O31,75 L-glutammina (stabile)219,15 Acido L-glutammico22,07 Glicina7,51 L-istidina x HCl x H2O20,96 L-idrossiprolina19,67 L-isoleucina39,36 L-leucina39,36 L-lisina x HCl36,54 L-metionina14,92 L-fenilalanina16,52 L-Prolina17,27 L-Serina26,28 L-treonina17,87 L-triptofano3,06 Sale disodico della L-tirosina26,10 L-Valina17,57 VitamineAcido p-amminobenzoico1,00 Acido ascorbico0,56 D(+)-biotina0,20 D-calcio pantotenato0,20 Cloruro di colina5,00 Acido folico10,0 Mio-inositolo36,00 Nicotinamide0,50 Acido nicotinico0,5 Piridossal HCl0,50 Piridossina HCl0,50 Riboflavina0,20 Cloridrato di tiamina0,20 Vitamina B122,0030,00 €*AccutaseVarianti: 100 mlReagente di dissociazione cellulare Accutase
- Un'alternativa delicata alla tripsina
Accutase è una soluzione per il distacco delle cellule che sta rivoluzionando il settore delle colture cellulari. Si tratta di una miscela di enzimi proteolitici e collagenolitici che imita l'azione della tripsina e della collagenasi. A differenza della tripsina, Accutase non contiene componenti di mammiferi o batteri ed è molto più delicato per le cellule, il che lo rende una soluzione ideale per il distacco di routine delle cellule dai contenitori di plastica standard per colture di tessuti e dai contenitori di plastica con rivestimento di adesione. In questo post esploreremo i vantaggi e gli usi di Accutase e come sta cambiando il gioco nella coltura cellulare.
Vantaggi di Accutase
Accutase presenta diversi vantaggi rispetto alle soluzioni di tripsina tradizionali. In primo luogo, può essere utilizzato ogni volta che è necessario un distacco delicato ed efficiente di qualsiasi linea cellulare aderente, il che lo rende un sostituto diretto della tripsina. In secondo luogo, Accutase funziona molto bene sulle cellule staminali embrionali e neuronali e ha dimostrato di mantenere la vitalità di queste cellule dopo il passaging. In terzo luogo, Accutase preserva la maggior parte degli epitopi per la successiva analisi in citometria a flusso, rendendola ideale per l'analisi dei marcatori della superficie cellulare.
Inoltre, non è necessario neutralizzare Accutase durante il passaggio di cellule aderenti. L'aggiunta di altro terreno dopo la divisione delle cellule diluisce Accutase in modo che non sia più in grado di staccare le cellule. Ciò elimina la necessità di una fase di inattivazione e fa risparmiare tempo ai tecnici delle colture cellulari. Infine, Accutase non deve essere aliquotato e un flacone è stabile in frigorifero per 2 mesi.
Applicazioni di Accutase
Accutase è un sostituto diretto della soluzione di tripsina e può essere utilizzato per il passaging delle linee cellulari. Inoltre, l'Accutasi è in grado di staccare le cellule per l'analisi di molti marcatori della superficie cellulare mediante citometria a flusso e per lo smistamento cellulare. Altre applicazioni a valle del trattamento con Accutase includono l'analisi dei marcatori della superficie cellulare, il saggio di crescita dei virus, la proliferazione cellulare, i saggi di migrazione delle cellule tumorali, il passaggio cellulare di routine, la scalabilità della produzione (bioreattore) e la citometria a flusso.
Composizione di Accutase
Accutase non contiene componenti di mammiferi o batteri ed è una miscela di enzimi naturali con attività enzimatica proteolitica e collagenolitica. È formulato a una concentrazione molto più bassa rispetto alla tripsina e alla collagenasi, il che lo rende meno tossico e più delicato, ma altrettanto efficace.
Efficacia di Accutase
È stato dimostrato che Accutase è efficiente nel distaccare le cellule primarie e staminali, mantenendo un'elevata vitalità cellulare rispetto agli enzimi di origine animale come la tripsina. il 100% delle cellule viene recuperato dopo 10 minuti e non vi è alcun danno nel lasciare le cellule in Accutase fino a 45 minuti, grazie all'autodigestione di Accutase.
In sintesi
In conclusione, Accutase è una soluzione potente che sta cambiando il gioco della coltura cellulare. Grazie alla sua natura delicata, all'efficienza e alla versatilità, Accutase è l'alternativa ideale alla tripsina. Se siete alla ricerca di una soluzione affidabile ed efficiente per il distacco delle cellule, Accutase è la soluzione che fa per voi.75,00 €*Soluzione antibiotica/antimicotica (100x)Panoramica del prodotto
Volume: 100 ml Conservazione: ≤-15°C Sterilità: Filtrato sterile
Lasoluzione antibiotica/antimicotica (100x) è un concentrato sterile pronto all'uso, progettato per ridurre i rischi di contaminazione microbica nelle colture cellulari e nelle relative applicazioni di laboratorio. Questa soluzione 100x contiene una combinazione consolidata di penicillina, streptomicina e amfotericina B, che fornisce un'attività antimicrobica ad ampio spettro contro batteri Gram-positivi e Gram-negativi, lieviti e funghi filamentosi. La formulazione è adatta all'uso in colture cellulari eucariotiche, terreni di coltura batterici e altri sistemi sensibili alla contaminazione, a sostegno di operazioni di laboratorio pulite e coerenti.
Applicazione e vantaggi Ottimizzata per i protocolli di ricerca di routine, questa soluzione è ampiamente utilizzata per mantenere condizioni asettiche nei flussi di lavoro delle colture cellulari. Offre prestazioni affidabili in ambienti sensibili alla contaminazione, aiutando i ricercatori a ridurre il rischio di crescita microbica senza compromettere la salute delle cellule o la riproducibilità degli esperimenti. La formulazione filtrata sterile elimina la necessità di ulteriori fasi di solubilizzazione, favorendo una preparazione semplificata dei terreni di coltura e riducendo la variabilità delle procedure quotidiane di laboratorio.
Uso e compatibilità Per ottenere concentrazioni standard di lavoro, diluire la soluzione 1:100 nel terreno di coltura completo. Il prodotto è compatibile con un'ampia gamma di linee cellulari di mammifero e di terreni di coltura basali. Grazie alla disponibilità costante delle scorte, i ricercatori possono beneficiare di una continuità di approvvigionamento affidabile e di una pianificazione logistica semplificata. La soluzione deve essere conservata a ≤ -15 °C e protetta da ripetuti cicli di congelamento e scongelamento per mantenerne la stabilità. Solo per uso di ricerca. Non per l'uso in procedure diagnostiche o terapeutiche. Non per uso umano o animale.45,00 €*PBSSoluzione salina tampone con fosfati (PBS)
La soluzione salina fosfato-bufferata (PBS) è una soluzione tampone ampiamente utilizzata nella ricerca biologica e chimica. Svolge un ruolo cruciale nel mantenere l'equilibrio del pH e l'osmolarità durante varie procedure sperimentali, tra cui l'elaborazione dei tessuti e la coltura cellulare. La nostra soluzione PBS è formulata meticolosamente con ingredienti di elevata purezza per garantire stabilità e affidabilità in ogni esperimento. L'osmolarità e le concentrazioni di ioni del nostro PBS imitano fedelmente quelle del corpo umano, rendendolo isotonico e non tossico per la maggior parte delle cellule.
Composizione della nostra soluzione PBS
La nostra soluzione PBS è una miscela regolata in base al pH di tamponi fosfatici e soluzioni saline di grado ultrapuro. A una concentrazione di lavoro 1X, contiene:
8000 mg/L di cloruro di sodio (NaCl)
200 mg/L Cloruro di potassio (KCl)
1150 mg/L Fosfato di sodio bibasico anidro (Na2HPO4)
200 mg/L Fosfato di potassio monobasico anidro (KH2PO4)
Questa composizione garantisce un pH e un equilibrio ionico ottimali, adatti a un'ampia gamma di applicazioni biologiche.
Applicazioni della nostra soluzione PBS
La nostra soluzione PBS è ideale per diverse applicazioni nella ricerca biologica. Le sue proprietà isotoniche e non tossiche la rendono adatta alla diluizione delle sostanze e al risciacquo dei contenitori cellulari. Le soluzioni PBS contenenti EDTA sono efficaci per staccare le cellule attaccate e raggrumate. Tuttavia, i metalli divalenti come lo zinco non devono essere aggiunti al PBS, poiché possono causare precipitazioni. In questi casi, si consiglia di utilizzare i tamponi Good's. Inoltre, la nostra soluzione di PBS è un'alternativa accettabile al terreno di trasporto virale per il trasporto e la conservazione dei virus a RNA, compreso il SARS-CoV-2.
Controllo di qualità
Filtrato sterile
Conservazione e durata di conservazione
Conservare a +2°C a +25°C, al riparo dalla luce.
Una volta aperto, conservare a 2°C
- 25°C e utilizzare entro 24 mesi.
Condizioni di spedizione
Temperatura ambiente
Manutenzione
Conservare in frigorifero a +2°C a +8°C al buio. Evitare il congelamento e il riscaldamento frequente a +37°C, in quanto riduce la qualità del prodotto.
Non riscaldare il terreno di coltura oltre i 37°C e non utilizzare fonti di calore non controllate come le microonde.
Se si deve utilizzare solo una parte del terreno di coltura, prelevare la quantità necessaria e riscaldarla a temperatura ambiente prima dell'uso.
Composizione
Categoria
Componenti
Concentrazione (mg/L)
Sali
Cloruro di potassio
200
Potassio fosfato monobasico anidro
200
Cloruro di sodio
8000
Sodio fosfato bibasico anidro
115020,00 €* -
Prodotti correlati
Prodotti correlati
Cellule U2OS-CRISPR-SNAPf-Nup358/RanBP2Organismo Umano Tessuto Osso Malattia Osteosarcoma 800,00 €*