Emberi sejtvonalak, a legapróbb markerekig hitelesítve
Minden általunk szállított emberi sejtvonal átesett STR-azonosító profilalkotáson, többszörös szennyeződésvizsgálaton és független ellenőrzésen, mielőtt elhagyta laboratóriumunkat.
Emberi sejtek
Üdvözöljük a Cytionnál, az első számú forrásnál a hitelesített és szennyeződésmentes emberi sejtvonalakhoz. Kiterjedt sejtbankunkat úgy állítottuk össze, hogy megbízhatóan és pontosan támogassa a biomedicinális kutatást. Minden modell szigorú tesztelésen esik át, hogy biztosítsuk genetikai identitását, tisztaságát és teljesítményét, lehetővé téve a reprodukálható eredményeket széles körű alkalmazásokban. Csúcstechnológiás kutatáshoz szükséges sejtek
Sejtek a legmodernebb kutatásokhoz
Fedezze fel hitelesített, validált és mycoplasma-mentes emberi sejtvonalak széles választékát, amelyek alkalmasak betegségmodellezésre, gyógyszerkutatásra, fehérjetermelésre, hibridóma-előállításra és vírusok szaporítására. Minden tétel ellenőrzött körülmények között készül, és több lépcsős minőség-ellenőrzésen esik át, hogy a felolvasztástól a kísérletig megbízhatóságot biztosítson.

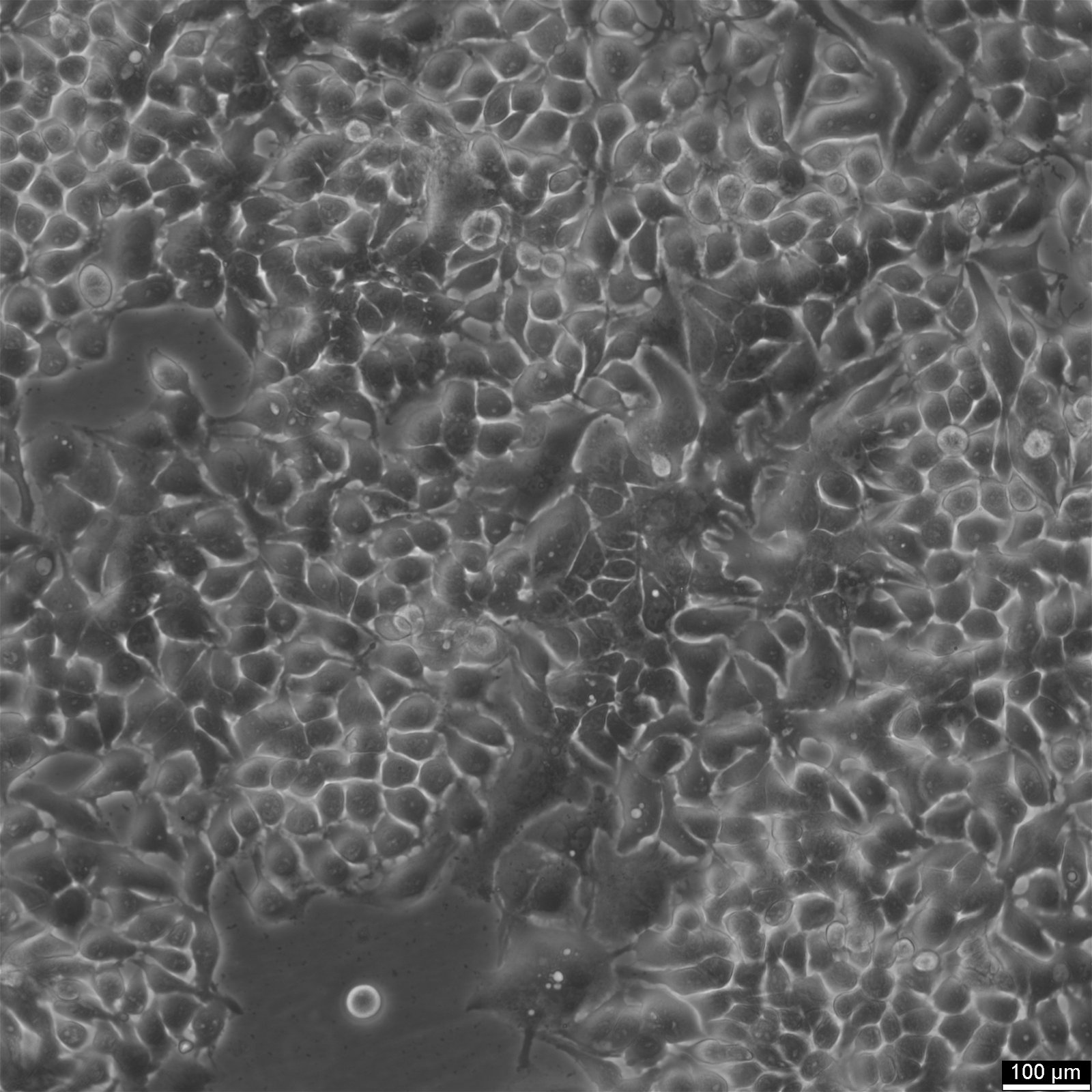
| Szervezet | Emberi |
|---|---|
| Szövet | Hasnyálmirigy |
| Betegség | Hasnyálmirigy ductus adenokarcinóma |
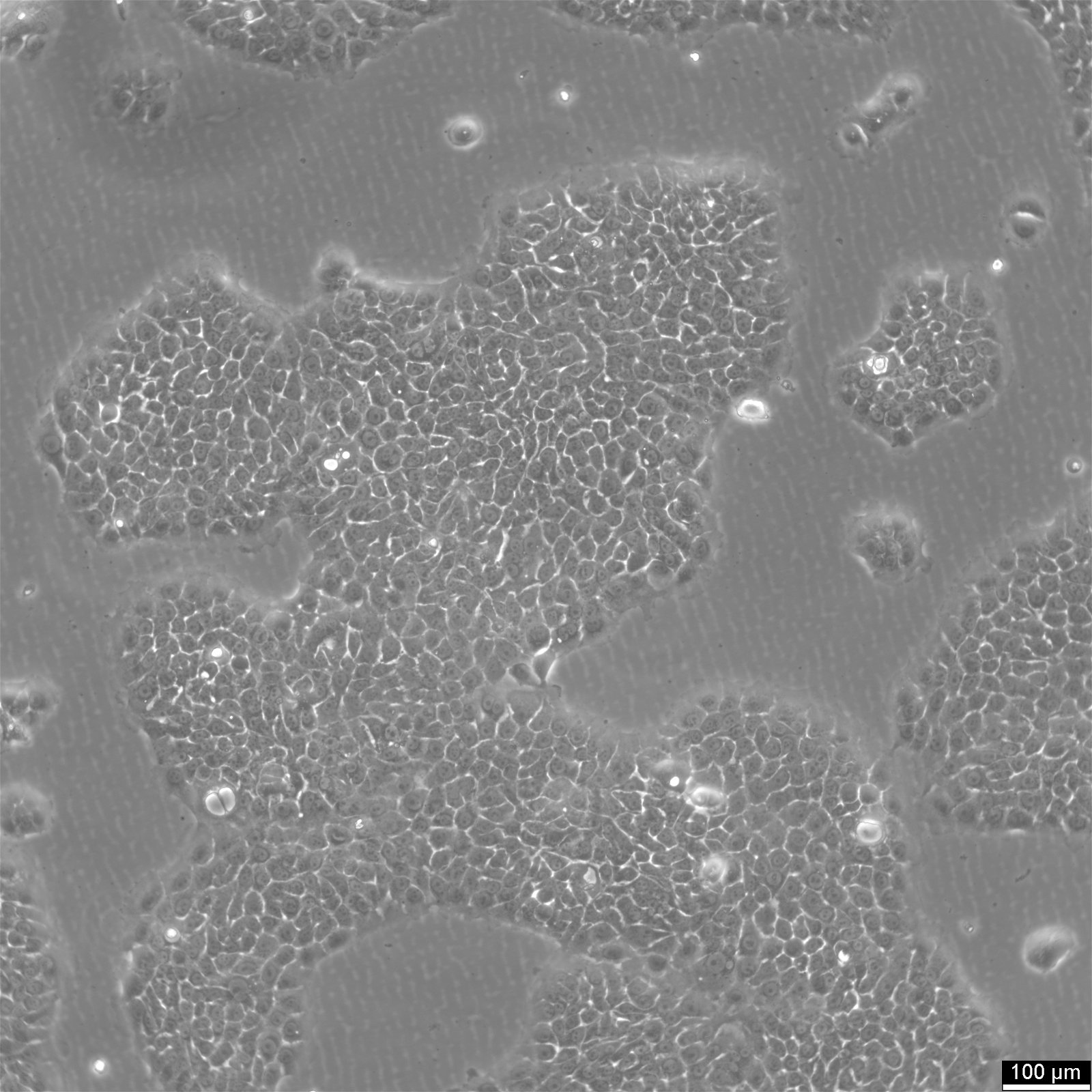
| Szervezet | Emberi |
|---|---|
| Szövet | Vastagbél, Dukes C típusa |
| Betegség | Kolorektális adenokarcinóma |
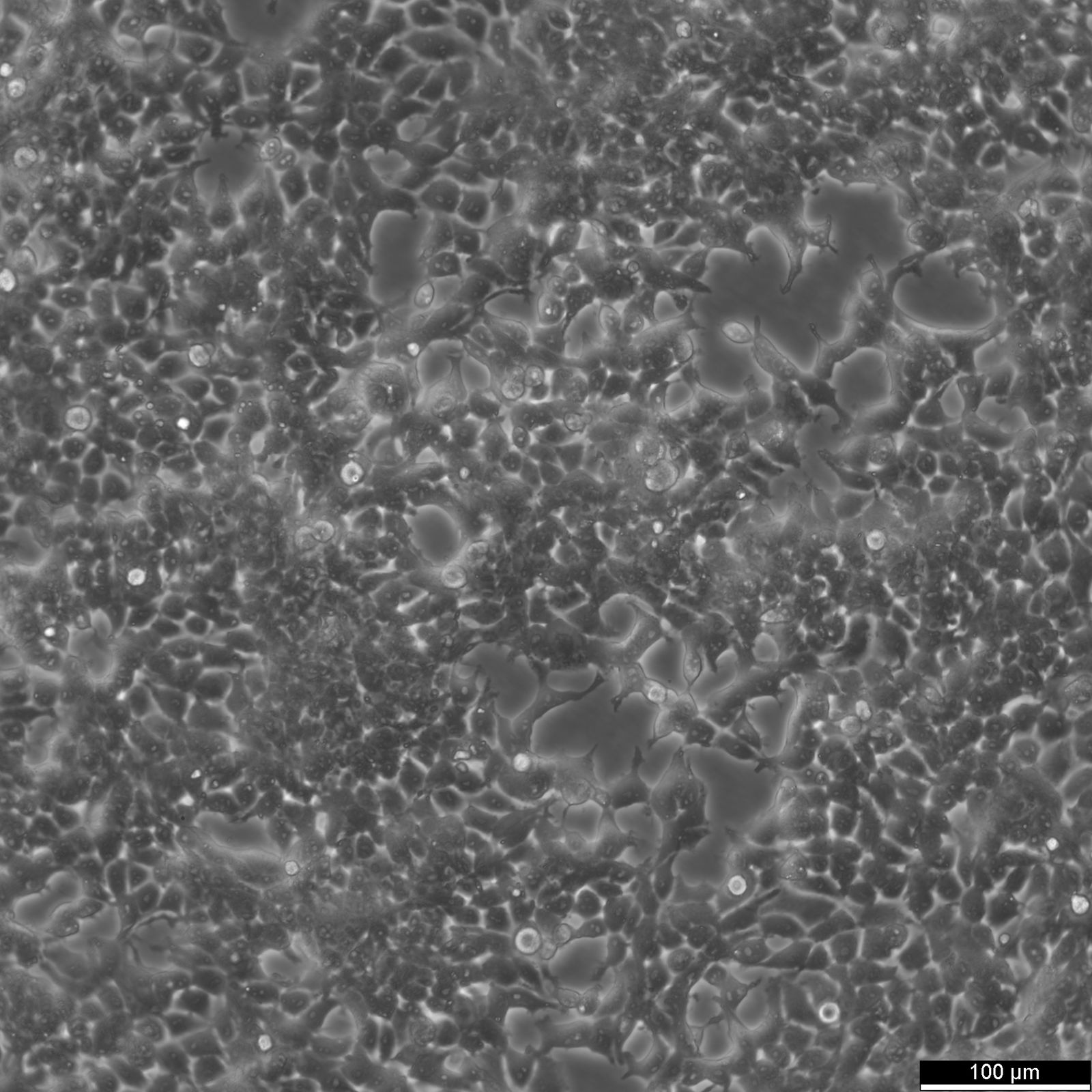
| Szervezet | Emberi |
|---|---|
| Szövet | Agy, jobb oldali frontális parieto-okcipitális kéreg |
| Betegség | Glioblastoma |
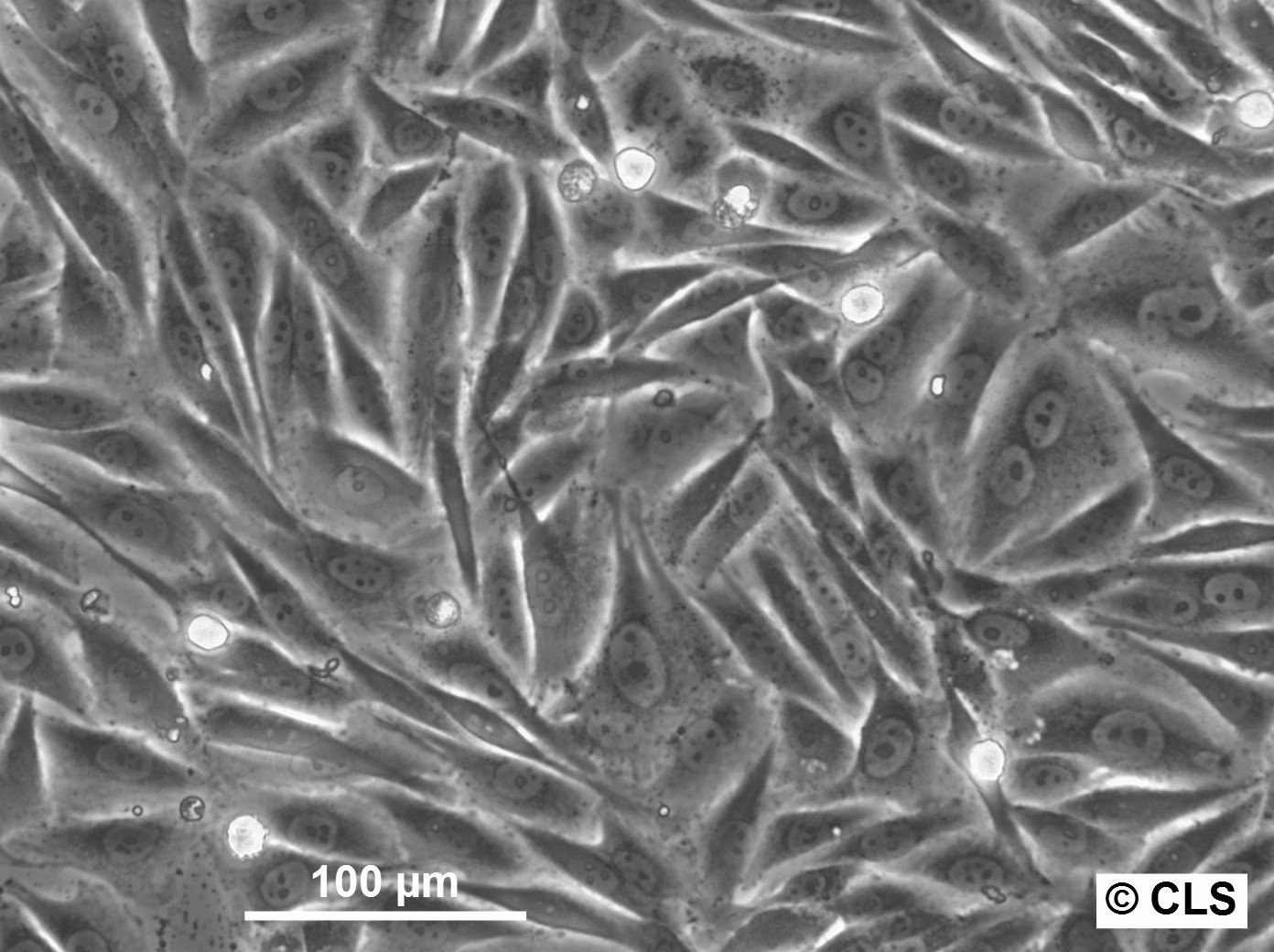
| Szervezet | Emberi |
|---|---|
| Szövet | Petefészek |
| Betegség | Alacsony fokú serosus petefészek karcinóma |