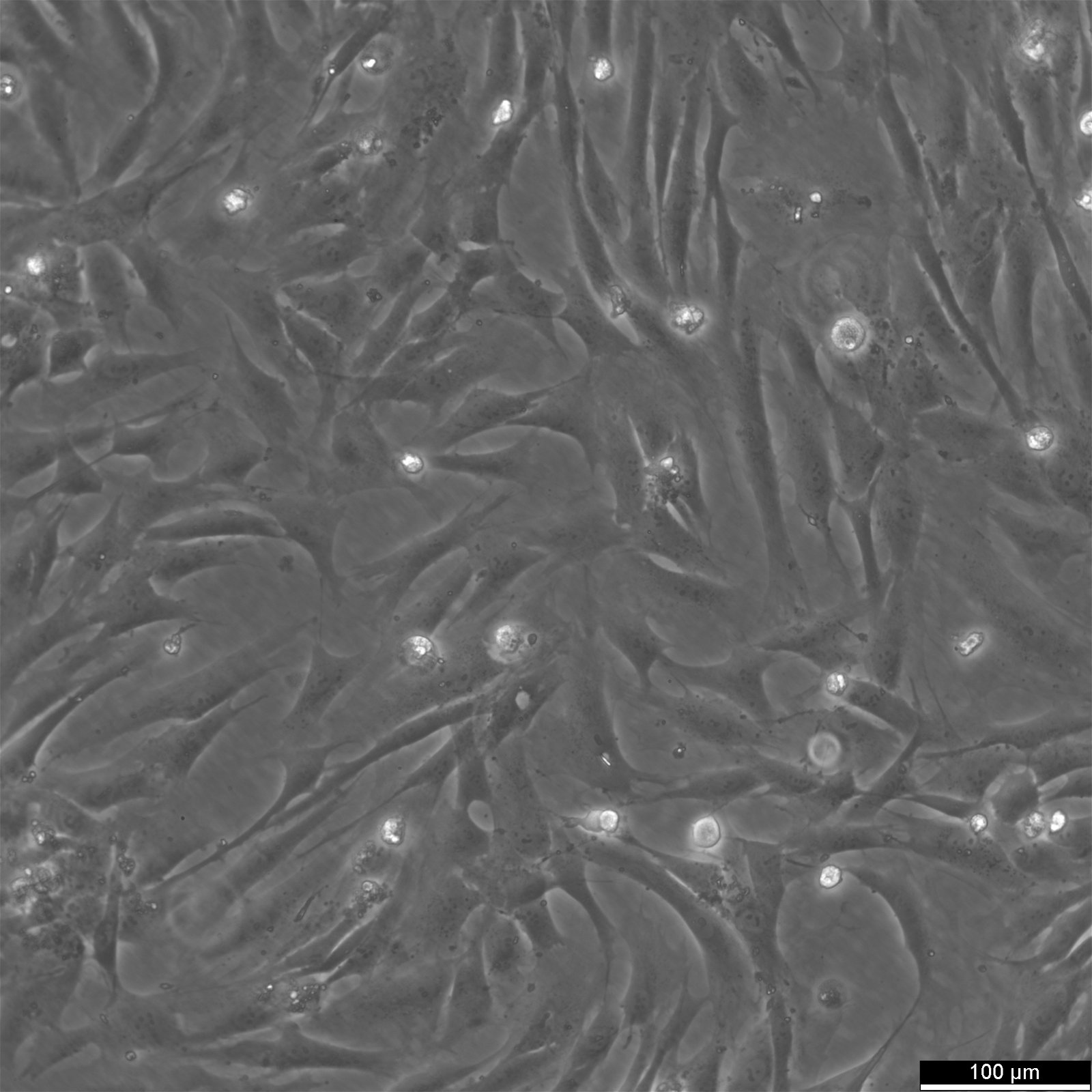
Emberi primer sejtek
A Cytion különböző szövetekből és donoroktól származó, gondosan összeválogatott humán primer sejtek portfólióját kínálja. Ezek a fiziológiailag releváns modellek a transzlációs kutatás, a toxicitási vizsgálatok, a regeneratív medicina és a fejlett in vitro tanulmányok támogatására lettek kifejlesztve. Minden tenyészetet ellenőrzött körülmények között állítanak elő, és szigorú minőség-ellenőrzésen vetik alá, hogy biztosítsák az identitást, a sterilitást és az állandó teljesítményt.
Fiziológiailag releváns modellek fejlett kutatásokhoz
Elsődleges sejtek portfóliónk több emberi szövetből származó endoteliális, epiteliális, fibroblaszt és őssejt populációkat tartalmaz. Ezek a modellek megőrzik eredeti szövetük legfontosabb funkcionális jellemzőit, megbízható rendszereket biztosítva betegségmodellezés, gyógyszervizsgálat és szövetmérnöki alkalmazások számára.
Mik azok az emberi primer sejtek?
Az elsődleges sejtek a megfelelő szövetek legtisztább képviselői. A szövetekből izolálják és feldolgozzák őket, hogy ideális körülmények között, kultúrában telepedhessenek meg. Jobban utánozzák az in vivo állapotot, és normális élettani jellemzőket mutatnak, mivel nem módosított, hanem szövetből származnak. Emiatt hasznos modellként szolgálhatnak a sejtfarmakológiai, toxikológiai és fiziológiai kutatásokhoz (beleértve az anyagcsere, az öregedés és a jelátvitel vizsgálatát). Ne feledje, hogy a primer sejtek tenyésztése és fenntartása nagyobb kihívást jelent, mint egy folyamatos sejtvonalé, mivel rövidebb az élettartamuk, és bizonyos számú sejtosztódás után abbahagyják az osztódást (vagy elöregednek). A sejtek jelátviteli útvonalainak vizsgálatát bonyolítja a donoroktól és a szubkultúrás gyakorlatok révén szerzett primer sejtek eredendő változékonysága. A jelátviteli vizsgálatok megkezdése előtt a kutatók gyakran végeznek szűrést annak megállapítására, hogy a sejtek reagálnak-e az általánosan használt ingerekre. Az idő- és pénzpazarlás elkerülése érdekében a primer sejtek a szűrés előtt stimulálhatók a főbb jelátviteli útvonalak aktiválására.
Miért érdemes humán primer sejteket használni?
Az immortalizált sejtvonalakat általában sejtvizsgálatként használják. Bár a tudósok elismerték, hogy a sejtvonalak okozta biológiai változások károsak lehetnek az élettani jelentőségük tanulmányozásában. A humán primer sejtek használata javítja a sejttenyészetekkel nyert adatok fiziológiai értékét, és egyre inkább fontosnak tartják őket a biológiai folyamatok, a betegségek lefolyásának és a gyógyszerfejlesztés tanulmányozásában.
A humán primer sejteket széles körben használják a sejtek közötti és intracelluláris kommunikáció, a fejlődésbiológia, valamint a rák, a Parkinson-kór és a cukorbetegség hátterében álló mechanizmusok in vitro vizsgálatára, számos más preklinikai és vizsgálati biológiai kutatási terület mellett. A kutatók már régóta használnak immortalizált sejtvonalakat a szövetek működésének tanulmányozására; azonban a nyilvánvaló mutációkkal és kromoszóma-rendellenességekkel rendelkező sejtvonalak nem biztos, hogy jó helyettesítői a normális sejteknek és a betegségek korai stádiumban történő kialakulásának. Egy adott szöveti sejttípus pontosabb modellje ma már elérhető az adott szövetből izolált és elsődleges sejttenyésztő közegben és kiegészítőkben fenntartott humán primer sejtek használatával.
Mi az elsődleges sejtkultúra?
Az immortalizált sejtvonalak használata helyett az elsődleges sejtkultúra során a sejteket közvetlenül a testen kívüli, többsejtű szervezetből tenyésztik. Egyes országokban, például az Egyesült Királyságban, jogilag elismerték, hogy az elsődleges sejtkultúrák jobban reprezentálják az in vivo szöveteket, mint a sejtvonalak. Mindazonáltal az elsődleges sejteknek megfelelő szubsztrátumra és tápanyagokra van szükségük a növekedéshez, és bizonyos számú osztódás után szeneszcens fenotípus alakul ki bennük, ami az osztódás végleges leállítását eredményezi. Ez a két tényező motiválja a sejtvonalak létrehozását. Mind a természetes úton immortalizált primer sejtek (pl. HeLa sejtek), mind a mesterségesen immortalizált primer sejtek (pl. HEK sejtek) korlátlan ideig tenyészthetők sejttenyészetben.
Humán primer sejtek szövettípusok szerint
A tudományos vizsgálatokban leggyakrabban használt humán primer sejtek közé tartoznak a hámsejtek, fibroblasztok, keratinociták, melanociták, endotélsejtek, izomsejtek, immunsejtek és őssejtek, például a mesenchymális őssejtek. Kezdjük azzal, hogy a tenyészetek heterogének (a szövetben jelen lévő sejttípusok keverékét képviselik), és csak meghatározott ideig tarthatók életben in vitro. A transzformáció egy olyan in vitro folyamat, amely lehetővé teszi, hogy a humán primer sejteket korlátlan számú szubkultúrára manipulálják. A transzformáció történhet természetes úton, vagy indukálható vegyi anyagokkal vagy vírusokkal. Miután genetikai transzformáción ment keresztül, egy primer kultúra korlátlanul osztódhat immortalizált másodlagos sejtvonallá, ha elegendő tápanyagot és helyet kap.
Endothelsejtek
A rákgyógyítás, a sebgyógyítás, a sejtszignál-kutatás, a nagy áteresztőképességű és nagy tartalmú szűrés, valamint a toxikológiai szűrés csak néhány olyan terület, amely hasznot húzhat a primer endotélsejtek kutatási eszközként való használatából.
Keratinociták
A felnőtt emberi bőr vagy az újszülöttkori fityma epidermiszéből származó keratinociták döntő szerepet játszanak az olyan bőrbetegségek, mint a pikkelysömör és a rák tanulmányozásában.
Epithelsejtek
A rákkutatástól a toxikológiai vizsgálatokig az elsődleges epithelsejtek felbecsülhetetlen értékű forrásnak bizonyultak a szervezet természetes védekező mechanizmusainak modellezésében.
Fibroblasztok
A pluripotens őssejtek (iPS) indukálása és a sebgyógyulás tanulmányozása csak néhány a primer fibroblasztok számos felhasználási módja közül.
Immunsejtek
A perifériás vér mononukleáris sejtjei, röviden PBMC, a vér mononukleáris sejtjei, amelyek kerek sejtmaggal rendelkeznek. Főként limfocitákat és monocitákat tartalmaznak, amelyek az immunválasz során fontos funkciókat vesznek át. A perifériás vér mononukleáris sejtjeit gyakran használják fertőzések diagnosztizálására vagy az esetleges oltási védelem kimutatására. A T-sejtek által közvetített sejtes immunválasz megismerése gyakran döntő fontosságú.
Melanociták
A melanociták, a melanin nevű pigmentet termelő, specializált bőrsejtek hasznos modellként szolgálnak olyan témák kutatásában, mint a sebgyógyulás, a toxicitás, a melanoma, az ultraibolya (UV) sugárzásra adott bőrválasz, a bőrbetegségek és a kozmetikumok.
Őssejtek
Az őssejtek képesek a legkülönbözőbb sejttípusokká differenciálódni. Differenciálódási képességüknek köszönhetően új lehetőségeket kínálnak az emberi szövetek és egészségi állapotok modellezésére.
Mesenchymális őssejtek
A mesenchymális őssejtek, más néven MSC-k, különböző emberi forrásokból, például csontvelőből, zsírból (zsírszövet), köldökzsinórszövetből (Wharton-kocsonya) és magzatvízből (a magzatot körülvevő folyadék) nyerhetők, és in vitro bővíthetők. Ezek a felnőttkori stroma őssejtek képesek a legkülönbözőbb sejttípusokká fejlődni. E sejttípusok közé tartoznak a csontsejtek, porcsejtek, izomsejtek, idegsejtek, bőrsejtek és szaruhártya sejtek.
Simaizomsejtek
Az üreges szervekben az elsődleges simaizomsejtek (SMC) bélelik a belső teret, és közvetítik a kontraktilitást. A rák és más betegségek mellett az SMC-k a magas vérnyomás fibrózisának modellezésére is felhasználhatók.
Primer sejtek és sejtvonalak
Vagy spontán mutáció révén, mint a transzformált rákos sejtvonalakban, vagy szándékos módosítással, mint a rákos gének mesterséges előállítása, a folyamatos sejtvonalak elnyerték a végtelen szaporodás lehetőségét (immortalizáltak). A folyamatos sejtvonalak általában megbízhatóbbak és kényelmesebbek a kezelésben, mint az elsődleges sejtek. A végtelenségig képesek terjeszkedni, és gyors hozzáférést biztosítanak a lényeges adatokhoz. A folyamatos sejtvonalak használatának vannak bizonyos korlátai, többek között az, hogy genetikailag módosított/transzformáltak, ami megváltoztathatja a fiziológiai jellemzőket, és nem felel meg az in vivo állapotnak, és hogy ez jelentős passzázs esetén idővel tovább változhat.
A primer sejtkultúra fejlődése
Az elsődleges sejtek hírhedt hírében állnak, hogy nehéz velük dolgozni. A folyamat azonban minden eddiginél egyszerűbbé válik, köszönhetően az elsődleges sejttenyésztés fejlődésének, a teljesen optimalizált protokollokkal rendelkező, kereskedelmi forgalomban kapható elsődleges sejtek elérhetőségének és a kevesebb ráfordítást igénylő új elemzési technikáknak.
A kétdimenziós sejtkultúráról a háromdimenziós sejtkultúrára való áttérés jelentős mérföldkőnek számít a területen. A szövetspecifikus architektúra, a sejt-sejt kölcsönhatások és a mechanikai/biokémiai jelátvitel a 2D kultúrában gyengülhet. Így ezeknek a kultúráknak a biológiai értékének van egy felső határa.
Másrészt a 3D sejtkultúra lehetővé teszi a sejtek terjeszkedését és kölcsönhatását egy 3D extracelluláris kerettel. Ez lehetővé teszi, hogy a sejtek kölcsönhatásba lépjenek egymással és az extracelluláris mátrixszal, így a 3D kultúrák fiziológiailag relevánsabbá válnak. A módszer pontossága az in vivo válaszok előrejelzésében forradalmian újszerűvé tette az olyan területeken, mint a gyógyszerkutatás és -fejlesztés. Emiatt a legmodernebb technológiák, mint például a betegekből származó organoidok és a szerv a chipen (organs-on-a-chip), rendkívül kontextuális modelleket biztosítanak a gyógyszerek szűréséhez és fejlesztéséhez.
A primer sejtgenerálás szűk keresztmetszetet jelent az elsődleges tenyésztésben. Ennek leküzdéséhez általában nagyobb szövetmennyiségre van szükség, amelynek elérése kihívást jelenthet. A jobb analitikai érzékenység azonban előrelépést jelent. Például a nagy mennyiségű primer sejtek tenyésztésének szükségessége csökken az egysejtes technológia alkalmazásával, amely magában foglalja a szekvenálást, a western blottingot és a tömegcitometriát.
Az elsődleges sejtkultúra ígéretes kilátásai
Az elsődleges sejttenyésztés általános nehézségeit a technológiai fejlődés enyhíti. Ez a módszer viszont gyorsan felváltja a többi módszert, mint a sejt- és molekuláris biológiai tanulmányok és gyakorlat arany standardja. A vakcinagyártás, a szervpótlás, az őssejtterápiák, a rákkutatás és még sok minden más nagymértékben profitálhat az elsődleges sejtkultúra folyamatos fejlődéséből.
Tippek és trükkök az elsődleges sejttenyésztéshez
A sejttágítás igényei
Az elsődleges sejtek tenyésztésének két legelterjedtebb módszere a szuszpenzióban vagy felületen (2D) történő tenyésztés. Egyes sejtek képesek szabadon lebegni a véráramban anélkül, hogy valaha is megtapadnának egy felületen (például a perifériás vérből származó sejtek). Különböző sejtvonalakat úgy alakítottak ki, hogy szuszpenziós kultúrákban fejlődjenek, ahol olyan sűrűségeket érhetnek el, amelyek 2D növekedési körülmények között elérhetetlenek. Az in vitro növekedéshez rögzítésre szoruló primer sejteket adherens sejteknek nevezzük, és ide tartoznak a szilárd szövetekben található sejtek is. Az adhéziós tulajdonságok javítása és a növekedéshez és differenciálódáshoz szükséges egyéb jelek biztosítása érdekében ezeket a sejteket általában lapos, bevonat nélküli műanyag edényben, de esetenként mikrohordozóban tenyésztik. Ez utóbbi lehetőség extracelluláris mátrixfehérjékkel (például kollagénnel és lamininnel) bevonható. A sejttenyésztéshez használt táptalaj egy alapközegből áll, amelyet a megfelelő növekedési faktorokkal és citokinekkel egészítettek ki. A sejtinkubátor a laboratóriumi inkubátorok speciális típusa, amelyet a sejtek tenyésztésére és meghatározott hőmérsékleten és gázkeverékben (emlőssejtek esetében általában 37 °C, 5% CO2) történő tartására használnak. A tenyésztett sejttípustól függően az optimális körülmények nagyon eltérőek lehetnek. A termesztett sejttípusoktól függően az optimális növekedési közeg a tényezők egyedi kombinációját tartalmazza, beleértve, de nem kizárólagosan a pH-t, a glükózkoncentrációt, a növekedési faktorokat és más tápanyagok jelenlétét.
A növekedési táptalajban lévő antibiotikumok létfontosságúak az elsődleges tenyészet létrehozása során, hogy megakadályozzák a gazdaszövetből származó szennyeződést. Néhány antibiotikum-kezelés gentamicin, penicillin, streptomicin és amfotericin B kombinációját tartalmazza. Az antibiotikumok hosszabb ideig történő alkalmazása azonban nem javasolt, mivel egyes reagensek (például az amfotericin B) hosszú távon toxikusak lehetnek a sejtekre.
A legtöbb primer sejt szeneszcencián megy keresztül, és bizonyos számú populációduplázódás után leáll az osztódásuk, ezért létfontosságú, hogy az izolálás után életben tartsuk őket. A sejtek hosszú távú életképessége szakértő sejttenyésztési technikákat és ideális tenyésztési körülményeket igényel (beleértve a megfelelő táptalajt, a megfelelő hőmérsékletet, a megfelelő gázkeveréket, a megfelelő pH-t, a növekedési faktorok megfelelő koncentrációját, a tápanyagok jelenlétét és a glükóz jelenlétét). Mivel a táptalajok kiegészítésére használt számos növekedési faktor állati vérből származik (a vérből származó összetevők rendelkeznek a szennyeződés lehetőségével), ajánlott minimalizálni vagy teljesen elkerülni a használatukat. Fontos továbbá az aszeptikus technika alkalmazása.
Szubkultúra és karbantartás
Amikor az izolált sejtek megtapadnak a tenyésztőedény felszínén, ez a fenntartási fázis kezdetét jelzi. A kötődés jellemzően 24 órával a tenyésztés megkezdése után következik be. A sejteket akkor kell szubkultúrázni, amikor elérnek egy bizonyos konfluencia százalékot és aktívan szaporodnak. Mivel a konfluencia utáni sejtek differenciálódhatnak és lassabb proliferációt mutathatnak a passzázs után, a legjobb, ha az elsődleges sejtkultúrákat a 100%-os konfluencia elérése előtt szubkultúrázzuk.
A friss táptalajban történő szubkultiválás fenntartja a horgonyzásfüggő sejtek exponenciális növekedését. A monokultúra szubkultiválása megszakítja a sejtek közötti és intracelluláris sejtfelszíni kölcsönhatásokat. Alacsony koncentrációjú proteolitikus enzimeket, például tripszin/EDTA-t alkalmaznak az adherens primer sejtek monoszlopokból vagy szövetekből történő kivonására. A disszociációt és az egysejtes oldattá hígítást követően a sejteket megszámolják, és friss tenyésztőedényekbe helyezik át, hogy újra rögzüljenek és szaporodjanak.
Kriokonzerválás és visszanyerés
A kriokonzerválás az élő sejteket alacsony hőmérsékleten történő fagyasztással konzerválja. A humán primer sejtek kriokonzerválása és felolvasztása megakadályozza a sejtek elhalását és károsodását a tárolás és felhasználás során. A humán primer sejtek krioprotektálása DMSO vagy glicerin segítségével történik (megfelelő hőmérsékleten és ellenőrzött fagyasztási sebességgel). A fagyasztási folyamatnak fokozatosan, percenként -1 °C-on kell történnie a jégkristályok kialakulásának megelőzése érdekében. A hosszú távú tároláshoz folyékony nitrogén (-196 °C) vagy -130 °C alatti hőmérséklet szükséges.
A kriotárolt sejtek felolvasztásához elegendő a fagyasztott sejteket 1-2 percre 37 °C-os vízfürdőbe meríteni. A humán primer sejteket a fagyasztóból való kiolvasztás után nem szabad centrifugálni (mivel a kriokonzerválásból való visszanyerés során rendkívül érzékenyek a károsodásra). A felolvasztás után azonnal alkalmas a sejtek kiültetésére, és a kiültetést követő első 24 órában elősegíti a kultúrák kötődését. 1 Miután a kriokonzervált primer sejtek rögzültek, az elhasznált táptalajt el kell távolítani (mivel a DMSO káros a primer sejtekre, és a kiolvasztás utáni életképesség csökkenését okozhatja).