A pluripotens őssejtek potenciáljának feltárása a regeneratív gyógyászatban
A pluripotens őssejtek lenyűgöző kutatási területet jelentenek, amely hatalmas lehetőségeket rejt magában a regeneratív gyógyászat és a betegségek modellezése terén. Ezek a sejtek, amelyek közé tartoznak a spontán immortalizált sejtvonalak, mint például a WI-38 sejtek, valamint a felnőtt szövetekből származó indukált pluripotens őssejtek (iPSC), rendelkeznek azzal az egyedülálló képességgel, hogy a szervezet bármely sejttípusává differenciálódjanak. Ez teszi őket felbecsülhetetlen értékű eszközzé az emberi fejlődés, a betegségmechanizmusok és a lehetséges terápiák tanulmányozásához.
A pluripotens őssejtek kutatásának élvonalában az indukált pluripotens őssejtek állnak, amelyeket a beteg saját sejtjeiből, például bőrfibroblasztokból vagy vérsejtekből lehet előállítani. E felnőtt sejtek speciális faktorok segítségével történő átprogramozásával a kutatók betegspecifikus iPSC-ket hozhatnak létre, amelyek megtartják a donor genetikai hátterét.
Az emberi primer sejtek jelentősége a pluripotens őssejtkutatásban
A humán primer sejtek a pluripotens őssejtek kutatásában is kulcsfontosságúak, mivel alapot biztosítanak az iPSC-eredetű sejtek összehasonlításához és validálásához. Például a humán fogtörzsi őssejtek (hDPSC) és a humán fogtüsző őssejtek (hDFSC ) értékes források a fogak fejlődésének és regenerációjának tanulmányozásához. Hasonlóképpen, a HUVEC, az egy donorból származó sejteket széles körben használják az érbiológiai és angiogenezis kutatásban, és viszonyítási alapként szolgálnak az iPSC-eredetű endotélsejtek értékeléséhez.
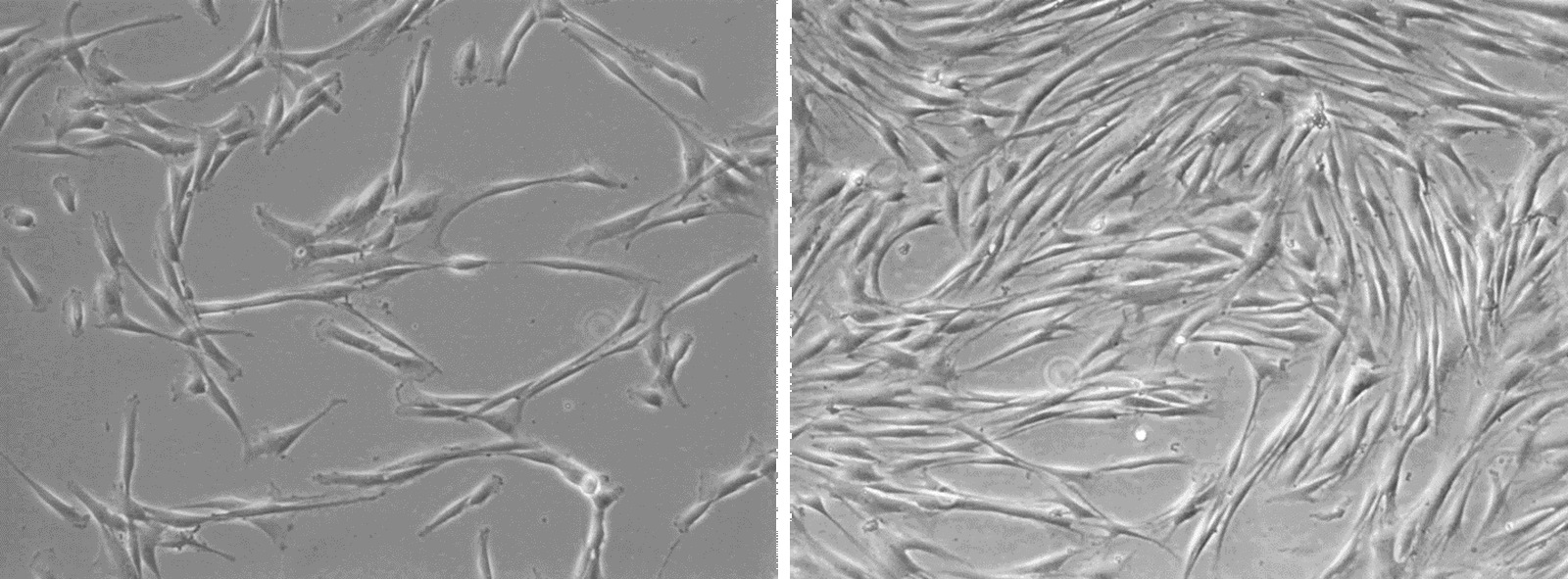
Egy másik példa a P-19 sejt, egyfajta pluripotens embrionális karcinóma, amelyet eredetileg egy C3H/He törzsű egér teratocarcinomájából nyertek. A bal oldalon látható P19 sejtvonal egérből (Mus musculus) származik.
Humán mesenchymális őssejtek katalógusa
A pluripotens őssejtek a regeneratív orvoslás és a fejlődésbiológiai kutatások sarokkövei. Ezek a sejtek, amelyek közé tartoznak az embrionális őssejtek (ESC) és az indukált pluripotens őssejtek (iPSC), figyelemre méltó képességgel rendelkeznek arra, hogy a szervezet bármely sejttípusává differenciálódjanak. Ez az egyedülálló tulajdonság felbecsülhetetlen értékű eszközzé teszi őket az emberi fejlődés tanulmányozásához, a betegségek modellezéséhez, a gyógyszerek szűréséhez és a lehetséges sejtalapú terápiákhoz. Az iPSC-k különösen azáltal forradalmasították a területet, hogy lehetővé tették a felnőtt szövetekből a betegspecifikus őssejtek létrehozását, ami izgalmas lehetőségeket nyitott meg a személyre szabott gyógyászat számára. A kutatók ma már képesek iPSC-ket előállítani különböző betegségekben szenvedő betegekből, azokat a megfelelő sejttípusokká differenciálni, és egy tálban tanulmányozni ezen állapotok mögöttes mechanizmusait. Ezen túlmenően, az a képesség, hogy a betegből származó iPSC-kből autológ sejtterápiákat lehet létrehozni, hatalmas ígéretet hordoz a regeneratív orvoslás számára, mivel ezek a sejtek potenciálisan felhasználhatók a sérült vagy beteg szövetek pótlására az immunrejekció kockázata nélkül. Ahogy a pluripotens őssejtek kutatása tovább fejlődik, egyre világosabbá válik, hogy ezek a sejtek kulcsfontosságú szerepet fognak játszani az orvostudomány jövőjének alakításában és az emberi biológia megértésében.
| Termék | Leírás | Cat. No. |
|---|---|---|
| Humán mesenchymális őssejtek - zsírszövet | Emberi zsírszövetből izolált mesenchymális őssejtek | 300645 |
| Humán mesenchymális őssejtek - Amnion | Emberi magzatburokból nyert mesenchymális őssejtek | 300644 |
| Humán mesenchymális őssejtek - csontvelő (HMSC-BM) | Emberi csontvelőből izolált mesenchymális őssejtek | 300665 |
| Humán mesenchymális őssejtek - Chorion Villi | Humán chorion villiből nyert mesenchymális őssejtek | 300646 |
| Humán mesenchymális őssejtek - endometrium | Humán endometriumszövetből izolált mesenchymális őssejtek | 300647 |
| Humán mesenchymális őssejtek - köldökzsinór - artéria | Humán köldökzsinór artériából nyert mesenchymális őssejtek | 300648 |
| Humán mesenchymális őssejtek - Whartons Jelly (HMSC-WJ) | Az emberi köldökzsinór Wharton-kocsonyából izolált mesenchymális őssejtek | 300685 |
Az iPSC-kben rejlő lehetőségek és kihívások a betegségek modellezésében és terápiájában
A betegből származó iPSC-k példátlan lehetőséget kínálnak az emberi betegségek edényben történő modellezésére. E sejtek betegség szempontjából releváns sejttípusokká történő differenciálásával a kutatók tanulmányozhatják a különböző kórképek hátterében álló molekuláris mechanizmusokat, és potenciális gyógyszerjelölteket szűrhetnek. Például a genetikai szívbetegségben szenvedő betegekből származó iPSC-eredetű kardiomiocitákat használták a betegség fenotípusainak reprodukálására és a terápiás vegyületek hatékonyságának tesztelésére [198]. Hasonlóképpen, az olyan neurológiai rendellenességekben szenvedő betegekből származó iPSC-eredetű neuronok, mint az Alzheimer- és a Parkinson-kór, értékes betekintést nyújtottak a betegség progressziójába és a gyógyszerre adott válaszba [199].
Számos kihívást kell azonban megoldani, mielőtt az iPSC-ket széles körben alkalmazni lehetne a betegségek modellezésére és terápiájára. Ezek közé tartoznak:
- Az iPSC-k átprogramozási hatékonyságának és minőségének változékonysága
- Genetikai és epigenetikai aberrációk az újraprogramozás során
- Az iPSC-ből származó sejtek éretlen vagy magzati fenotípusa
- A differenciálásra és érlelésre vonatkozó szabványosított protokollok hiánya
- A tumorigenitással és immunogenitással kapcsolatos biztonsági aggályok
A kutatás célja, hogy ezeket a problémákat hatékonyabb és szabványosított átprogramozási módszerek kidolgozásával, a differenciálási protokollok finomításával és szigorú minőségellenőrzési intézkedések végrehajtásával kezelje. A génszerkesztési technológiák, mint például a CRISPR/Cas9, fejlődése lehetővé teszi a betegséget okozó mutációk korrekcióját a betegből származó iPSC-kben is, megnyitva az utat az autológ sejtpótló terápiák előtt [200].
Az iPSC-k jövője a regeneratív gyógyászatban
Az iPSC-technológia megjelenése izgalmas lehetőségeket nyitott meg a regeneratív gyógyászat számára. Az embrionális őssejtekkel ellentétben az iPSC-k a beteg saját sejtjeiből nyerhetők, így elkerülhetők az etikai aggályok és az immunrejekció kockázata. Számos preklinikai vizsgálat bizonyította az iPSC-ból származó sejtekben rejlő lehetőségeket különböző betegségek kezelésében, mint például:
- Parkinson-kór: IPSC-ből származó dopaminerg neuronok transzplantációja állatmodellekben [201]
- Gerincvelő-sérülés: A funkcionális helyreállást elősegítő iPSC-eredetű neurális prekurzor sejtek beültetése [202]
- Makuladegeneráció: A károsodott retinális pigment epithelium pótlása iPSC-eredetű sejtekkel [203]
- Szívelégtelenség: IPSC-ből származó kardiomiociták befecskendezése a szívműködés javítására [204]
A terület előrehaladtával várhatóan több olyan klinikai vizsgálat is megjelenik majd, amelyekben iPSC-eredetű sejteket használnak. Ahhoz azonban, hogy ezek az ígéretes preklinikai eredmények biztonságos és hatékony terápiákká váljanak, számos akadályt kell leküzdeni, például az iPSC-eredetű sejtek tisztaságának és stabilitásának biztosítása, skálázható gyártási folyamatok kifejlesztése és megfelelő szabályozási irányelvek kialakítása.
Összefoglalva, az iPSC-k hatékony eszközt jelentenek a betegségmodellezés, a gyógyszerkutatás és a regeneratív orvoslás számára. Bár még mindig vannak kihívások, a kutatás gyors üteme és a technológiai fejlődés ezen a területen nagy ígéretet jelent a különböző emberi betegségek kezelésének forradalmasítására. A tudósok, klinikusok és szabályozó testületek közötti további interdiszciplináris együttműködés döntő fontosságú lesz az iPSC-kben rejlő lehetőségek teljes körű kiaknázásában az emberi egészség javítása érdekében.
Kulcspontok
- az iPSC-k szomatikus sejtekből származnak a pluripotenciához kapcsolódó gének bevitelével
- az iPSC-k hasonló tulajdonságokkal rendelkeznek, mint az embrionális őssejtek, de elkerülik az etikai aggályokat
- A betegből származó iPSC-k lehetővé teszik a betegségek modellezését és a gyógyszerek személyre szabott szűrését
- az iPSC-ből származó sejtek ígéretes eredményeket mutattak különböző betegségek preklinikai vizsgálataiban
- Az iPSC-kutatás kihívásai közé tartozik a variabilitás, a genetikai instabilitás és a biztonsági aggályok
- Az átprogramozás, a differenciálás és a génszerkesztési technológiák terén elért előrelépések mozdítják elő a területet
- Az iPSC-alapú terápiák klinikai átültetése technikai és szabályozási akadályok leküzdését igényli
- Az interdiszciplináris együttműködések kulcsfontosságúak az iPSC-kben rejlő lehetőségek teljes körű kiaknázásához a regeneratív gyógyászatban

EGY PARTNER, AKIBEN MEGBÍZHAT: CYTION
A pluripotens őssejtek lehetséges alkalmazásai és jövőbeli irányai
A pluripotens őssejtek kutatási területe óriási ígéreteket hordoz a regeneratív orvoslás forradalmasítására, valamint az emberi fejlődés és betegségek megértésének előmozdítására. Mind a humán embrionális őssejtek (hESC), mind az indukált pluripotens őssejtek (hiPSC) rendelkeznek azzal a figyelemre méltó képességgel, hogy a szervezet bármely sejttípusává differenciálódjanak, ami felbecsülhetetlen értékű eszközzé teszi őket a betegségmechanizmusok, a gyógyszerek szűrése és a lehetséges sejtalapú terápiák tanulmányozásában.
a pluripotens őssejtek egyik legizgalmasabb alkalmazása a regeneratív gyógyászatban való felhasználásuk. Preklinikai vizsgálatok bizonyították a hESC- és hiPSC-eredetű sejtek terápiás potenciálját különböző betegségmodellekben, például gerincvelő-sérülés, vakság és szívbetegségek esetén. Jelenleg számos klinikai vizsgálat folyik hESC-eredetű termékekkel, amelyek olyan betegségeket céloznak meg, mint a gerincvelő-sérülés, a makula degeneráció és az 1-es típusú cukorbetegség (1. táblázat). Japánban jóváhagyták továbbá a világ első olyan klinikai vizsgálatát, amelyben hiPSC-ből származó retina pigment epithel sejteket használnak a makuladegeneráció kezelésére.
Mielőtt azonban a pluripotens őssejtekben rejlő teljes potenciál a klinikai gyakorlatban megvalósulhat, számos kihívással kell szembenézni:
- Hatékony és biztonságos átprogramozási módszerek kifejlesztése vírusvektorok és onkogének használata nélkül
- Szigorú minőségellenőrzési intézkedések kialakítása a hESC- és hiPSC-származékok biztonságának és funkcionalitásának biztosítása érdekében
- Differenciálási protokollok optimalizálása a tiszta és funkcionális sejtpopulációk előállítása érdekében
- Alapos preklinikai vizsgálatok elvégzése megfelelő állatmodelleken a pluripotens őssejt-alapú terápiák hatékonyságának és biztonságosságának felmérése érdekében
- A szabályozási környezetben való eligazodás a klinikai vizsgálatokhoz és az esetleges kereskedelmi forgalomba hozatalhoz szükséges engedély megszerzése érdekében
A pluripotens őssejtek, különösen a hiPSC-k másik ígéretes alkalmazása a betegségek modellezése és a gyógyszerkutatás. A betegekből származó hiPSC-k képesek a betegség patológiájának különböző aspektusait reprodukálni, amikor releváns sejttípusokká differenciálódnak, ami hatékony platformot biztosít a betegség mechanizmusainak tanulmányozásához és új terápiás célpontok azonosításához. Ezen túlmenően az egészséges donorokból és betegekből származó hiPSC-k fiziológiailag relevánsabb rendszert kínálnak a gyógyszerek hatékonyságának és toxicitásának értékeléséhez, mint a hagyományos halhatatlan emberi sejtvonalak.
Összefoglalva, bár jelentős előrelépés történt a pluripotens őssejtek kutatása terén, további vizsgálatokra van szükség a pluripotencia és a differenciálódás biológiájának teljes megértéséhez, valamint a terápiás alkalmazásokkal kapcsolatos kihívások leküzdéséhez. Az átprogramozási technológiák javítására, a megbízható differenciálási protokollok létrehozására, valamint a hESC- és hiPSC-eredetű termékek biztonságosságának és hatékonyságának biztosítására irányuló folyamatos erőfeszítések megnyitják az utat e nagy teljesítményű eszközök klinikai alkalmazására a regeneratív gyógyászatban és a gyógyszerkutatásban.
A pluripotens őssejtekben rejlő hatalmas lehetőségek kihasználásával innovatív terápiák kifejlesztésén dolgozhatunk az emberi betegségek széles körére, és végső soron javíthatjuk a betegek állapotát.