
Bevezetés
Az orvosbiológiai kutatások hatalmas területén a sejtvonalak a meg nem énekelt hősökké váltak, amelyek csendben forradalmasítják az emberi egészség és a betegségek megértését. Ezek az apró, élő laboratóriumok számtalan felfedezéshez nyitottak ajtót, a sejtmechanizmusok bonyolultságának feltárásától az életmentő terápiák kifejlesztéséig. A sejtvonalak jelentősége a tudományos kutatásban évről évre növekszik, mivel páratlan ablakot nyújtanak a biológia összetett világába.
A rendelkezésre álló számtalan sejtvonal közül azonban csak néhány kiválasztott emelkedett ki, és a modern biomedicina munkagépeiként érdemelték ki helyüket. Ezek a sejtvonalak újra és újra bebizonyították értéküket, és a kutatóknak olyan eszközöket biztosítanak, amelyekkel kitolhatják a tudományos ismeretek határait. Ebben a cikkben egy magával ragadó utazásra indulunk az 5 legfontosabb sejtvonalon keresztül, amelyek kitörölhetetlen nyomot hagytak az orvosbiológiai kutatás világában. A HeLa sejtek szerény kezdeteitől a HEK293 sejtek által lehetővé tett élvonalbeli innovációkig, felfedezzük e sejtes erőművek lenyűgöző történeteit, és azt a mélyreható hatást, amelyet az életről alkotott elképzeléseinkre gyakoroltak. Csatlakozzon hozzánk, hogy belemerüljünk e rendkívüli sejtvonalak titkaiba, és felfedezzük, hogyan segítik elő a jövő orvosbiológiai áttöréseit.
Top 5 sejtvonal a biogyógyászati kutatásban
HeLa sejtek
Az első halhatatlan emberi sejtvonal, amelyet 1951-ben Henrietta Lacks méhnyakrákos sejtjeiből hoztak létre. A HeLa sejtek számos tudományos áttörésben játszottak szerepet, többek között a gyermekbénulás elleni vakcina kifejlesztésében.
HEK293 sejtek
Emberi embrionális veséből származó epitélsejtek, amelyeket széles körben használnak tranziens és stabil transzformációs kísérletekre, fehérjeexpresszióra és -termelésre, valamint elektrofiziológiai kísérletekre.
MCF-7 sejtek
A hormonális szabályozással, gyógyszerfejlesztéssel és a mellrák biológiájának tanulmányozásával kapcsolatos kutatásokban általánosan használt emlőrákos sejtvonal.
CHO sejtek
Kínai hörcsög petefészek sejtek, amelyeket széles körben használnak biológiai, orvosi és gyógyszeripari kutatási alkalmazásokban, például rekombináns fehérjék előállításában és az epidermális növekedési faktor receptor vizsgálatában.
PC-12 sejtek
Patkány mellékvesekéregből származó sejtvonal, amelyet széles körben használnak az idegtudományi kutatásokban, különösen a neuronális differenciálódás, a neurotranszmitter-szintézis és a neurotoxicitás vizsgálatában.
5. szám: Sf9 sejtek

Az Sf9 sejtek az őszi pajzstetű (Spodoptera frugiperda) petefészekszövetéből származnak, és a rovarsejtkultúra és a fehérjeexpressziós vizsgálatok sarokkövévé váltak. Ezek a sokoldalú sejtek egyedülálló módon képesek adhezív vagy szuszpenziós kultúrákban növekedni, így a kisléptékű laboratóriumi kutatásoktól a nagyüzemi termelésig számos alkalmazásban jól alkalmazhatók.
Az Sf9 sejtek egyik legfontosabb előnye, hogy kompatibilisek a baculovírus expressziós vektorrendszerrel (BEVS). Ez a nagy teljesítményű eszköz lehetővé teszi a kutatók számára, hogy idegen géneket juttassanak be a sejtekbe módosított baculovírusok segítségével, ami nagy mennyiségű rekombináns fehérje előállítását eredményezi. Az Sf9/BEVS kombináció különösen hatékonynak bizonyult olyan összetett emlősfehérjék expressziójában, amelyek biológiai aktivitásukhoz elengedhetetlen poszt-transzlációs módosításokat igényelnek, mint például a glikoziláció és a megfelelő hajtogatás.
Az Sf9 sejtek sikere a fehérje előállításában széles körben elterjedt vakcinák, terápiás fehérjék és diagnosztikai reagensek előállításához vezetett. Az egyik figyelemre méltó példa a CERVARIX® HPV vakcina előállítása, amely Sf9 sejteket használ a vakcina kulcskomponensének, a humán papillomavírus L1 fehérjéjének kifejezésére. E fehérje nagy mennyiségben és nagy tisztasággal történő előállításának képessége döntő szerepet játszott ennek az életmentő vakcinának a kifejlesztésében és terjesztésében.
A biotechnológiai alkalmazásokon túl az Sf9 sejtek az alapkutatásban is felbecsülhetetlen értékűnek bizonyultak, különösen a rovarbiológia és a gazdatest-patogén kölcsönhatások tanulmányozásában. Mivel a rovarok számos emberi és állati betegség fontos vektorai, a biológiájuk alapjául szolgáló sejtes és molekuláris mechanizmusok megértése kulcsfontosságú betekintést nyújthat a betegségek átvitelébe és a védekezési stratégiákba.
Összefoglalva, az Sf9 sejtek sokoldalúságuk, robusztusságuk és a fehérjeexpresszióban elért páratlan sikereik miatt az orvosbiológiai kutatásban a top 5 sejtvonal között foglalnak helyet. Ahogy a kutatók tovább feszegetik a tudományos ismeretek határait, az Sf9 sejtek kétségtelenül alapvető eszköz maradnak az arzenáljukban, és áttörést hoznak mind az alap-, mind az alkalmazott kutatásban.
4. szám: CHO sejtek
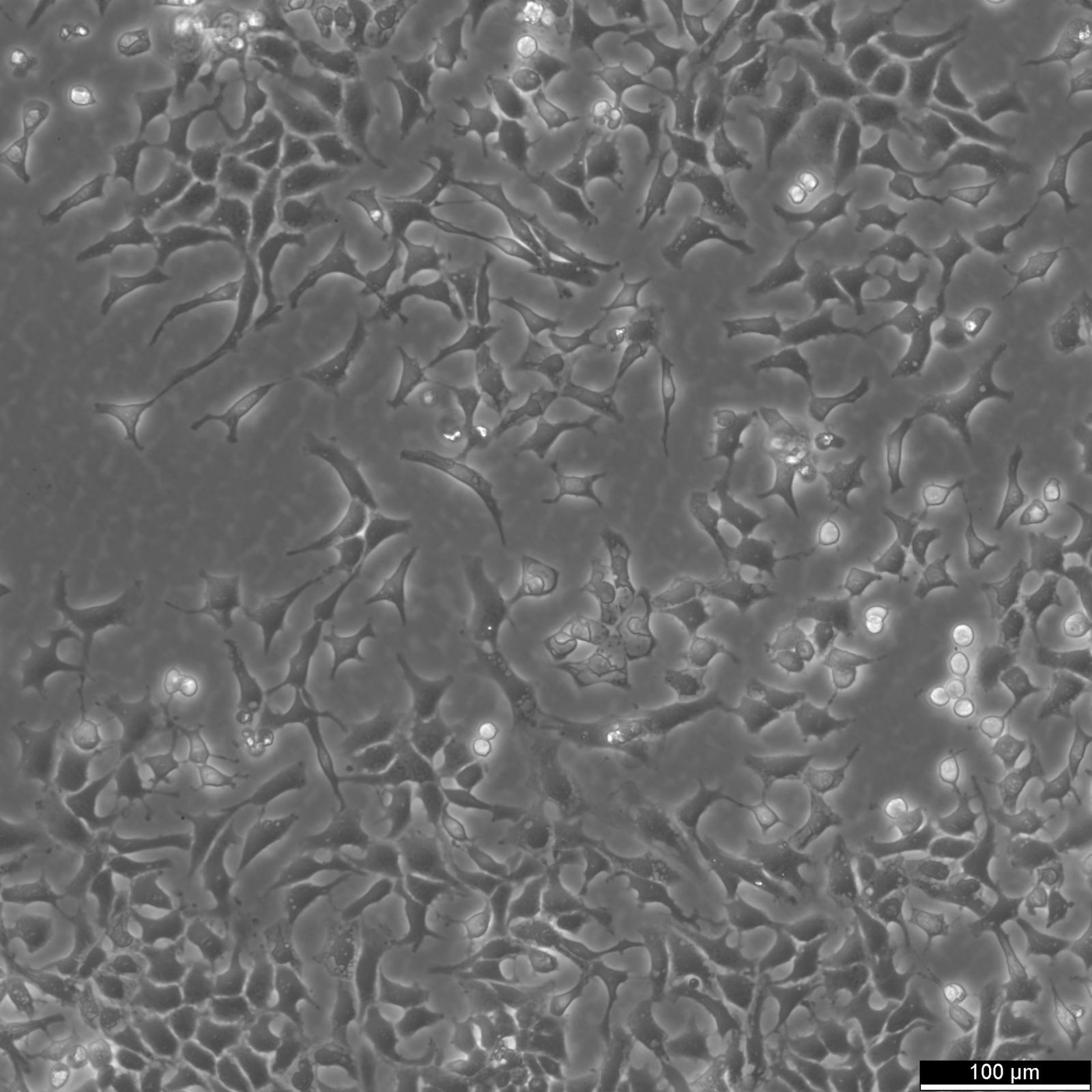
A CHO-sejtek, vagyis a kínai hörcsög petefészek sejtjei az orvosbiológiai kutatás és a biotechnológia világának egyik alapkövévé váltak. Ezek az emlőssejtek, amelyeket először 1957-ben Theodore Puck izolált, rendkívül sokoldalú és robusztus eszköznek bizonyultak az alkalmazások széles skáláján, az alapkutatástól kezdve az életmentő terápiák előállításáig.
A CHO-sejtek sikerének egyik kulcstényezője a különböző tenyésztési körülményekhez való alkalmazkodóképességük. Adherens vagy szuszpenziós tenyészetekben is termeszthetők, lehetővé téve a kutatók számára, hogy szükség szerint növeljék a termelést. A CHO sejtek emellett képesek komplex poszt-transzlációs módosítások, például glikoziláció elvégzésére, amelyek számos emlős fehérje megfelelő működéséhez elengedhetetlenek.
A CHO-sejtek képessége, hogy biológiailag aktív fehérjéket állítanak elő, a biofarmáciai ipar munkagépeivé tette őket. Napjainkban a CHO sejteket terápiás fehérjék széles skálájának előállítására használják, beleértve a monoklonális antitesteket, hormonokat és enzimeket. Valójában a CHO-sejtek felelősek a piacon lévő összes rekombináns fehérje terápiás szer mintegy 70%-ának előállításáért, amelynek becsült globális piaci értéke meghaladja a 100 milliárd dollárt.
A biotechnológiában való alkalmazásukon túl a CHO-sejtek az alapvető biológiai folyamatok megértésében is fontos szerepet játszottak. Például az epidermális növekedési faktor receptor (EGFR) tanulmányozására használták őket, amely a sejtek növekedésének és túlélésének kulcsfontosságú szereplője, és amely a rákban gyakran diszregulált. Az EGFR CHO-sejtekben történő expressziójával a kutatók képesek voltak feltárni a jelátviteli útvonalakat, és célzott terápiákat fejleszteni a tumorok aktivitásának gátlására.
Ahogy a biofarmakonok iránti kereslet egyre nő, úgy nő a CHO-sejtek jelentősége is a kutatásban és a gyártásban. A CHO-sejtvonalak optimalizálására irányuló folyamatos erőfeszítések, mint például a fehérjék hozamának növelése, a glikozilációs minták javítása és a vírusfertőzés kockázatának csökkentése, tovább erősítik pozíciójukat, mint a betegségek elleni küzdelem kritikus eszközét.
Összefoglalva, a CHO-sejtek a biogyógyászati kutatásban a legjobb sejtvonalak között foglalnak helyet alkalmazkodóképességük, komplex emlősfehérjék előállítására való képességük és a biofarmáciai iparban elért széleskörű sikereik miatt. A biológia rejtélyeinek megfejtése és az új terápiák kifejlesztése során a CHO-sejtek kétségtelenül létfontosságú forrás maradnak a tudósok és a gyártók számára egyaránt.
3. szám: Immortalizált emberi sejtvonalak
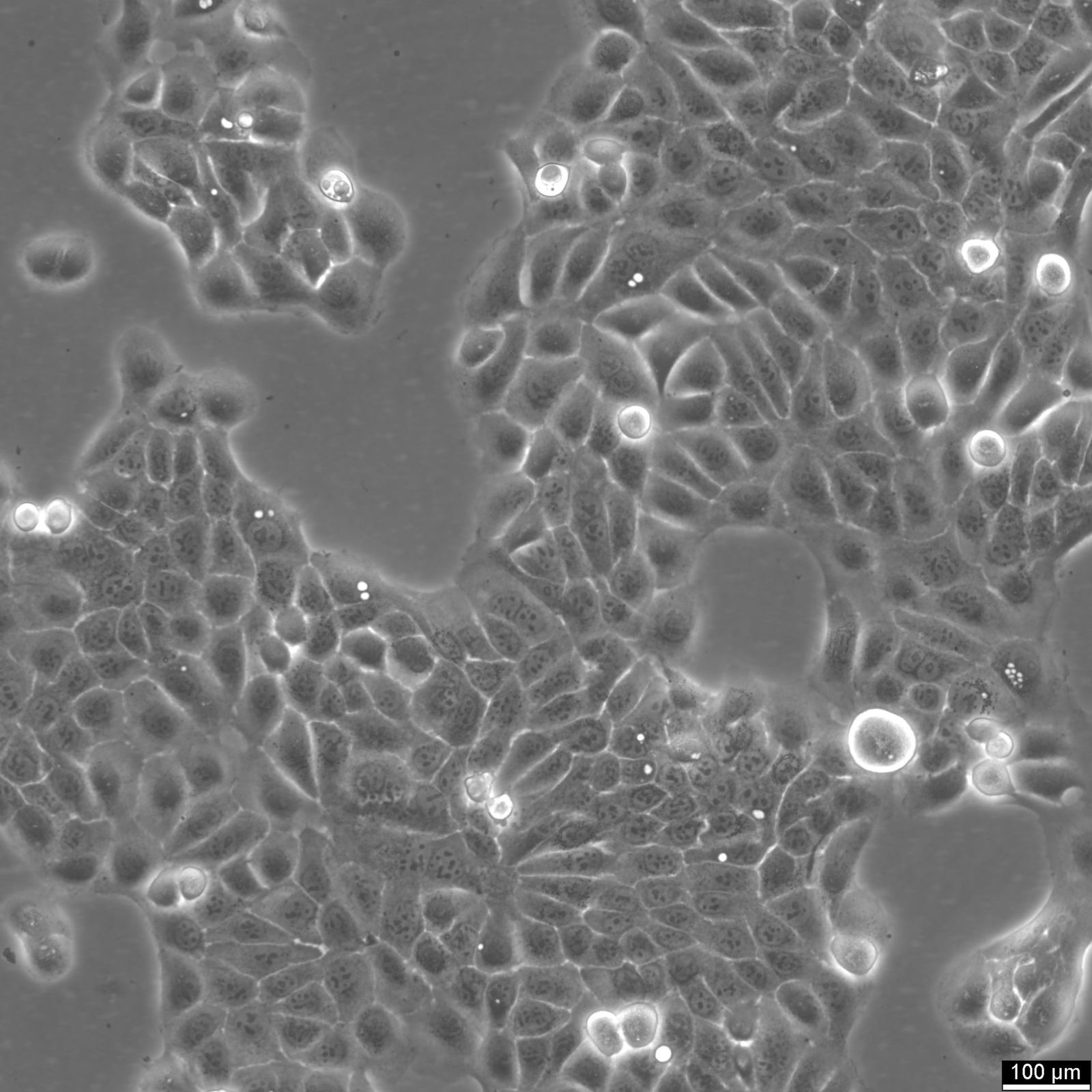
Az immortalizált emberi sejtvonalak nélkülözhetetlen eszközzé váltak az orvosbiológiai kutatásban, mivel a kutatók számára gyakorlatilag végtelen mennyiségű genetikailag egységes sejtet kínálnak az emberi biológia és a betegségek tanulmányozásához. Ezek a sejtvonalak különböző szövetekből származnak, és genetikailag módosították vagy természetes úton szelektálták őket, hogy legyőzzék a sejtosztódás normális korlátait, lehetővé téve számukra a korlátlan szaporodást a kultúrában.
Az immortalizált humán sejtvonalak egyik legjelentősebb előnye, hogy egységes és reprodukálható modellt biztosítanak a humán biológia tanulmányozásához. Azáltal, hogy kiküszöbölik a primer sejtekkel kapcsolatos változékonyságot, amelyek korlátozott élettartammal rendelkeznek és donoronként eltérőek lehetnek, az immortalizált sejtvonalak lehetővé teszik a kutatók számára, hogy nagyobb pontossággal és megbízhatósággal végezzék a kísérleteket.
A ma rendelkezésre álló immortalizált emberi sejtvonalak széles skálája széles, és mindegyik sejtvonal egyedi betekintést nyújt a humán biológia vagy a betegségek sajátos aspektusaiba. Például a humán T-sejtes leukémiából származó Jurkat sejtek fontos szerepet játszanak a T-sejtek jelátvitelének és az immunválasznak a tanulmányozásában. Hasonlóképpen, az MCF-7 sejteket, egy emlőrákos sejtvonalat széles körben használják az emlőrák molekuláris mechanizmusainak vizsgálatára és a potenciális terápiás szerek szűrésére.
Az NCI-60 humán tumorsejtvonalak szűrése, amely kilenc különböző tumortípust képviselő 60 immortalizált humán rákos sejtvonal gyűjteménye, az 1980-as évek végi létrehozása óta értékes forrása a rákkutatásnak. Ezt a panelt több százezer vegyület rákellenes aktivitásának szűrésére használták, ami számos ígéretes gyógyszerjelölt azonosításához vezetett, és elősegítette a rák biológiájának megértését.
Számos előnyük ellenére alapvető fontosságú felismerni az immortalizált emberi sejtvonalak korlátait. Ezek a sejtek a halhatatlanság elérése érdekében jelentős genetikai változásokon mentek keresztül, amelyek nem feltétlenül tükrözik pontosan a normális emberi sejtek in vivo viselkedését. Ezen túlmenően e sejtek hosszú távú tenyésztése további genetikai és fenotípusos változásokhoz vezethet, ami hangsúlyozza a rendszeres sejtvonal-hitelesítés és a minőségellenőrzési intézkedések fontosságát.
Összefoglalva, az immortalizált emberi sejtvonalak forradalmasították az orvosbiológiai kutatást, mivel a biológiai folyamatok és betegségek széles körének tanulmányozásához az emberi sejtek szabványosított és kimeríthetetlen forrását biztosítják. Ahogy a kutatók folytatják az új sejtvonalak kifejlesztését és a meglévők finomítását, ezek a nagy teljesítményű eszközök kétségtelenül központi szerepet fognak játszani a humán biológia megértésében és az új terápiák kifejlesztésében az elkövetkező években.
2. szám: HEK293 sejtek
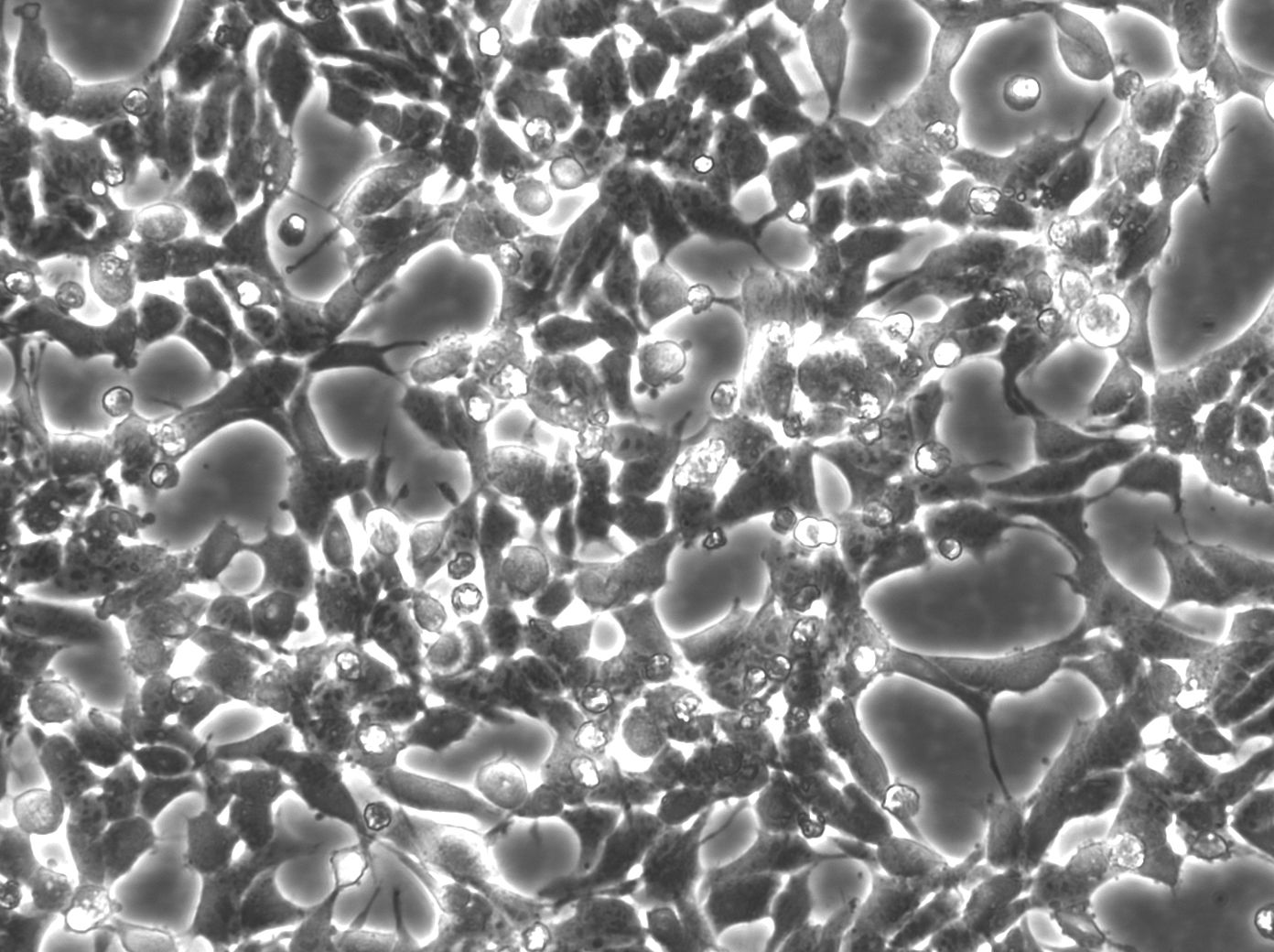
AHEK293 sejtek, vagyis a Humán embrionális vese 293 sejtek sokoldalúságuk, könnyű tenyészthetőségük és nagyfokú transzfecálhatóságuk miatt az egyik legszélesebb körben használt sejtvonalakká váltak az orvosbiológiai kutatásban. Ezeket a sejteket eredetileg 1973-ban emberi embrionális vesesejtekből nyerték adenovírus DNS-sel történő transzformációval, és azóta számos alkalmazáshoz adaptálták őket.
A HEK293 sejtek egyik fő erőssége, hogy a megfelelő expressziós vektorokkal transzfektálva nagy mennyiségű rekombináns fehérjét képesek kifejezni. Ez felbecsülhetetlen értékű eszközzé tette őket a fehérjék működésének, a jelátviteli útvonalak és a gyógyszer-fehérje kölcsönhatások tanulmányozására. A HEK293 sejtek emellett képesek a megfelelő fehérjefunkcióhoz szükséges számos poszttranszlációs módosítás elvégzésére, ami biztosítja, hogy az ezekben a sejtekben előállított rekombináns fehérjék nagyon hasonlítanak natív társaikra.
A HEK293 sejteket a fehérjeexpressziós vizsgálatokban való hasznosságukon túl a génterápia területén is széles körben használják. Ezek a sejtek rendkívül megengedőek a vírusfertőzés és -szaporodás szempontjából, így ideális platformot jelentenek a génszállításban használt vírusvektorok előállításához. Valójában a HEK293 sejteket számos, az FDA által jóváhagyott génterápiás termék, például a gerincvelői izomsorvadás kezelésére szolgáló Zolgensma® előállítására használták.
Az utóbbi években a HEK293 sejtek értékes eszközként jelentek meg az ioncsatornák és a G-fehérje kapcsolt receptorok (GPCR) tanulmányozásában is. E fehérjék HEK293 sejtekben történő expressziójával és fejlett elektrofiziológiai technikák alkalmazásával a kutatók új betekintést nyerhettek szerkezetükbe, működésükbe és farmakológiájukba. Ez új gyógyszercélpontok azonosításához és szelektívebb és hatásosabb terápiák kifejlesztéséhez vezetett.
Számos előnyük ellenére fontos elismerni, hogy a HEK293 sejtek nem korlátlanok. Immortalizált sejtvonalként nem mindig tükrözik pontosan a normál emberi sejtek in vivo viselkedését. Ráadásul az e sejtek létrehozásához használt adenovírusos transzformáció jelentős genomiális átrendeződéseket és a génexpresszióban bekövetkezett változásokat eredményezett, ami hatással lehet biológiai tulajdonságaikra.
Összefoglalva, a HEK293 sejtek sokoldalúságuk, nagyfokú transzfecálhatóságuk és a fehérjeexpresszió, génterápia és ioncsatorna/GPCR-vizsgálatok terén elért széleskörű eredményeik miatt az orvosbiológiai kutatások egyik legfontosabb sejtvonalaként érdemelték ki helyüket. Ahogy a kutatók tovább feszegetik a tudományos ismeretek határait, a HEK293 sejtek kétségtelenül a humán biológia és a betegségek összetettségének feltárására szolgáló eszköz maradnak.
1. szám: HeLa sejtek

AHeLa-sejtek, az első halhatatlan emberi sejtvonal lenyűgöző és ellentmondásos története kitörölhetetlen nyomot hagyott az orvosbiológiai kutatásokban. A Henrietta Lackstól 1951-ben levett méhnyakrákos sejtekből származó HeLa sejtek több mint fél évszázada a tudományos felfedezések élvonalában vannak, és számos áttöréshez járultak hozzá a rákkutatástól a vakcinák kifejlesztéséig terjedő területeken.
A HeLa-sejtek egyik legfigyelemreméltóbb tulajdonsága a kivételes ellenálló képességük és alkalmazkodóképességük. Ezek a sejtek sokféle körülmények között képesek túlélni és szaporodni, így ideális modellként szolgálnak a gyógyszerek, toxinok és egyéb környezeti tényezők emberi sejtekre gyakorolt hatásainak tanulmányozására. A HeLa sejtek továbbá szokatlanul magas telomeráz aktivitással rendelkeznek, ami lehetővé teszi számukra, hogy megőrizzék telomerjeiket és elkerüljék a sejtek öregedését, ami hozzájárul halhatatlanságukhoz.
A HeLa sejtek hatását az orvosbiológiai kutatásra nem lehet eléggé hangsúlyozni. A sejtbiológia gyakorlatilag minden aspektusának tanulmányozására felhasználták őket, az olyan alapvető sejtfolyamatoktól kezdve, mint a DNS-replikáció és a fehérjeszintézis, egészen az olyan összetett betegségmechanizmusokig, mint a vírusfertőzés és a rák progressziója. Valójában a HeLa sejtek fontos szerepet játszottak a gyermekbénulás elleni vakcina kifejlesztésében az 1950-es években, és azóta számos vírus, köztük a HIV, a Zika és a SARS-CoV-2 tanulmányozására használják őket.
A HeLa sejtek története azonban nem ellentmondásmentes. Évtizedekig a nyilvánosság számára ismeretlen volt e sejtek eredete, és Henrietta Lacks családja nem tudott arról, hogy sejtjeit az ő beleegyezése nélkül vették el és használták fel kutatásra. Ez fontos etikai kérdéseket vet fel a tájékozott beleegyezéssel, a betegek magánéletével és az emberi szövetek árucikké tételével kapcsolatban.
Az elmúlt években erőfeszítéseket tettek Henrietta Lacks tudományhoz való hozzájárulásának elismerésére, és arra, hogy a családjával együtt részt vegyenek a HeLa sejtek felhasználásáról szóló vitákban. 2013-ban a Nemzeti Egészségügyi Intézetek megállapodást kötöttek a Lacks családdal a HeLa genomadatokhoz való hozzáférési munkacsoport létrehozásáról, amely bizonyos fokú ellenőrzést biztosít a család számára a HeLa genomadatok kutatásban való felhasználása felett.
A származásukkal kapcsolatos etikai aggályok ellenére a HeLa-sejtek továbbra is az orvosbiológiai kutatás alapvető eszközei. Egyedülálló tulajdonságaik és történelmi jelentőségük megszilárdította helyüket a világ legszélesebb körben használt és legbefolyásosabb sejtvonalaként. Miközben továbbra is küzdünk a HeLa-sejtek tudományos és etikai következményeivel, egyértelmű, hogy a tudományra és a társadalomra gyakorolt hatásuk még nemzedékekig fennmarad.
Következtetés
Az ebben a cikkben vizsgált 5 legfontosabb sejtvonal - Sf9, CHO, immortalizált emberi sejtvonalak, HEK293 és HeLa - mindegyike kulcsfontosságú szerepet játszott a biológia és a betegségek megértésében. Ezek a sejtvonalak felbecsülhetetlen értékű eszközként szolgáltak a kutatók számára, lehetővé téve úttörő felfedezéseket, és megnyitva az utat új terápiák és kezelések előtt.
Az orvosbiológiai kutatás jövőjét tekintve egyértelmű, hogy a sejtvonalak továbbra is a tudományos fejlődés motorjai lesznek. Azáltal, hogy szabványosított és hozzáférhető modellt biztosítanak az összetett biológiai folyamatok tanulmányozásához, a sejtvonalak lehetővé teszik a kutatók számára, hogy új kérdéseket tegyenek fel, merész hipotéziseket teszteljenek, és kitolják a lehetőségek határait.
A HeLa sejtek története azonban arra emlékeztet minket, hogy a sejtvonalak felhasználása a kutatásban nem mentes az etikai és társadalmi következményektől. Tudósként felelősségünk, hogy foglalkozzunk ezekkel a kérdésekkel, és biztosítsuk, hogy munkánkat a betegek autonómiájának, magánéletének és méltóságának maximális tiszteletben tartásával végezzük.
Végső soron az orvosbiológiai kutatás sikere nemcsak a tudományos eszközeink erejétől függ, hanem attól is, hogy milyen tisztességgel és együttérzéssel használjuk azokat. A sejtvonal-kutatásban rejlő tudományos lehetőségek és etikai kihívások felvállalásával továbbra is megfejthetjük az élet rejtélyeit, és olyan jövőért dolgozhatunk, amelyben a tudományos fejlődés előnyeit mindenki élvezheti.
