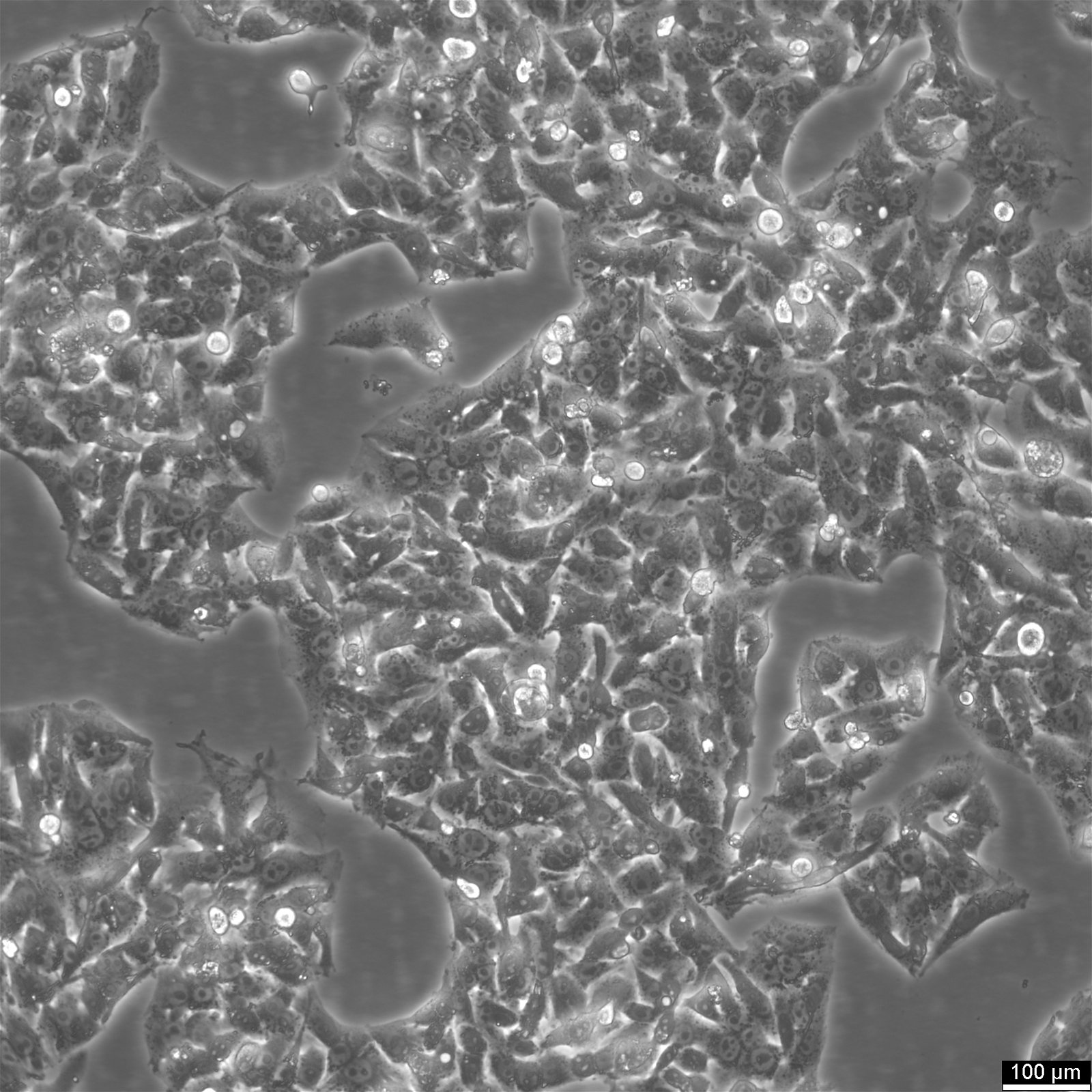
HepG2 sejtek - Májrákkutatási erőforrás
AHep-G2 egy emberi májrákos sejtvonal, amely egy 15 éves kaukázusi férfi májszövetéből származik, aki hepatocelluláris karcinómában szenvedett. Ezeket a sejteket gyakran használják gyógyszer-metabolizmus és májtoxicitás vizsgálatokban. Bár a HepG2 sejtek magas proliferációs rátával és epithelszerű megjelenéssel rendelkeznek, nem tumorigén és különböző differenciált májfunkciókat látnak el. 1975-ben a kutatók a HepG2 sejteket hepatocelluláris karcinómából származtatták, így ez volt az első májsejtvonal, amely a hepatociták kritikus jellemzőit mutatta. A korábban létrehozott SK-Hep1 sejtvonallal ellentétben, amelyből hiányoznak az alapvető májsejtmarkerek, a HepG2 sejtek képesek különböző plazmafehérjéket szekretálni, és értékes modellt biztosítanak a humán hepatociták sejtfelszíni domének intracelluláris dinamikájának tanulmányozásához. Ezek a sejtek epithelszerű morfológiát mutatnak, kromoszómaszámuk 55, és humán növekedési hormonnal stimulálhatók.
HepG2 jellemzők
Az elsődleges hepatociták tipikus alakja kocka alakú, és általában két magot tartalmaz. Ezzel szemben a HepG2 sejtek epithelszerű morfológiával rendelkeznek, egyetlen sejtmaggal és sejtenként 48-54 kromoszóma számmal. Bár a HepG2 sejtek a teljes sejtfehérje akár 25%-át is kitehetik, méretük nagyobb, mint a normál hepatocitáké, a teljes sejtfehérje mintegy 10%-át teszik ki. A sejtfehérjék kritikus szereplők a sejten belül, a gének által meghatározott funkciókat hajtják végre.
A daganatos sejtek, beleértve a kromoszómák rendellenes számával rendelkező sejteket is, gyakran mutatják a sejtmagok számának növekedését, sejtenként akár hétre is. Magas fokú in vitro differenciáltságuk miatt a HepG2 sejtek ideális modellt jelentenek az epecsatorna-, szinuszoidális membránfehérjék és lipidek intracelluláris forgalmának és dinamikájának tanulmányozására a humán hepatocitákban.
A HepG2 sejtek átlagos átmérője 10-20 µm körül van, ami kisebb, mint a 15 µm átmérőjű hepatocitáké, de hasonló a hepatoblasztóma (HB) tumorsejtjeihez, amelyek átmérője 10-20 µm között mozog.
HepG2 genetika
A Hep-G2 sejtvonal számos transzlokációt mutat, többek között az 1. és 21. kromoszóma rövid karjai között, a 2., 16. és 17. kromoszóma triszómiáit, valamint a 20. kromoszóma tetraszómiáját. A 4q3 kromoszóma régiójának elvesztése is megfigyelhető, amely a hepatoblasztómában (HB) gyakran megfigyelhető t(1;4) transzlokációhoz és más kromoszóma-rendellenességekhez, például a 2. és 20. kromoszóma triszómiájához társul. A HepG2 sejtekben a kromoszómák száma 50 és 60 között mozog, ami hiperdiploid kariotípust jelez, míg egyes esetekben több mint 100 kromoszómát mutatnak, és tetraploid megnagyobbodás jellemzi őket. A HepG2 sejtek körülbelül 7,5 pg DNS-t tartalmaznak, 15%-kal többet, mint egy átlagos szomatikus sejt. Ehhez képest a primer hepatociták kocka alakú sejtek, és jellemzően két sejtmagot tartalmaznak [1].
A HepG2 sejtek mutációs profilja
A HepG2 sejtvonal a TERT promóter régió C228T mutációját hordozza, amely a hepatocelluláris karcinómában (HCC) és a hepatoblasztómában (HB) is jelen van. Ez a mutáció a rákos sejtek telomerjeinek védelme révén hozzájárul az immortalizációhoz. Emellett a HepG2 sejtek vad típusú TP53-at mutatnak, amely kritikus gén az emberi rák elnyomása szempontjából, mivel szerepet játszik a sejtciklus megállításában, az apoptózisban és az öregedésben. E gén mutációi elősegíthetik a sejtek proliferációját.
A HepG2 sejtek számos útvonalban vesznek részt, beleértve a sejtnövekedés, a túlélési útvonalak, mint például a magzati és embrionális HB, valamint a Wnt/β-katenin útvonal diszregulációját. A sejtvonal továbbá a CTNNB1 gén harmadik exonjának jellegzetes deléciójával rendelkezik, amely megegyezik az epithelialis típusú HB-ban megfigyelhető delécióval [2,3].
A HepG2 hepatocelluláris karcinóma sejtek áttekintése a májkutatásban
Az emberi hepatomából származó HepG2 sejtek felbecsülhetetlen értékű eszközzé váltak a májfunkciók és a májbetegségek, köztük a hepatocelluláris karcinóma kutatásában. Ezek a májsejtvonalak betekintést nyújtanak a humán hepatociták sejtválaszaiba különböző kísérleti körülmények között. A luciferáz riporter plazmidok használata a HepG2 sejtekben különösen hatékony a génexpresszió és a sejttranszfekciók nyomon követésére, amelyek alapvető fontosságúak az anyagcsere-kutatásban, például az etanol májsejtekre gyakorolt hatásának vizsgálatában
Vírusfertőzések és májbetegségek vizsgálata HepG2 sejtek felhasználásával
Az olyan immortalizált májtumor-sejtvonalak, mint a HepG2 és a Huh7, alapvető fontosságúak a vírusfertőzések tanulmányozásában, mivel a hepatitis D (HDV) teljes sejtciklusú replikációját és a hepatitis B (HBV) expresszióját mutatják [5,6]. Ezzel párhuzamosan a HepaRG sejtvonalak kritikus szerepet játszanak a HBV belépési mechanizmusainak feltárásában [7]. A HepG2 sejteket számos humán májbetegség vizsgálatára is alkalmazzák, a genetikai állapotoktól kezdve, mint a progresszív familiáris intrahepatikus kolesztázis (PFIC) és a Dubin-Johnson-szindróma, a citotoxikus és genotoxikus szerekkel kapcsolatos környezeti és étrendi vizsgálatokig, valamint a gyógyszercélzás és a hepatokarcinogenezis kutatásában [8,9]. Használatuk kiterjed a bio-mesterséges májeszközökkel végzett vizsgálatokra is
A HepG2 sejtek kölcsönhatásai a biomatériákkal a szövetszerkesztés során
A HepG2 sejtek és a különböző biomaterialok kölcsönhatása kulcsfontosságú a szövetmérnöki munkában. Az olyan technikák, mint a kolloid szondatechnika, segítenek megérteni ezeket a kölcsönhatásokat a sejtek adhéziós tulajdonságainak mérésével, amelyek létfontosságúak a sejtek életképességének meghatározásához az állványok és a pontos májszövetmodellek kifejlesztéséhez
A sejtek viselkedése és innovációk a HepG2-alapú modellekben
A sejtek viselkedésének tanulmányozása a HepG2-alapú modellekben kulcsfontosságú a májbetegségek kutatásában. A háromdimenziós szferoid sejtkultúrákban elért fejlődés a HepG2 sejtek szferoidjainak létrehozásához vezetett, amelyek fiziológiailag relevánsabb modellt kínálnak, amely a normális hepatocitákhoz közelebb áll. Ezek a fokozott metabolikus aktivitással rendelkező 3D modellek azt jelzik, hogy a HepG2 sejtek a hepatoblasztóma modelljeként szolgálhatnak, és jelentősek a rákkezelési kutatásokban, különösen a májtumorok szimulálása és az új terápiás megközelítések tesztelése szempontjából [10-12]
A HepG2 összehasonlítása és jellemzői más tumorsejtvonalak között
A HepG2 az egyik legszélesebb körben használt májtumor-sejtvonal, amelyet a tudományos kutatásban való széles körű alkalmazása miatt választottak ki a mintegy 40 rendelkezésre álló májtumor-sejtvonal közül [13]. Annak ellenére, hogy bizonyos citokróm P450 enzimek a normál hepatocitákhoz képest gyengén vagy egyáltalán nem expresszálódnak, a HepG2 metabolikus profilja ösztönözte a sejtvonal módosítására irányuló erőfeszítéseket a jobb gyógyszeranyagcsere-vizsgálatok érdekében [13]. Az olyan tumoros sejtvonalakkal összehasonlítva, mint az MCF7, PC3, 143B és HEK293, a HepG2 sejtek egyedi aminosavtartalom-profilt mutatnak, amely jelentősen befolyásolja a fehérjeszintézist és a szekréciót, kiemelve egyedi metabolikus útvonalaikat [14]
A májbetegségekkel kapcsolatos kutatások felfedezése a HepG2-vel
HepG2 sejtek szubkultiválása
Az alábbi öt lépésben eltávolíthatjuk az Accutase segítségével a sejttenyésztő lombikokból a megtapadt sejteket:
- Távolítsa el a tápfolyadékot a sejttenyésztő lombikból, és öblítse le a megtapadt sejteket kalcium- és magnéziummentes PBS-sel. T25-ös lombikokhoz 3-5 ml PBS-t, T75-ös lombikokhoz 5-10 ml-t használjon.
- Adjunk Accutázt a sejttenyésztő lombikhoz, T25 lombikonként 1-2 ml-t, T75 lombikonként 2,5 ml-t használva. Ügyeljen arra, hogy az Accutase a teljes sejtlapot befedje.
- Inkubálja a lombikot szobahőmérsékleten 8-10 percig.
- Óvatosan reszuszpendálja a sejteket a tápfolyadékkal, 10 ml friss tápfolyadékot használva.
- Centrifugálja a reszuszpendált sejteket 5 percig 300xg-nél, szuszpendálja őket újra friss tápfolyadékban, és adagolja őket friss tápfolyadékot tartalmazó új lombikokba.
A HepG2 sejtek jövőbeli kilátásai
A HepG2 sejtvonalban rejlő teljes potenciál feltárása a citokrómok expressziójának növelése terén elért úttörő eredményekkel folytatódik. A kutatók a háromdimenziós szferoid sejtkultúrák lehetőségét is vizsgálják, amelyek fiziológiailag relevánsabb rendszert kínálnak. A metabolikus aktivitás, beleértve a citokrómokat is, figyelemre méltóan magasabb a 3D szferoid HepG2 modellekben, mint a 2D sejtekben, ami közelebb visz minket egy olyan modell létrehozásához, amely a normális hepatocitákat tükrözi. Emellett a sejtfelszíni fehérjék helytelen eloszlásának hátterében álló dinamikus folyamatok feltárása utat nyithat a májbetegségek jobb megértéséhez
HepG2 sejtek: GYIK
Hivatkozások
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiation-induced chromosomal breakage and rejoining in interphase-metaphase chromosomes of human lymphocytes, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4 Inhibition: Új terápiás stratégia a P53 reaktiválására a hepatoblasztómában. Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53 Mutations and hepatocellular Carcinoma: Insights into the Etiology and Pathogenesis of Liver Cancer. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Kritikai vizsgálat a Hepatoma sejtvonalak HepG2 és Huh7 használhatóságáról, mint modellekről a reszekálható hepatocelluláris karcinóma metabolikus reprezentációjára. Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Cell culture Models for the Investigation of Hepatitis B and D Virus Infection. Viruses 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Viruses. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Infection of a Human Hepatoma Cell Line by Hepatitis B Virus. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. Egy humán eredetű májsejtvonal felhasználása citoprotektív, antigenotoxikus és kogenotoxikus anyagok kimutatására. Toxikológia. 2004; 198(1-3): 329-340.
- Fanelli, A. HepG2 (máj hepatocelluláris karcinóma): sejttenyésztés. HepG2. Letöltve 2017. december 3.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Cytochrome P450-eket expresszáló HepG2-eredetű sejtek fejlesztése a metabolizmushoz kapcsolódó gyógyszer-indukált májtoxicitás értékelésére. Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. Az in vitro anyagcsere-aktiválás alkalmazása a nagy áteresztőképességű szűrésben. Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. A dehidroepiandroszteron-szulfotranszferáz gén lefelé szabályozása humán hepatocelluláris karcinómában. Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Cancer stem/progenitor cells are highly enriched in CD133 + CD44 + population in hepatocellular carcinoma. Int J Cancer. 2010; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. A cianemazin metabolizmusában részt vevő humán citokróm P450 enzimek jellemzése. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.