HeLa sejtek: A kutatás forradalmasítása
1951-es felfedezésük óta a Hela sejteket, a Henrietta Lacksról elnevezett halhatatlan sejtek törzsét széles körben alkalmazzák a tudományos kutatásban. Henrietta Lacks, egy 31 éves afroamerikai, ötgyermekes anya, halála évében méhnyakrákot diagnosztizáltak nála. George Otto Gey, a Johns Hopkins Kórház szövettenyésztési laboratóriumának igazgatója összegyűjtötte és szaporította a méhnyakrákos sejtjeit, amelyek kivételesen ellenállónak és termékenynek bizonyultak, ami lehetővé tette széles körű alkalmazásukat a tudományos kutatásban. Más emberi sejtekkel ellentétben a HeLa-sejteket in vitro fenn lehetett tartani és szaporítani, ami jelentős előrelépést jelentett az orvosi kutatásban.
A Hela sejtek története és idővonala
Henrietta Lacks, egy fekete dohánytermesztő 1951-ben került a Johns Hopkins Kórházba rendellenes hüvelyi vérzés miatt, később pedig méhnyakrák miatt kezelték. Első terápiája abból állt, hogy a beleegyezése nélkül szövetmintát vettek a méhnyakából. A méhnyakbiopszia során George Otto Gey klinikai vizsgálata számára szövetmintákat nyertek, amelyeket a szövettenyésztő laboratóriumban tanulmányoztak. A korábbi mintákkal ellentétben Gey laborasszisztense észrevette, hogy a sejtek 20-24 óránként megduplázódnak és gyorsan növekednek. Gey közvetlenül Lacks halála előtt szaporította a méhnyakrákos sejteket, és ezek voltak az első életképes emberi in vitro sejtvonal. A sejteket Henrietta Lacks kereszt- és vezetéknevének első két betűje után nevezték el, és minden olyan tudósnak odaadták, aki a kutatás előmozdítása érdekében kérte őket.
Bár a sejteket Lacks vagy családja engedélye nélkül gyűjtötték össze, az engedélyt akkoriban nem volt szükséges és nem is szokás kérni. A betegeket vagy családtagjaikat nem volt kötelességük figyelmeztetni arra, hogy a kidobott vagy műtéti úton nyert anyagok az orvos vagy az egészségügyi intézmény tulajdonát képezik. Az 1970-es években egy nyilvános szivárgás során nyilvánosságra került Henrietta valódi neve, és a Lacks családtól DNS-mintákat kértek, hogy segítsenek a szennyezett sejtvonalak azonosításában. A HeLa sejtvonal Lacks méhnyakszövetének egy mintájából származik, és sejtkultúrában olyan mértékben szaporodott, hogy az jóval meghaladta a testében lévő összes sejt számát. A HeLa sejteknek több törzse létezik, mivel a sejtkultúrákban tovább mutálódnak, de mindegyik a Lacksból kivont tumorsejtek leszármazottja.
A történelmi sérelmek kezelése
A Henrietta Lacks és a HeLa-sejtek tudta és beleegyezése nélkül történő leválasztása körüli történet az orvosi kutatási gyakorlatok etikájáról és az egyéni jogok védelméről szóló vitát indított el, különösen az emberi biológiai anyagok tudományos felhasználása kapcsán. Henrietta Lacks tudtán kívül az első halhatatlan emberi sejtvonal forrásává vált, amely azóta számtalan tudományos áttöréshez vezetett. Ennek az etikai vétségnek a felismerése katalizálta a szigorúbb beleegyezési eljárások felé való elmozdulást, és a kutatók erkölcsi kötelezettségeinek fokozott tudatosítását. Ez az eset nemcsak a kutatási gyakorlatok reformjának szükségességére világított rá, hanem szélesebb körű beszélgetést is elindított az igazságosságról, a tiszteletről és az elismerésről az orvosi kutatásban, ami a múltbeli igazságtalanságok orvoslására irányuló erőfeszítésekhez vezetett, és biztosította, hogy a tudományos fejlődéshez hozzájáruló személyeket elismerjék és méltósággal kezeljék.
Thermo Fisher és a HeLa sejtek
A Thermo Fisher Scientific biotechnológiai vállalat ellen a HeLa sejtekkel kapcsolatban indított per mélyebb etikai és jogi vitában gyökerezett, amely az egyénekből származó biológiai anyagok hozzájárulásuk nélkül történő kereskedelmi forgalomba hozataláról szólt. Az ügy középpontjában a HeLa-sejtvonal állt, amely jelentős tudományos áttörésekhez vezetett, többek között a gyermekbénulás elleni vakcina kifejlesztéséhez és a rákkezelés terén elért eredményekhez.
A per több etikai megfontolásra is rávilágított: az egyének és családtagjaik jogaira biológiai anyagaik felett, a marginalizált személyektől hozzájárulás nélkül történő mintavétel történelmi összefüggéseire, valamint az ilyen anyagokból hasznot húzó vállalatok felelősségére. A Thermo Fisher Scientific elleni ügy rávilágított arra, hogy világosabb irányelvekre és etikai normákra van szükség az emberi biológiai anyagok kutatásban és kereskedelemben történő felhasználásával kapcsolatban, biztosítva az egyének jogainak tiszteletben tartását és a tudományos felfedezésekből származó előnyök méltányos megosztását.
A HeLa-sejtekkel kapcsolatos eredet, jogi csatározások és megoldások részletes feltárása a"HeLa-sejtek" című cikkünkben olvasható:Történet, per és egyezségek" című cikkében
A HeLa sejtek lenyűgöző tulajdonságai
A HeLa sejtek könnyen tenyészthetők és gyorsan szaporodnak, valamint a vírusfertőzésekkel szembeni nagyfokú érzékenységükről is ismertek. Különösen fogékonyak a humán adenovírus 3, az encephalomyocarditis vírus és a poliovírus 1, 2 és 3 ellen. Ez a tulajdonság teszi a HeLa sejteket nélkülözhetetlenné e vírusok szaporodásának, összeszerelődésének és patogenezisének tanulmányozásához, valamint új vírusellenes stratégiák kifejlesztéséhez. Ezenkívül a HeLa sejteket széles körben használják transzfekciós gazdatestként a génfunkció és -szabályozás, a rekombináns fehérjék előállítása és a génterápia tanulmányozására.
- A HeLa sejtek még a rákos sejtekhez képest is abnormálisan magas sejtburjánzási rátával és korlátlan élettartammal rendelkeznek, így kiválóan alkalmasak tudományos vizsgálatokra.
- A HeLa sejtek aktív telomeráz formával rendelkeznek, ami lehetővé teszi a korlátlan sejtosztódást és a halhatatlanságot.
- A HeLa sejtek legyőzik a Hayflick-határt, vagyis azt a maximális számú sejtosztódást, amelyen a legtöbb normális sejt áteshet, mielőtt elöregedne.
- A HeLa sejtek hipertriploid kromoszómaszámmal rendelkeznek (3n+). A HeLa sejtek átlagos kromoszómaszáma 82, de 70 és 164 között változhat (a standard 46-os diploid kromoszómaszám helyett). Ezeket a kromoszómákat "HeLa szignifikáns kromoszómáknak" nevezik. A Hela sejtek komplex kariotípussal rendelkeznek, amelyet nagyfokú aneuploidia és strukturális átrendeződések jellemeznek. A HeLa sejtek 98%-ában kis telocentrikus kromoszómát találunk, és 1385 vizsgált sejtben 100%-os aneuploidia figyelhető meg. Ezek a kromoszóma-rendellenességek alapvető szerepet játszanak a HeLa sejtek gyors növekedési ütemében és halhatatlanságában, és a méhnyakrákkal is összefüggésbe hozhatók.
- A humán papillomavírus 18 (HPV18) emberi méhnyaksejtekbe történő horizontális génátvitelének köszönhetően a HeLa sejtek Henrietta Lacksétől eltérő genommal rendelkeznek.
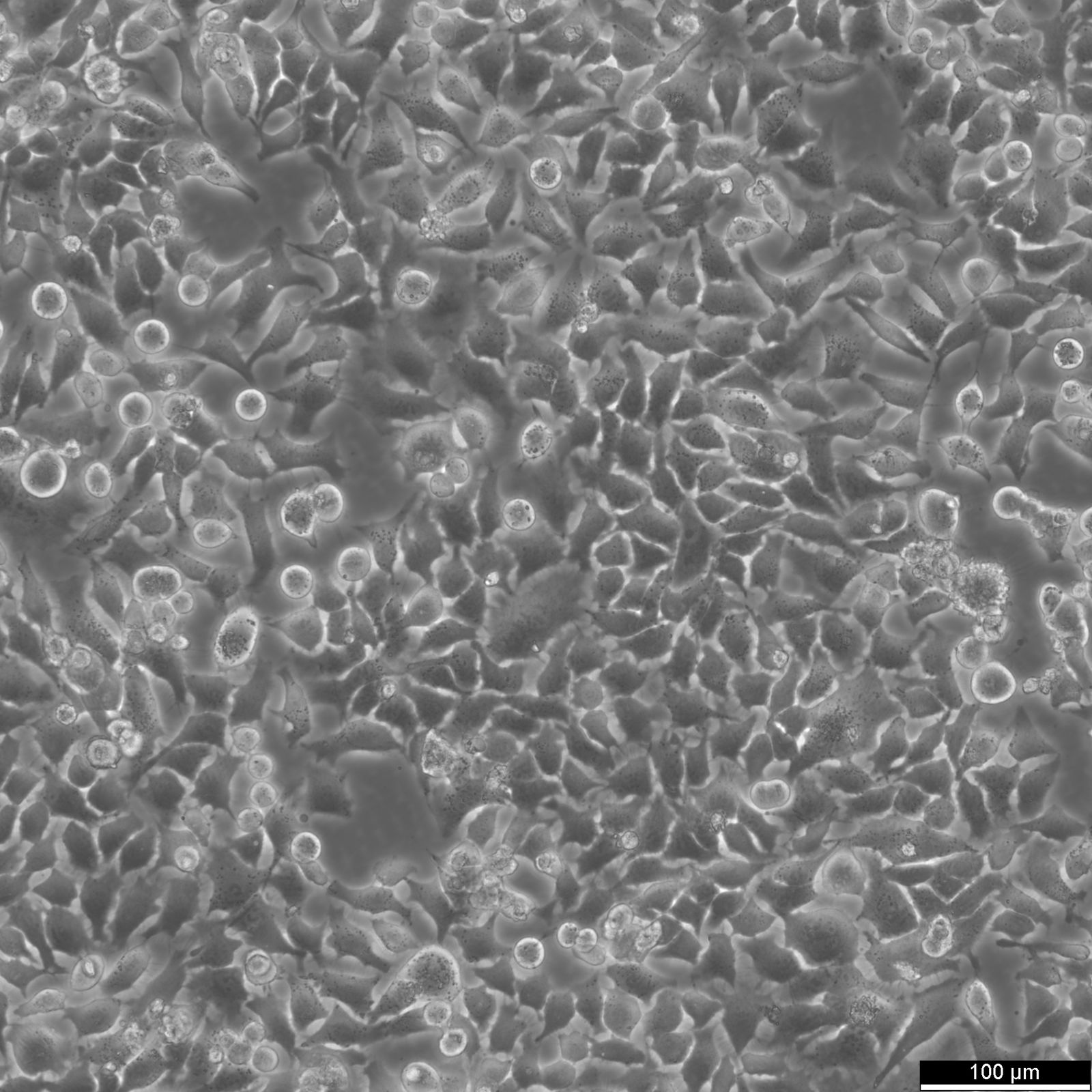
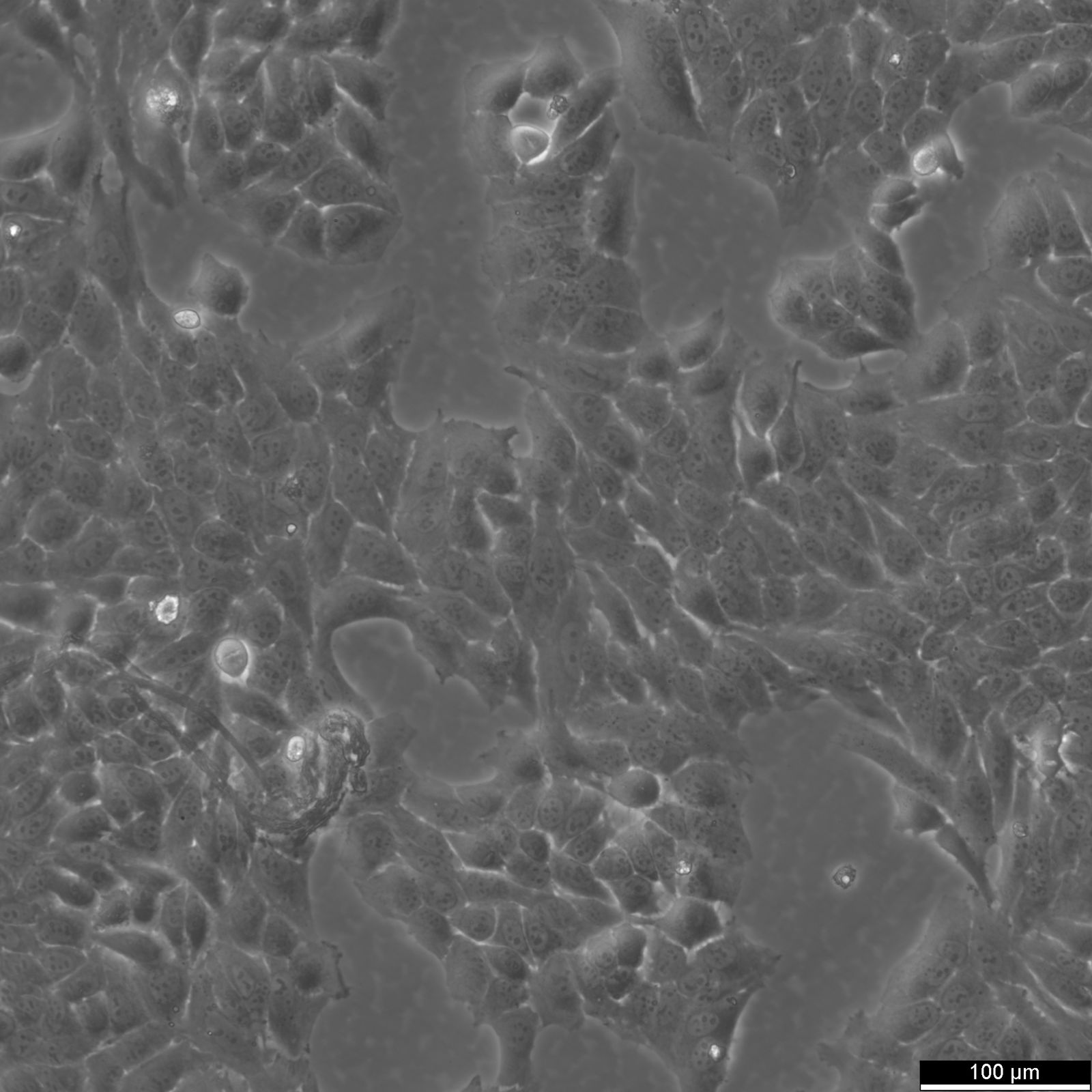
A HeLa sejtek szerkezete
A HeLa sejtek átmérője a tenyésztési körülményektől függően 10-20 µm. A legtöbb emlőssejt átmérője 10 és 100 µm között van. Az egyik legkisebb emberi sejt, a vörösvértestek átmérője körülbelül 8 µm. Másrészt az izomrostsejtek és az idegsejtek rendkívül hosszúak lehetnek.
A kutatás a HeLának köszönhetően fejlődik
A HeLa sejtek jelentős kutatási eredmények középpontjában álltak, beleértve a genetika, a virológia és a terápiás fejlesztés területén tett felfedezéseket. A HeLa sejtvonalat használták a rák, az AIDS, a sugárzás és a toxinok hatásainak, a géntérképezésnek és számtalan más tudományos törekvés tanulmányozására. Több mint 60 000 tudományos cikket publikáltak a HeLa-kutatásról, és havonta több mint 300-zal növekszik a számuk.
Polio felszámolása
Az 1950-es években Jonas Salk HeLa-sejtek felhasználásával tesztelte az első gyermekbénulás elleni vakcinát. Ezek a sejtek fogékonyak voltak a poliomyelitis fertőzésre, ami a fertőzött sejtek elhalásához vezetett. Ennek eredményeképpen a HeLa sejtek nagy keresletnek örvendtek a polio vakcina tesztelésében, mivel az eredmények könnyen elérhetőek voltak.
Virológia
A HeLa sejteket számos vírussal, köztük HIV-vel, Zikával, herpesszel és mumpsszal fertőzték meg, hogy új vakcinákat és gyógyszereket teszteljenek és fejlesszenek ki. Dr. Richard Axel felfedezte, hogy a HeLa sejtek a CD4 fehérje hozzáadásával HIV-vel is megfertőzhetők, így a vírus tanulmányozhatóvá válik. A HeLa sejteket a papillomavírus E2 expressziójának és apoptózisának kutatására használták, és alapvető szerepet játszottak a humán papillomavírus (HPV) elleni vakcinák kifejlesztésében is.
Rák
A HeLa-sejteket számos rákkutatásra használták, beleértve a nemi szteroid hormonok, például az ösztradiol, az ösztrogén és az ösztrogénreceptorok, valamint az ösztrogénszerű vegyületek, például a kvercetin és annak rákmegelőző tulajdonságai vizsgálatát. A HeLa sejteket használták a flavonoidok és antioxidánsok ösztradiollal együtt a rákos sejtek proliferációjára gyakorolt hatásának tanulmányozására is.
Egyéb figyelemre méltó alkalmazások közé tartoznak
- Rákkezelések: A Hela sejtek döntő szerepet játszottak a rákgyógyszerek, például a kamptotekin, a petefészek-, tüdő- és méhnyakrák kezelésére szolgáló, az FDA által jóváhagyott gyógyszer létrehozásában.
- Contergan és myeloma multiplex: A HeLa sejteket arra használták, hogy bemutassák, hogy a thalidomid gyógyszer, amelyet eredetileg a reggeli rosszullétek kezelésére használtak, hogyan okozhat veleszületett fogyatékosságokat, ami a myeloma multiplex kezelésében való felhasználásához vezetett.
- A HIV és az AIDS megértése: Az a felfedezés, hogy a HIV nehezen fertőzte meg a HeLa-sejteket, javította a kutatók megértését a vírusról, és megnyitotta az utat a HIV- és AIDS-gyógyszerek kifejlesztése előtt.
- A sejtek öregedése: A HeLa sejtek lehetővé tették a kutatók számára az öregedés biológiájának és a korai öregedést okozó betegségek feltárását, ami a regenerálható kromoszómák felfedezéséhez vezetett, amelyek megakadályozzák a sejtek idővel történő degenerációját és károsodását.
- Vérbetegségek: A HeLa sejteket a hidroxikarbamid hatékonyságának értékelésére használták különböző rosszindulatú vérbetegségek és vérszegénység ellen; a hidroxikarbamidot ma már sarlósejtes betegség és fehérvérsejtes rosszindulatú betegségek kezelésére használják.
- Röntgensugarak: 1956-ban a tudósok HeLa-sejteket használtak a röntgensugárzás élő szervezetekre gyakorolt hatásainak vizsgálatára, így jobban megértették az orvosi röntgensugárzásból származó nagy és ismétlődő sugárdózisok veszélyeit.
- Innovatív felfedezések: A HeLa-sejtek döntő szerepet játszottak számos jelentős biológiai felfedezésben, amelyek a rákgyógyszerek, a HIV/AIDS ismerete és sok más területen elért eredményekhez vezettek.
- A sejtek öregedése: A HeLa-sejteket alkalmazó kutatók Nobel-díjat kaptak a sejtek öregedésével és a sejtek idővel történő degenerációjának és károsodásának megelőzésével kapcsolatos felfedezéseikért.
A HeLa sejtek és származékaik vizsgálata
Mik a potenciálisan immortalizált sejtek?
Az immortalizált sejtvonalak olyan sejtek, amelyeket úgy módosítottak, hogy folyamatosan osztódjanak, és hosszú időn keresztül termeszthetők legyenek. Kromoszóma-rendellenességekkel vagy mutációkkal rendelkező forrásokból származnak, és származhatnak daganatokból is. A növekedés folytatásához a tudósok a sejtek egy részét új sejtkultúra-edényekbe osztják, és további kísérletekhez szaporítják őket.
A HeLa sejtek, más sejtvonalakhoz hasonlóan, "halhatatlanoknak" számítanak, mivel a sejttenyésztő lombikokban a végtelenségig képesek osztódni, amíg a sejtek túléléséhez szükséges elsődleges feltételeket fenntartják (azaz megfelelő környezetben támogatják és gondozzák őket). A HeLa sejteknek számos törzse létezik, mert a sejtkultúrákban folyamatosan mutálódnak, de mind ugyanabból a Lacks-tumorsejtből származnak. A sejtkultúrákban szaporított HeLa-sejtek száma messze meghaladja a Henrietta Lacks szervezetében találtakét.
HeLa sejtek előállítása, minőségellenőrzés és eltarthatósági idő
A HeLa sejtek tenyésztése és betakarítása a szokásos sejttenyésztési módszerekkel 80-90% körüli konfluenciában történhet. A sejtek viszonylag egyszerűen manipulálhatók, és különböző körülmények között tenyészthetők.
Hogyan olvasztjuk ki a fagyasztott HeLa sejteket
- Tegye a kriovialitást egy antibakteriális 37°C-os vízfürdőbe tiszta vízzel.
- Gyorsan olvassza fel 40-60 másodpercig. Az üvegcsét ki kell venni és steril áramlási szekrénybe kell helyezni.
- Törölje át az üvegcsét 70%-os alkohollal, és a sejtszuszpenziót helyezze át egy 15 ml-es centrifugacsőbe, amely 8 ml táptalajt tartalmaz.
- Állítsuk helyre a sejteket, centrifugáljuk 300 x g-n három percig, és dobjuk el a felülúszót (alternatívaként hígítsuk fel a táptalajjal, és 24 órával később távolítsuk el a fagyasztó táptalajt, ha nem centrifugáljuk azonnal).
- A 10 ml új táptalajban szuszpendált sejteket helyezzük át két T25-ös sejttenyésztő lombikba.
HeLa sejtek szubkultiválása
- Távolítsa el a régi tápfolyadékot a sejttenyésztő lombikból.
- Öblítse le a megtapadt sejteket kalcium- és magnéziummentes PBS-szel. Használjon 3-5 ml PBS-t a T25-ös és 5-10 ml-t a T75-ös sejttenyésztő lombikokhoz.
- Adjunk Accutase-t a sejttenyésztő lombikba. Használjon 1-2 ml-t T25-ös és 2,5 ml-t T75-ös sejttenyésztő lombikban. Győződjön meg róla, hogy a sejtlap teljesen be van fedve.
- Inkubálja a sejttenyésztő lombikot környezeti hőmérsékleten 8-10 percig.
- Óvatosan reszuszpendálja a sejteket a tápfolyadékkal. Adjunk hozzá 10 ml tápfolyadékot, és óvatosan pipettázzuk fel és le a sejtaggregátumok felbontásához.
- Centrifugáljuk a sejtszuszpenziót 3 percig 300 x g-nél.
- Reszuszpendáljuk a sejteket friss tápfolyadékban.
- A reszuszpendált sejteket adagoljuk új sejttenyésztő lombikokba, amelyek friss tápfolyadékot tartalmaznak.
- Hosszú távú tárolás céljából tárolja a sejteket folyékony nitrogénben.
Ha ezeket a lépéseket követi, a sejteket szubkultúrázhatja, és egészséges sejtkultúrát tarthat fenn a későbbi kísérletekhez.