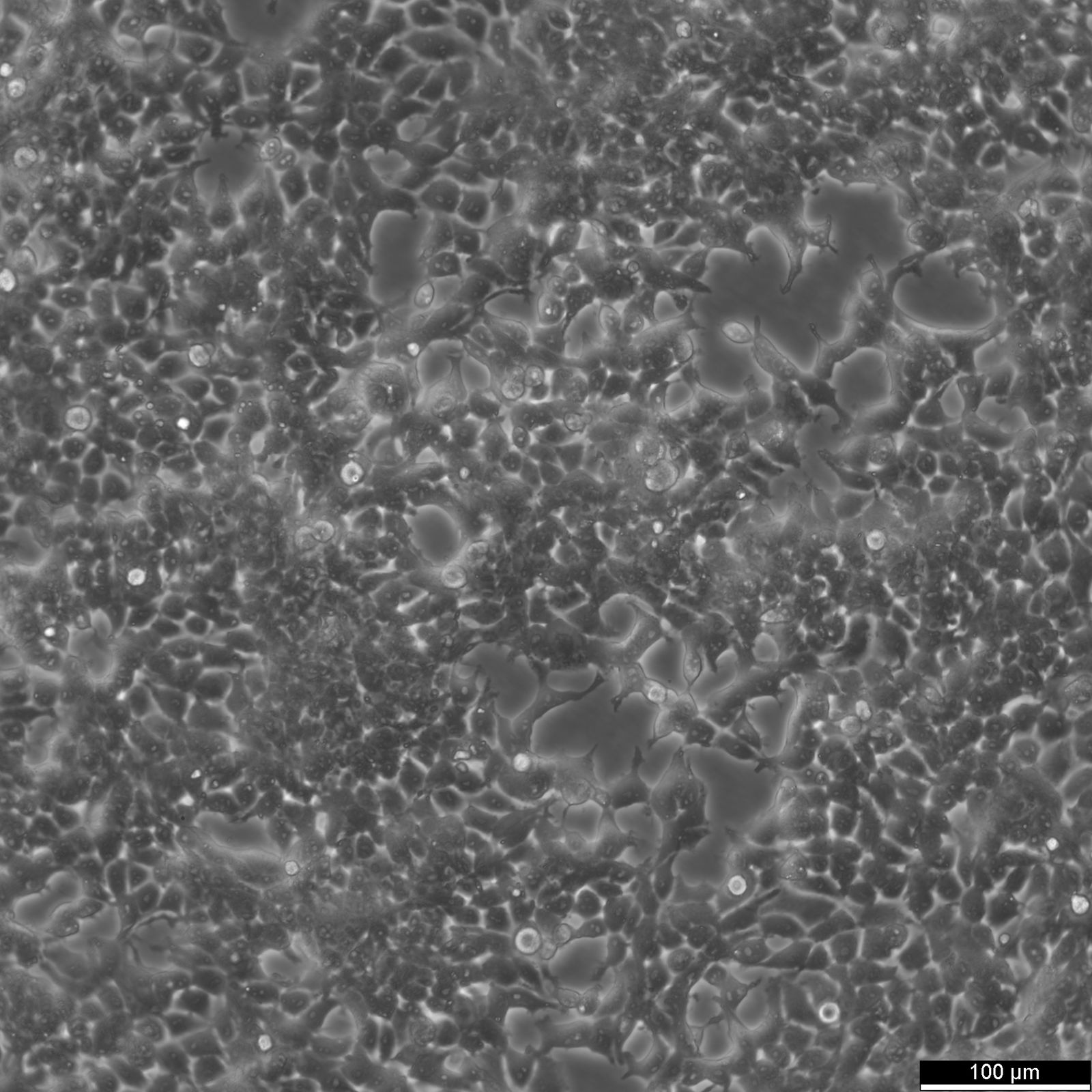
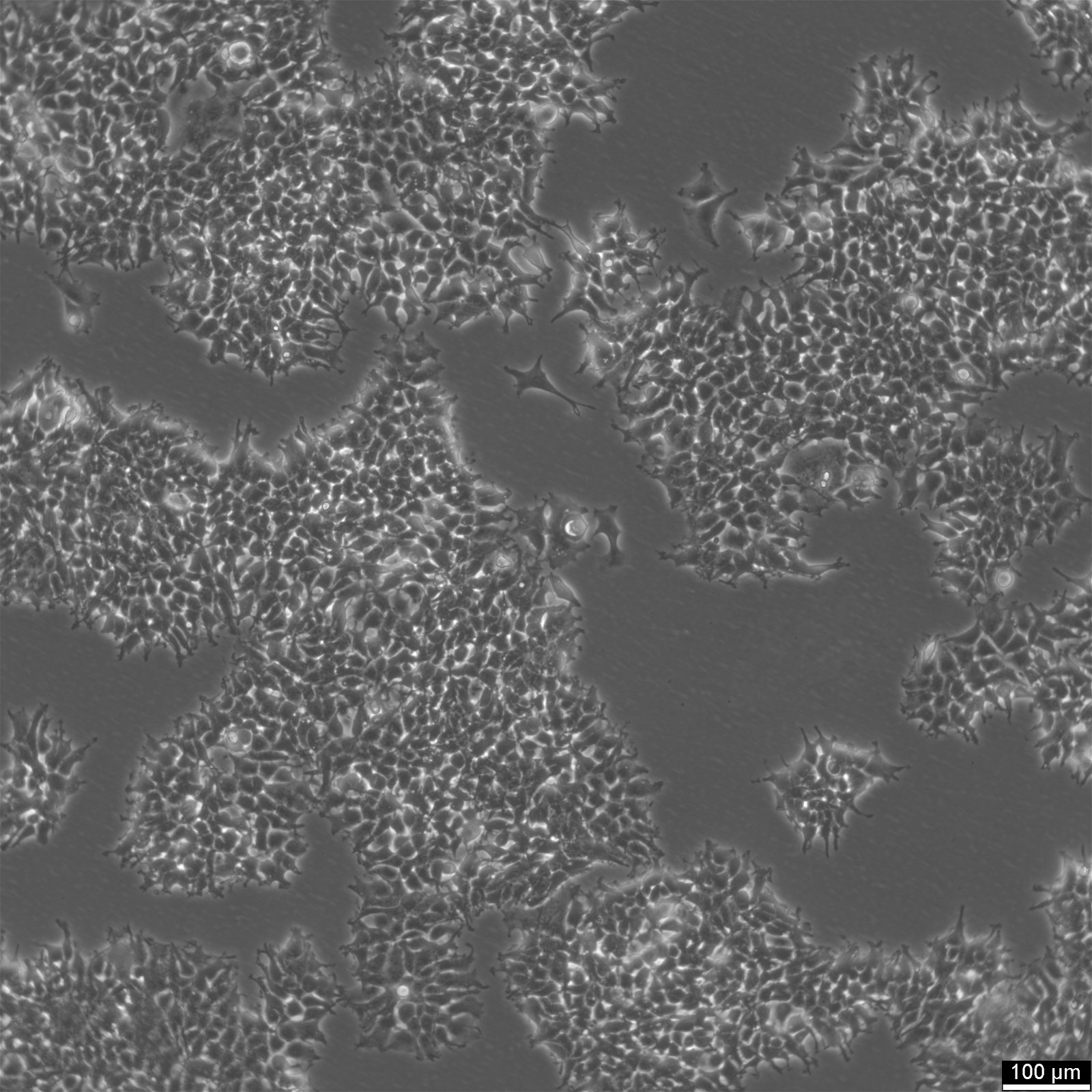
HEK293T sejtek: A transzfekciós vizsgálatokban rejlő lehetőségek felszabadítása
AHEK293T sejtek az ipari biotechnológiában, a toxikológiában és a rákkutatásban széles körben alkalmazott humán embrionális vesesejtek. Ezeket az immortalizált sejteket különböző terápiás fehérjék és vírusok előállítására is használják.
A HEK293T sejtek általános jellemzői és eredete
Ez a cikkrész a HEK293T sejtvonal eredetével és általános információival foglalkozik.
- A HEK293T sejtvonal laboratóriumban tenyésztett primer emberi embrionális vesesejtekből származik. A kutatók az 1970-es évek elején fejlesztették ki ezeket a sejteket úgy, hogy az embrionális vesesejteket nyírt 5. típusú adenovírus DNS-töredékekkel transzfektálták. A kutatók a HEK293T sejtvonalat a 40-es simian vírus (SV40) nagy T-antigénjének a HEK293 sejtek genomjába történő bevitelével hozták létre. Ez a módosítás lehetővé tette a kutatók számára, hogy a 293 sejteket könnyen transzfektálják, és alkalmassá tette őket fehérje előállítására és génexpressziós vizsgálatokra [1].
- A HEK293T sejtek epithelszerű morfológiával rendelkeznek. Hosszúkás és lapított alakot képviselnek, határozott sejthatárral.
- A HEK293T sejtek mérete 11 és 15 µm közötti átmérőjű.
- Az SV40 large-t antigénnel rendelkező HEK293T sejtek komplex kariotípussal rendelkeznek. Ezek a sejtek hipotriploidok, 3-szor kevesebb kromoszómát tartalmaznak, mint egy haploid ivarsejt, és 64-es modális kromoszómaszámmal rendelkeznek.
Mi a különbség a HEK293T és a HEK293 között?
Mind a HEK293, mind a HEK293T sejtvonalak emberi eredetűek. A HEK293T a HEK293 sejtvonal népszerű származéka. A tudósok ezeket a sejteket az eredeti humán embrionális vese 293 sejtekből fejlesztették ki SV40 nagy T antigénnel történő transzfektálással, míg az immortalizált HEK293 sejteket humán embrionális vesesejtek transzformálásával és tenyésztésével hozták létre nyírt humán adenovírus 5 DNS-töredékekkel.
Sejttechnológiák és a HEK293T sejtek orvosbiológiai alkalmazásai
Sejtkultúra és sejtbankolás a HEK293T kutatásban
A HEK293T sejtek, amelyek a humán embrionális vese 293-as sejtjeiből származnak, robusztus növekedésük és könnyű transzfekciójuk miatt széles körben használatosak a sejtkultúrában. Ahhoz, hogy ezekkel a sejtekkel dolgozhassanak, a kutatóknak prioritást kell adniuk a sejtbankolásnak, ami a sejtek tárolását jelenti a hosszabb kutatási és terápiás felhasználás céljából. A sejtek tulajdonságainak megőrzése és a sejtek hosszú távú életképességének biztosítása érdekében fokozatos sejtbanki megközelítést kell alkalmazniuk. A sejtbankok létrehozása megköveteli a helyes gyártási gyakorlatra vonatkozó előírások betartását a sejtek életképességének és integritásának biztosítása érdekében a terápiás alkalmazásokhoz.
A helyes gyártási gyakorlatok döntő fontosságúak a HEK293T sejtbankok előállítása során, amelyek mind a kutatási, mind a terápiás alkalmazások alapját képezik. A mester sejtbank referenciapontként szolgál minden későbbi sejttermékhez. Ezeknek a sejteknek a terápiás alkalmazásokhoz, például a génterápiákhoz szükséges lentivirális előállítása szigorú szabályozási előírásokat követ a végtermékek biztonságosságának és hatékonyságának biztosítása érdekében.
HEK293T-t használó protokollok és vizsgálatok
A citotechnológiában a HEK293T sejtek tulajdonságainak értékelésére speciális protokollokat és vizsgálatokat terveznek. Ezek közé tartozik a génterápiás vektorok hatékonyságának és a sejtek extracelluláris mátrixszal való kölcsönhatásának értékelése tányérban vagy szuszpenziós kultúrában. A HEK293T sejtek integritásának megőrzése érdekében a kutatók precízen választják ki a transzfekcióhoz szükséges reagenseket, és a nyersanyagokat szigorú minőségellenőrzési teszteknek vetik alá.
A HEK293T sejtvonal kutatási alkalmazásai
- Oltóanyag-fejlesztés: A HEK293T sejtvonalat vírusok tanulmányozására és vírusvektor-alapú vakcinák előállítására használták a különböző vírusfertőzések elleni küzdelem érdekében. Egy tanulmány ezt az embrionális vesesejtvonalat használta a COVID-19 vírus humán angiotenzin-konvertáló enzim 2 (ACE2) révén történő sejtbe jutásának strukturális és funkcionális alapjainak vizsgálatára [3]. Emellett egy nemrégiben végzett tanulmány HEK93T sejteket használt SARS-CoV-2 tüskés áltipizált lentivírus részecskék előállítására [4].
- Toxikológiai kutatás: Ezt a humán embrionális vesesejtvonalat széles körben használják gyógyszerek toxicitásának és hatékonyságának vizsgálatára. A 2022-ben végzett kutatás a HEK293T-t, mint normális emberi sejtvonalat használta a Caladium lindenii kivonatok citotoxikus potenciáljának validálására a HepG2 májrákos sejtvonallal szemben [5].
- Génexpressziós vizsgálatok: Az SV40 nagy T antigénnel rendelkező HEK293T sejtvonal jól transzfektálható, így alkalmas génexpressziós vizsgálatokra. Egy vizsgálatban HEK293T sejteket használtak a hosszú nem kódoló RNS SNHG16 szerepének vizsgálatára a trofoblasztok funkcióinak szabályozásában. A vizsgálat kimutatta, hogy az LncRNS SNHG16 kölcsönhatásba lép a miR-218-5p/LASP1 tengellyel, hogy közvetítse ezeket a hatásokat [6].
Sejtterápiás innovációk HEK293T sejtek felhasználásával
A HEK293T sejtterápiában elért előrelépések
A HEK293T sejtek jelentős mértékben hozzájárulnak a sejtterápiához, különösen a génterápiához használt vírusvektorok előállításához. Ezek a sejtek nélkülözhetetlenek a helyes gyártási gyakorlat előírásait betartó gyártási folyamatokban, mivel biztosítják a kiváló minőségű génterápiás termékek előállítását. A gyártó személyzet képzése is a HEK293T sejtek egyedi tulajdonságainak kezelésére és az ezekből a sejtekből származó gyógyszerek magas színvonalának fenntartására összpontosít.
HEK293T sejtek a klinikai vizsgálatokban és a génterápiában
A HEK293T sejtvonal kulcsfontosságú szerepet játszik a génterápiás termékek fejlesztésében, és szerves részét képezi az új sejtterápiák piacra dobását célzó klinikai vizsgálatoknak. Ez magában foglalja a sejtvonal nagy transzfektivitásának kihasználását a génszállításhoz, olyan vektorok felhasználásával, mint például a lentivirális csomagolóvektorok, ahol az integráz D64V mutáció figyelemre méltó előrelépés volt a biztonság növelése érdekében.
Innovatív technikák a HEK293T sejttenyésztésben
A HEK293T sejtek sokoldalúsága támogatja az innovatív technikákat mind a kétdimenziós, mind az összetettebb dimenziós sejtkultúrákban. Ez az alkalmazkodóképesség kulcsfontosságú a különböző típusú orvosbiológiai kutatásokhoz szükséges sejttermékek feltárásában, beleértve a rákkutatást, ahol ezeket a sejteket tumorogén folyamatok és gyógyszertesztek tanulmányozására használják. Emellett a HEK293T vonal fontos szerepet játszik a lentivirális részecskék előállításában, amelyek mind a kutatási, mind a terápiás vektorok gyártási folyamataihoz elengedhetetlenek.
HEK293 sejtek vásárlása az Ön kutatásához
Emelje kutatásainak színvonalát HEK293 sejtjeinkkel, amelyek a génexpressziós vizsgálatokban és vakcinagyártásban való alkalmazkodóképességükről híresek. Kínálatunkban olyan sokoldalú származékok szerepelnek, mint a HEK293T, a HEK293 szuszpenzióval adaptált vonal, a HEK293T/17, az AAV-293 és a 2V6.11. Fedezze fel széleskörű választékunkat, hogy támogassa és előmozdítsa kísérleti munkáját.
A HEK293T sejtvonal tenyésztési információi
A HEK293T sejteket széles körben tenyésztik a kutatólaboratóriumokban. A HEK293T sejttenyészet fejlesztése előtt tudnia kell: Mennyi a HEK293T sejtek megduplázódási ideje? Milyen a HEK293T médium? Mi a HEK293T sejtek vetési sűrűsége?
A HEK293T sejtek tenyésztésének legfontosabb pontjai
|
Megduplázódási idő: |
A HEK293T sejtek esetében megadott megduplázódási idő 30 óra. |
|
Adhezív vagy szuszpenzióban: |
A HEK293T egy adherens sejtvonal. |
|
Ültetési sűrűség: |
A HEK293T sejteket 1 x104 sejt/cm2 sűrűséggel vetik. Ezzel a vetési sűrűséggel a sejtek körülbelül 4 nap alatt képesek konfluens monoréteget képezni. A beültetéshez az adherens sejteket az accutáz disszociációs oldat segítségével választjuk le. A levált sejteket centrifugáljuk, majd óvatosan reszuszpendáljuk a növekedési tápfolyadékot használva. Ezt követően a sejteket új lombikokba adagoljuk a tenyésztéshez. |
|
Növesztőközeg: |
A HEK293T sejteket EMEM-ben (Eagle's minimal essential medium) tenyésztjük, amely 1,0 g/L L-glükózt, 2,2 g/L NaHCO3-t, 2,0 mM L-glutamint és 10% magzati szarvasmarha szérumot tartalmaz. A táptalajt hetente kétszer kell cserélni. |
|
Növekedési feltételek: |
A HEK293T sejtkultúrákat 37 °C-os, párásított inkubátorban tartjuk, 5%-os CO2-ellátás mellett. |
|
Tárolás: |
A humán embrionális vese HEK293T sejteket hosszabb ideig folyékony nitrogén gőzfázisában vagy -150°C alatti hőmérsékleten tárolják. |
|
Fagyasztási folyamat és közeg: |
A HEK293 sejtek CM-1 vagy CM-ACF fagyasztási közegben fagyaszthatók. A HEK293T sejtek életképességének védelme érdekében lassú, fokozatos 1°C-os hőmérsékletcsökkenést lehetővé tevő fagyasztási folyamatok javasoltak. |
|
Felolvasztási folyamat: |
A fagyasztott sejtek üvegét vízfürdőben (37°C) gyorsan kevergetjük, amíg egy kis jégcsomó nem marad. A sejteket újra szuszpendáljuk a közegben és centrifugáljuk a fagyasztási közeg összetevőinek eltávolítása érdekében. A visszanyert sejteket ezután új lombikokban tenyésztik, amelyekben növekedési tápfolyadékot tartalmaznak. |
|
Biológiai biztonsági szint: |
A HEK293T sejtkultúrák kezeléséhez és fenntartásához 1. biológiai biztonsági szintű laboratórium szükséges. |
HEK293T sejtvonal: HEKT Hektar: Előnyök és korlátok
A 293T humán embrionális vesesejtekhez az előnyök és korlátok egyedülálló kombinációja társul. Az alábbiakban áttekintjük e sejtvonal néhány fő előnyét és hátrányát.
A HEK293T sejtek előnyei és hátrányai
A HEK293T sejtek jelentős előnyei közé tartozik a magas transzfektivitásuk, ahol a sejtvonal figyelemre méltó hatékonyságot mutat az idegen DNS felvételében és a bőséges fehérjék előállításában. Ez a tulajdonságuk miatt széles körben kedveltek mind tranziens, mind stabil transzfekciós vizsgálatokhoz. Emellett a HEK293T sejttenyészetek ismertek könnyű fenntarthatóságukról, így robusztusságuk és egyszerű kezelési követelményeik miatt kiváló választás különböző laboratóriumi kísérletekhez.
A HEK293T sejtkultúráknak azonban vannak korlátai. Az egyik elsődleges probléma a mikrobiális szennyeződés kockázata, amely jelentősen befolyásolhatja a sejtek morfológiáját, génexpresszióját és más kritikus jellemzőket, ami esetleg pontatlan kísérleti eredményekhez vezethet. Továbbá, bár a HEK293T sejtek alkalmasak hosszú távú kísérletek elvégzésére, a hosszabb tenyésztési időszakok veszélyeztethetik a sejtek egészségét. Ez befolyásolhatja a transzfekciós hatékonyságukat és a növekedési rátájukat, ezért a sejtek integritásának megőrzése érdekében általában ajánlott a passzázsszámot 20-ra vagy az alá korlátozni.
Gyakran ismételt kérdések a HEK293T sejtkultúráról és alkalmazásokról
HEK293T sejtek: HEKTAN: Kutatási publikációk
Ebben a szakaszban megemlítünk néhány ígéretes kutatási publikációt, amelyekben HEK293T sejtek szerepelnek.
Ez a publikáció 2022-ben jelenik meg a BioRxiv folyóiratban. Ebben a tanulmányban HEK293T sejteket használtak COVID-19 vírus mRNS-vakcinák kifejlesztésére, amelyek a spike gén N-terminális és RBD (receptorkötő domén) doménjeit kódolják.
A cirkuláris HER2 RNS pozitív hármas negatív emlőrák érzékeny a Pertuzumabra
Ez a kutatás a Molecular Cancer 2020 című folyóiratban jelent meg. A tanulmány azt javasolta, hogy a körkörös HER2 RNS-expresszió a hármas negatív emlőráksejtekben érzékennyé teszi a Pertuzumab gyógyszeres kezelésre. A kutatók HEK293 sejteket használtak a lentivírus előállításához és a cirkuláris HER2 gén transzfekciójához ebben a tanulmányban.
Az IFITM3 vírusellenes szerepe a prototípusos habos vírusfertőzésben
Ez a tanulmány a Virology Journal 2022-es számában jelent meg. Ebben a tanulmányban HEK293T sejteket használtak az IFITM3 (interferon-indukált transzmembránfehérje 3) antivirális hatásának vizsgálatára prototípus foamy vírus (PFV) fertőzésben.
A Nature Scientific Reports (2017) című szaklapban megjelent kutatási közlemény HEK293T sejteket használt, és azt vizsgálta, hogy a miRNS-21 a PI3K/AKT jelátviteli útvonal, valamint a SMAD7 és PTEN gének expressziójának szabályozásán keresztül közvetíti a metformin által kiváltott antiangiogén hatást.
A mikroRNS-608 gátolja a hólyagrák proliferációját az AKT/FOXO3a jelátviteli útvonalon keresztül
Ez a kutatás a Molecular Cancer folyóiratban jelent meg 2017-ben. Ebben a tanulmányban HEK293 sejteket használtak a miRNS-608 hólyagrák elleni antiproliferatív potenciáljának vizsgálatára.
HEK293T sejtvonalra vonatkozó források: Protocols, Videos, and More
Az alábbiakban néhány forrás található a HEK293T sejtekkel kapcsolatban:
- HEK293T sejtek transzfektálása.
- HEK sejtek transzfekciója: Ez a videó a HEK293 humán embrionális vese sejtvonal általános transzfekciós protokollját mutatja be.
- Sejtek passziválása: Ez a videó az adherens sejtek osztásának vagy szubkultiválásának eljárását ismerteti.
Sejttenyésztési protokollok
A HEK293T sejtek sejttenyésztési protokolljai itt találhatók.
- HEK293T sejtek osztása: Ez az oldal részletes, lépésről lépésre történő útmutatót nyújt a HEK293 sejtek szubkultúrázásához.
- Humán embrionális vesesejtek tenyésztése: Ezen a linken a HEK293T sejttenyésztési protokollt találja.
Hivatkozások
- Tan, E., et al., HEK293 sejtvonal mint rekombináns fehérjék és vírusvektorok előállításának platformja. Frontiers in Bioengineering and Biotechnology, 2021, 9.
- Kim, M.J., et al., Az AMPKα1 szabályozza a tüdő- és emlőrák progresszióját a TLR4 által közvetített TRAF6-BECN1 jelátviteli tengely szabályozásával. Cancers (Basel), 2020, 12(11).
- Wang, Q., et al., A SARS-CoV-2 belépésének strukturális és funkcionális alapja a humán ACE2 felhasználásával. Cell, 2020. 181(4): p. 894-904.
- Gale, E.C., et al., Hydrogel-alapú lassan felszabaduló receptor-kötő domén alegység vakcina kiváltja a SARS-CoV-2 elleni neutralizáló antitestválaszt. bioRxiv, 2021.
- Kalsoom, A., et al., In Vitro Evaluation of Cytotoxic Potential of Caladium lindenii Extracts on Human Hepatocarcinoma HepG2 and Normal HEK293T Cell Lines. Biomed Res Int, 2022, p. 1279961.
- Yu, Z., et al., LncRNS SNHG16 szabályozza a trofoblaszt funkciókat a miR-218-5p/LASP1 tengelyen keresztül. J Mol Histol, 2021. 52(5): p. 1021-1033.