HCT116 sejtvonal: A vastagbélrák-kutatás egyik pillére
AHCT116 sejtvonal a vastagbélrák kutatásának sarokköve, amely felbecsülhetetlen betekintést nyújt a betegség patogenezisébe és a lehetséges terápiás lehetőségekbe. A rákkutatásban és a farmakológiai vizsgálatokban való hasznosságáról híres HCT116 megkönnyíti a tumor viselkedésének és a gyógyszerek hatékonyságának kulcsfontosságú vizsgálatát.
A HCT116 sejtek eredete és alapvető jellemzői
A HCT116 sejtek gyökereinek és alapvető tulajdonságainak, például morfológiai jellemzőinek, genetikai felépítésének és sejtméreteinek megértése alapvető fontosságú azon kutatók számára, akik e sejtvonalat használó tanulmányokba kezdenek.
Származás és genetikai tájkép: A HCT116 sejtek egy 48 éves kaukázusi férfi vastagbeléből származnak, akinél vastagbélrákot diagnosztizáltak, és a RAS/RAF/MEK/ERK jelátviteli útvonal részét képező KRAS gén 13. kodonjában (G13D) mutációval rendelkeznek. Ez a bizonyos mutáció kulcsfontosságú e sejtek onkogén átalakulásában, ami kiemeli jelentőségüket a rákkutatásban.
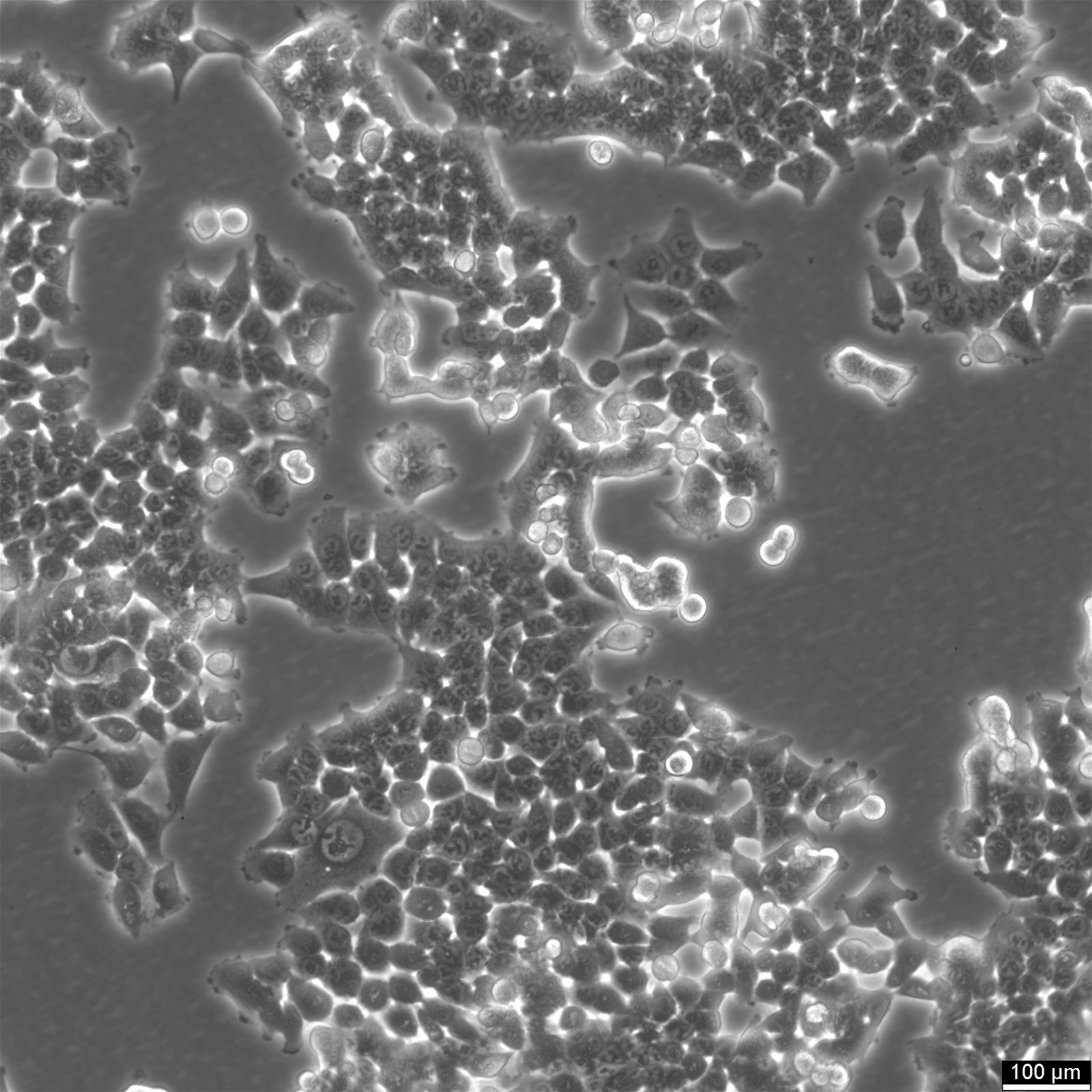
Morfológia és növekedési jellemzők: A HCT116 sejtek epithelszerű morfológiát mutatnak, és jellemzően monoréteges kultúrákban növekednek, de 150-400 µm átmérőjű szferoidokat is képezhetnek. A növekedési mintázat ezen alkalmazkodóképessége hangsúlyozza sokoldalúságukat a különböző kísérleti elrendezésekben.
Kromoszóma profil: A HCT116 sejtek kromoszómális összetétele közel diploid, a sejtpopuláció körülbelül 70%-a 45 kromoszómát tartalmaz. Figyelemre méltó, hogy a 8-as, 10-es, 16-os és 17-es kromoszómák hosszú karjain visszatérő amplifikáció található, míg az Y kromoszóma hiányzik, ami hozzájárul egyedi genomikai jellegzetességükhöz.
Összehasonlító elemzés: HCT116 vs. HT29 sejtvonalak
A HCT116 és a HT29, egy másik humán kolorektális karcinóma sejtvonal egymás mellé helyezésekor egyértelmű különbségek mutatkoznak onkogén potenciáljuk és differenciálódási képességük tekintetében:
Onkogén agresszivitás és differenciálódás: A HCT116 sejteket magas onkogén agresszivitás és korlátozott differenciálódási potenciál jellemzi, ami az agresszív tumorfenotípusok tanulmányozásának modelljévé teszi őket. Ezzel szemben a HT29 sejtek képesek enterocita-szerű és mucintermelő vonalba differenciálódni, így olyan kontrasztos modellt biztosítanak, amely a vastagbélrák biológiájának különböző aspektusait utánozza.
A HCT116 és a HT29 sejtvonalak összehasonlító megértése gazdagítja a kutatók rendelkezésére álló eszköztárat, lehetővé téve a vastagbélrák sokrétű természetének árnyaltabb vizsgálatát.
HCT116 sejtek kezelése
|
Megduplázódási idő: |
A HCT116 rákos sejtek megduplázódási ideje 25 és 35 óra között van. |
|
Adhezív vagy szuszpenzióban: |
A HCT116 vastagbélrákos sejtvonal adherens, a sejtek monoszlopokban növekednek. |
|
Ültetési sűrűség: |
A HCT116 sejtkultúrához 2 x104 sejt/cm2 vetési sűrűség ajánlott. A szubkultúrázáshoz a sejteket 1x PBS mosás után Accutase oldattal kell leválasztani. A centrifugálást követően a sejtpelletet friss tápfolyadékban reszuszpendáljuk, és új lombikba helyezzük át. |
|
Növesztőközeg: |
A HCT116 sejtek tenyésztéséhez a 3,0 g/L L-glükózzal, 1,5 mM L-glutaminnal, 3,0 g/L NaHCO3-mal és 10% magzati szarvasmarha szérummal kiegészített McCoys 5a táptalaj optimális. A táptalajt hetente 1-2 alkalommal célszerű megújítani. |
|
Növekedési feltételek (hőmérséklet,CO2): |
A tenyésztés 37 °C-os, párásított inkubátorban történik, 5%-osCO2 légkörben. |
|
Tárolás: |
A HCT116 sejtek -150°C alatti hőmérsékleten tárolhatók folyékony nitrogén gőz- vagy folyadékfázisában. |
|
Fagyasztási folyamat és közeg: |
A kriokonzerváláshoz CM-1 vagy CM-ACF közeget használjunk. A fagyasztás szabályozott sebességű, percenként 1°C-os fokozatos hőmérsékletcsökkenést lehetővé tevő, a sejtek életképességének megőrzését elősegítő fagyasztási módszer ajánlott. |
|
Felolvasztási folyamat: |
A HCT116 sejteket 37 °C-os vízfürdőben olvasztjuk fel. Növesztőközeg hozzáadása után centrifugálással távolítsa el a fagyasztóközeg maradványait. Reszuszpendálja a sejtpelletet friss tápfolyadékban, és új lombikokban tenyészti. |
|
Biológiai biztonsági szint: |
Szint |
A HCT116 sejtvonal előnyei
Ez a szakasz a HCT116 sejtvonallal foglalkozik, kiemelve a rákkutatásban, különösen a vastagbélrák vizsgálatában betöltött központi szerepét, és megvitatja a benne rejlő előnyöket.
A HCT116 sejtvonal számos kulcsfontosságú előnye miatt kiemelkedik a rákkutatásban:
Vastagbélrák modell: Széles körben elismert in vitro modellként szolgál a vastagbélrák, a harmadik leggyakoribb rákos megbetegedés világszerte. A humán vastagbélrák utánzásának fontossága miatt felbecsülhetetlen értékű a rák biológiájának megértéséhez és a terápiás stratégiák teszteléséhez.
Homogenitás: Figyelemre méltó, hogy a HCT116 sejtek mintegy 70%-a egységes genetikai profilt mutat, ami viszonylag homogén populációt jelent. Ez az egységesség kulcsfontosságú a génexpresszióra, a sejtek jelátviteli útvonalaira és a gyógyszeres kezelések hatékonyságának értékelésére összpontosító vizsgálatokhoz, mivel biztosítja a kísérleti eredmények következetességét és megbízhatóságát.
Transzfekciós hatékonyság: A HCT116 sejtek egyik megkülönböztető jellemzője, hogy jól transzfektálhatók, különösen vírusvektorokkal. Ez a tulajdonság különösen előnyös a génterápiás kutatásokban, mivel lehetővé teszi a genetikai anyag hatékony és precíz bevitelét, megkönnyítve ezzel a fejlett genetikai manipulációkat és funkcionális vizsgálatokat.
Fejlessze felfedezéseit hitelesített HCT116 sejtvonalunkkal
A HCT116 sejtvonal kutatási alkalmazásai
A HCT116 sejtvonal a rákkutatásban széles körben alkalmazható. Néhány kiemelkedő alkalmazás:
Rákbiológia
A HCT116 vastagbélrák-sejtvonalat a vastagbélrák progressziójának és fejlődésének tanulmányozására használják. Ezenkívül segít megvilágítani a rák proliferációjában, migrációjában és inváziójában szerepet játszó mögöttes mechanizmusokat és jelátviteli útvonalakat. Egy tanulmány a HCT116 sejteket a gyógyszerrezisztencia kialakulásában szerepet játszó gének tanulmányozására használta. A kutatók az MDR1 gént túlexpresszálták a vastagbélráksejtekben, és megfigyelték a NOX (NADPH-oxid) izoformák és az Nrf2 expresszióját. A vizsgálat kimutatta, hogy a NOX2 és az Nrf2 felszabályozása kemorezisztenciát okoz a rákos sejtekben; így ezek a gének célzottan megcélozhatók a rákterápia során kialakuló rezisztencia leküzdésére [1]. Hasonlóképpen, egy 2021-ben végzett kutatás arról számolt be, hogy az NF-κB jelátviteli útvonal részt vesz a vastagbélrák proliferációjának és migrációjának szabályozásában. Így célzottan megcélozható a vastagbélrák elleni új és hatékony terápiák kifejlesztésére [2].
Az onkológia területén alapvető fontosságú a sejtciklus, a proliferáció és növekedés, valamint az apoptózis bonyolult folyamatainak megértése. Ezek a biológiai funkciók kulcsfontosságúak a humán sejtvonalak tanulmányozásában, különösen a rosszindulatú sejtekből, például humán vastagbélráksejtekből és hasnyálmirigyrák modellekből származó sejtvonalakban. A HCT116 és SW620 sejtvonalak például fontos szerepet játszanak a vastagbélrák, illetve a hasnyálmirigyrák hátterében álló mechanizmusok feltárásában. Az olyan technikák segítségével, mint az áramlási citometria és a klonogén vizsgálatok, a kutatók megismerhetik a génexpressziós profilokat és a tumorokon belül a független sejtek viselkedését, így fényt deríthetnek arra, hogy a rák hogyan kommunikál az extracelluláris mátrixon belül.
Az apoptózis szerepe a rák progressziójában
Az apoptózis, vagyis a programozott sejthalál kritikus szerepet játszik a sejtek homeosztázisának fenntartásában, és a rákkutatás egyik kulcsfontosságú területe. A nem kapcsolódó apoptózis és a kifejezetten a rák kontextusában indukált apoptózis, például a vastagbélrákos sejthalál közötti különbségtétel döntő fontosságú. Ez a folyamat nem csupán a sejtek eltávolításáról szól, hanem olyan jelek összetett kölcsönhatását foglalja magában, amelyek befolyásolhatják a tumor növekedését és az áttétképzést. Az apoptózis és a sejthalál metasztázis-szupresszorokkal és tumorszupresszor aktivitással együtt történő vizsgálatával a tudósok betekintést nyerhetnek a rák progresszióját és metasztatikus potenciálját szabályozó útvonalakba.
Metasztázis és molekuláris markerek a rákban
A metasztázis továbbra is a rák egyik legfélelmetesebb aspektusa, a rosszindulatú sejtek terjedésében a hematogén metasztázis jelentős gondot jelent. A metasztázis feltárása magában foglalja a rákos sejtek mozgásának és inváziós képességének, vagyis a sejtek lokomóciójának tanulmányozását, valamint azt, hogy a sejtek hogyan lépnek kölcsönhatásba környezetükkel, beleértve az extracelluláris mátrixot is. Az olyan molekuláris markerek, mint a CD133 expressziója és az epidermális növekedési faktor receptora kritikus fontosságúak a pozitív vastagbélrákos sejtek és más ráktípusok viselkedésének azonosításában és megértésében. A SIRT6 útvonal például a daganatos növekedés és a metasztatikus vastagbélrák modulálásában játszott potenciális szerepe miatt került az érdeklődés középpontjába.
Toxikológia/gyógyszerfejlesztés
A HCT116 sejtvonalat új rákgyógyszerek szűrési modelljeként használják. Számos vizsgálatot végeztek a rákellenes gyógyszerek, köztük a természetes termékek és a kémiailag szintetizált nanorészecskék hatékonyságának és toxicitásának felmérésére. Így a kutatás egy növényi drog, a Caesalpinia pulcherrima kivonatából szintetizált ezüst nanorészecskék citotoxicitását értékelte HCT116 sejtekben [3]. Egy tanulmányban a kutatók a HCT116 rákos sejtvonalat használták a kakaótea vizes kivonatának rákellenes potenciáljának értékelésére. Azt találták, hogy a kakaótea kivonat csökkenti a vastagbélrák proliferációját és sejtpusztulást idéz elő [4]. Egy másik tanulmány HCT116 rákos sejteket használt, és felfedezte, hogy a légkrumplit, Dioscorea bulbifera, kivonatok pro-apoptotikus aktivitást mutatnak a vastagbélrákos sejtekben a JNK jelátviteli kaszkád aktiválásán és az ERK1/2 gén szuppresszióján keresztül [5].
A metformin rákos sejtekre gyakorolt hatásai, különösen a vastagbél- és hasnyálmirigyrák összefüggésében, jól példázzák, hogy a rákos sejtek biológiai funkcióinak megértése hogyan vezethet potenciális terápiás stratégiákhoz. A rákos sejtek klonogén túlélésének, vagyis a klónképzésre való képességének kutatása olyan szerekkel való kezelés hatására, mint a metformin, vagy olyan specifikus útvonalak, mint az epidermális növekedési faktor receptor megcélzása, értékes betekintést nyújthat a hatékony rákkezelésekbe. Ezenkívül a HCT116 klónok és HCT116 sejtpopulációk használata ezekben a vizsgálatokban lehetővé teszi annak árnyaltabb megértését, hogy a rákos sejtek hogyan reagálnak a különböző terápiás beavatkozásokra, ami megnyitja az utat a rákkezelés személyre szabottabb megközelítései előtt.
HCT116 sejtek: H116TT: Kutatási publikációk
Ez a szakasz néhány jelentős és legtöbbet idézett, a HCT116 sejtvonalat bemutató közelmúltbeli publikációt tekint át.
Ez a tanulmány a Journal of Photochemistry and Photobiology B: Biology (2017) című folyóiratban jelent meg. A kutatók HCT116 vastagbélrák és A549 tüdőrák sejtvonalakat használtak a piper nigrum magból szintetizált ón-oxid nanorészecskék citotoxikus hatásának értékelésére.
A Cancer Letters (2018) című szaklapban megjelent kutatás azt javasolja, hogy az SNHG15 lncRNS elősegíti a vastagbélráksejtek migrációját vastagbélrák-sejtvonalakban, köztük a HCT116-ban.
A TUG1 hosszú nem kódoló RNS túlterjedése elősegíti a vastagbélrák progresszióját
Ez a cikk a Medical Science Monitor folyóiratban jelent meg 2016-ban. A tanulmány megállapította, hogy az onkogén LncRNS TUG1 elősegíti a HCT116 vastagbélráksejtek proliferációját és migrációját.
A Biochemical Pharmacology folyóiratban (2018) megjelent kutatás azt javasolja, hogy a gyógyszerrezisztencia kialakulása feljebb tornássza a H2S-termelő enzimek szintjét a HCT116 vastagbélráksejtekben.
Az International Journal of Environmental Health Research (2023) című folyóiratban megjelent kutatási cikk azt javasolja, hogy az Inula viscosa L. kivonat a mikroRNS-ek szabályozásán keresztül gyakorol rákellenes hatást a HCT116 vastagbélráksejtekre.
Források a HCT116 sejtekhez
Az alábbiakban néhány forrás található a HCT116 sejtekkel kapcsolatban.
- A HCT116 transzfektálása: Ez a videó lépésről-lépésre bemutatja a HCT116 rákos sejtek transzfektálását.
- HCT116 sejtvonal tenyésztése: Ez a videó a HCT116 vastagbélrákos sejtvonal szubkultúrázási protokollját mutatja be.
- A HCT116 sejtvonal szubkultúrázása: Ez a weboldal sok hasznos információt tartalmaz a HCT116 tenyésztőközeggel kapcsolatban. Ezenkívül a sejtek fagyasztására, felolvasztására és szubkultiválására vonatkozó eljárásokat is tartalmaz.
Gyakran ismételt kérdések a HCT116 sejtekről
hivatkozások
- Waghela, B.N., F.U. Vaidya és C. Pathak: A NOX-2 és Nrf-2 preregulációja elősegíti az 5-fluorouracil rezisztenciát a humán vastagbélrák (HCT-116) sejtekben. Biochemistry (Moscow), 2021, 86, p. 262-274.
- Yang, M., et al., Az asztragalin gátolja a humán vastagbélrák HCT116 sejtek proliferációját és migrációját az NF-κB jelátviteli útvonal szabályozásával. Frontiers in Pharmacology, 2021, 12: p. 639256.
- Deepika, S., C.I. Selvaraj és S.M. Roopan, A Caesalpinia pulcherrima L. swartz bioaktivitásának szűrése és a kivonatból szintetizált ezüst nanorészecskék citotoxicitása a HCT116 sejtvonalon. Materials Science and Engineering, C, 2020, 106, p. 110279.
- Gao, X., et al., A kakaó tea (Camellia ptilophylla) mitokondrium-függő apoptózist indukál a HCT116 sejtekben ROS-termelésen és a PI3K/Akt jelátviteli útvonalon keresztül. Food Research International, 2020, 129, p. 108854.
- Hidayat, A.F.A., et al., Dioscorea bulbifera indukálta apoptózist az ERK 1/2 gátlásán és a JNK jelátviteli útvonalak aktiválásán keresztül HCT116 humán kolorektális karcinóma sejtekben. Biomedicina és farmakoterápia, 2018. 104: p. 806-816.