C2C12 Myoblast sejtek: Úttörő szerepet játszó izombiológiai és regenerációs kutatások
Az izombiológia és -regeneráció területén elismert C2C12 myoblast sejtek nélkülözhetetlen eszközként szolgálnak a vázizomzat kialakulásának, differenciálódásának és molekuláris dinamikájának bonyolultságát kutató kutatók számára. Ez az egérből származó sejtvonal robusztus platformot kínál az izomműködés és -javítás sejtes és genetikai alapjainak feltárásához.
Mielőtt a C2C12-sejtekkel megkezdené az utazást, elengedhetetlen, hogy megismerkedjen eredetükkel, jellemzőikkel és alkalmazásaikkal. Ez az áttekintés alapvető betekintést nyújt a következőkbe:
A C2C12 mioblaszt sejtek alapjainak feltárása
A C2C12 sejtek eredetének és egyedi tulajdonságainak megértése alapvető fontosságú a bennük rejlő kutatási potenciál kihasználásában. Ez a rész a következőkre világít rá:
- A C2C12 sejtek kezdete Yaffe és Saxel 1977-es úttörő munkájára vezethető vissza, akik ezt a sejtvonalat egy 2 hónapos C3H egér combizmából állították elő egy zúzódásos sérülést követően. Ez az eredettörténet rávilágít e sejtek rugalmasságára és regenerációs képességére.
- Kultúrában a C2C12 sejtek figyelemre méltó alkalmazkodóképességet mutatnak, magas szérumtartalmú körülmények között gyarapodnak a proliferációhoz, és alacsony szérumtartalmú körülmények között, szérumpótló tenyésztési rendszerekben átmennek myotube-képződésbe , differenciálódnak, proliferáló myoblastokból érett myotube-okká alakulnak át. Ezt az átmenetet a jelek jól összehangolt hálózata irányítja, az intracelluláris metabolikus eltolódásoktól a membrántranszporterek változásaiig, ami ablakot nyit a sejtek alkalmazkodására és specializációjára.
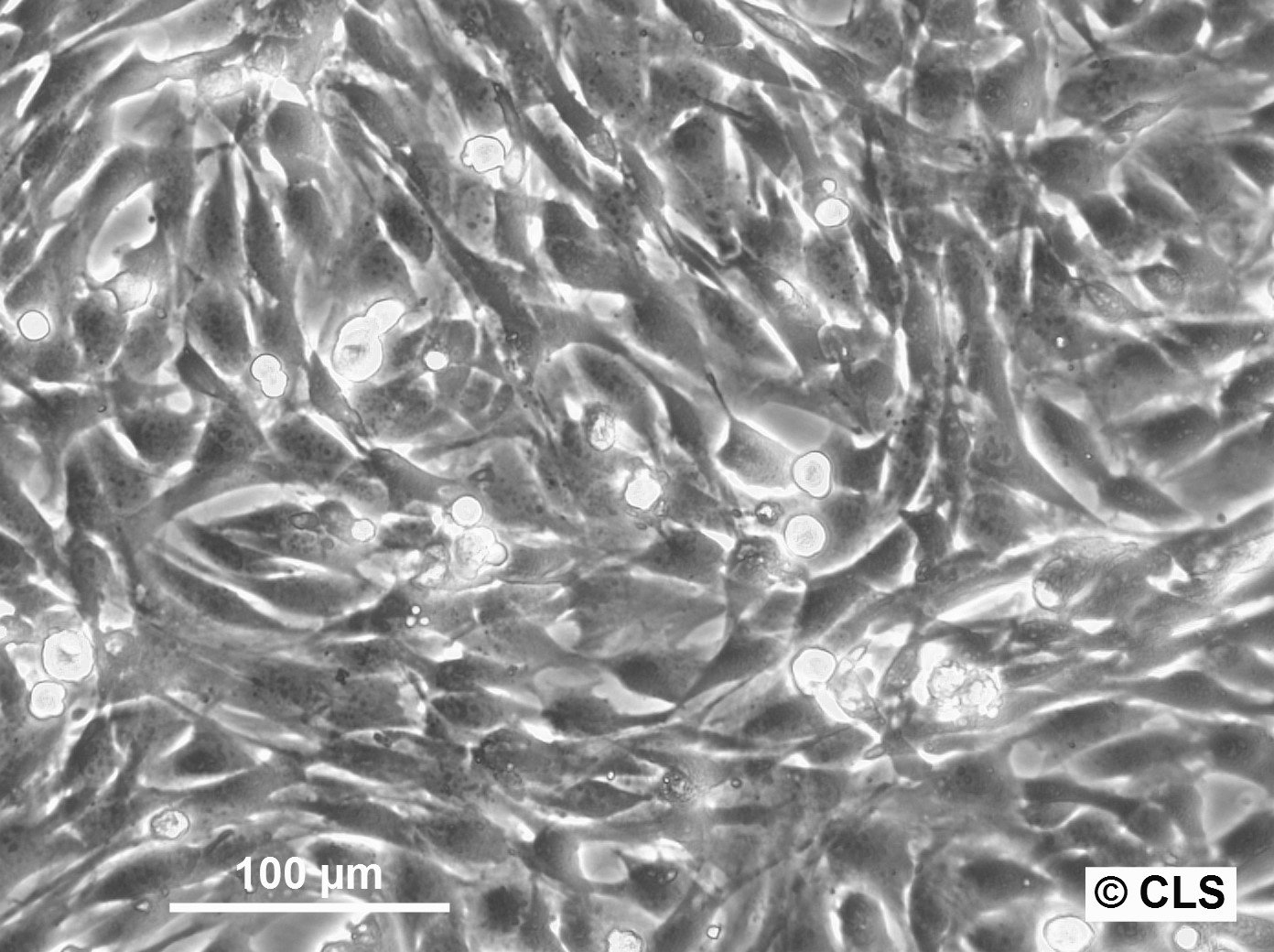
- A C2C12 sejtek jellegzetes, myoblaszt-szerű morfológiája, amelyet sugárirányú elágazás és megnyúlt rostok jellemeznek, dinamikus modellt biztosít az izomsejtek viselkedésének és kölcsönhatásainak tanulmányozásához.
- A diploid kromoszómastátusz fenntartásával a C2C12 sejtek stabil genetikai hátteret biztosítanak a kísérletekhez, így a kutatási eredmények következetessége és megbízhatósága biztosított.
Induljon el a C2C12 mioblaszt sejtekkel folytatott kutatási útra, hogy új dimenziókat tárjon fel az izombiológia és -regeneráció terén, kihasználva a bennük rejlő lehetőségeket az izombetegségek és a terápiás stratégiák jobb megértése érdekében.
A C2C12 sejtek tenyésztésére vonatkozó információk
A C2C12 sejtek, amelyek széles körben elismert szerepet játszanak az izombiológiai kutatásokban, speciális körülményeket igényelnek az optimális növekedéshez és differenciálódáshoz. Az alábbiakban a C2C12 myoblastok tenyésztése során figyelembe veendő legfontosabb szempontokat ismertetjük:
Megduplázódási idő: A C2C12 sejtek megduplázódási ideje általában 12-24 óra, ami jelzi, hogy ideális körülmények között gyorsan szaporodnak.
Sejttípus: Ezek a myoblastok tapadó sejtek, ezért a rögzüléshez és a növekedéshez megfelelő felületre van szükségük.
Ültetési sűrűség: A C2C12 sejtek ideális vetési sűrűsége körülbelül 1 x 10^4 sejt/cm^2. Ennél a sűrűségnél a sejtek általában körülbelül 4 nap alatt érik el a konfluenciát, ezért a sejtek túlnövekedésének megelőzése érdekében elengedhetetlen a sejtkonfluencia ellenőrzése.
Növekedési közeg: A C2C12 sejtek tenyésztéséhez ajánlott táptalaj az RPMI 1640, 10% magzati szarvasmarha szérummal (FBS) és 2,1 mM L-glutaminnal dúsítva. Ez a táptalaj támogatja a sejtek tápanyagszükségletét és elősegíti az egészséges szaporodást.
Növekedési feltételek: A tenyésztés 37°C-on, 5% CO2-vel ellátott, párásított inkubátorban a legjobb, amely a fiziológiás körülményeket utánzó környezetet teremt.
Tárolás: A C2C12 sejteket hosszú távú tartósítás céljából folyékony nitrogén gőzfázisában vagy ultraalacsony hőmérsékletű fagyasztószekrényekben tárolják, -150°C alatti hőmérsékleten tartva.
Fagyasztás és felolvasztás: A CM-1 vagy CM-ACF fagyasztási közeget használva lassú fagyasztási módszer ajánlott a hőmérséklet fokozatos csökkentése és a sejtek életképességének megőrzése érdekében. Felolvasztás után a sejteket óvatosan reszuszpendáljuk friss tápfolyadékban, centrifugáljuk a fagyasztóközeg eltávolítása érdekében, majd új tenyésztőlombikokba helyezzük át.
Biológiai biztonság: A C2C12 sejtek tenyésztéséhez 1. biológiai biztonsági szint szükséges, amely biztosítja a biztonságos kezelési és karbantartási gyakorlatot a laboratóriumban.
E tenyésztési paraméterek betartása biztosítja a C2C12 sejtek egészségét és életképességét, elősegítve a sikeres kísérleteket és kutatási eredményeket az izombiológia területén és azon túl.
C2C12 sejtvonal: Előnyök és korlátok
A vázizomszövetből származó C2C12 egér mioblaszt sejtvonal széles körben elismert az orvosbiológiai kutatások területén az előnyei és korlátai egyedülálló halmaza miatt.
Előnyök
Jól jellemzett: A C2C12 sejteket széles körben tanulmányozták, ami mélyreható ismereteket nyújt fiziológiai és biológiai tulajdonságaikról, például morfológiájukról, differenciálódási potenciáljukról és a különböző ingerekre adott válaszaikról. Ez az alapos jellemzés biztosítja a kutatási eredmények megbízhatóságát és reprodukálhatóságát.
Izomdifferenciálódás: A C2C12 sejtek egyik fő erőssége az a képességük, hogy izomcsövekké differenciálódnak, ami az izomsejtek fejlődését utánozza. Ez teszi őket alapvető eszközzé az izmok biológiájának feltárásához, beleértve az izomsejtek kialakulását, fejlődését és az izomműködés szempontjából kulcsfontosságú kontraktilis fehérjék kifejeződését.
Sokoldalú modell a sejtbiológiához: Jól dokumentált modellként a C2C12 sejtek betekintést nyújtanak számos sejtfolyamatba, beleértve az oxidatív stresszre adott válaszokat, a glükóz anyagcserét, az inzulin jelátvitelt és az inzulinrezisztencia hátterében álló mechanizmusokat. Használatuk megkönnyíti e folyamatok mélyebb megértését mind sejtes, mind molekuláris szinten.
Korlátozások
Fajspecifikus különbségek: Mivel a C2C12 sejtek egérből származó sejtvonalról van szó, nem biztos, hogy tökéletesen reprodukálják az emberi izom biológiáját. Az egerek és az emberek közötti génexpresszió, a sejtanyagcsere és a fiziológiai válaszok közötti különbségek korlátozhatják a kutatási eredmények közvetlen alkalmazhatóságát emberi körülményekre.
Ezek a szempontok rávilágítanak a C2C12 sejtek kritikus szerepére az izomkutatásban, ugyanakkor hangsúlyozzák a korlátok figyelembevételének fontosságát, különösen az adatok emberi biológiára való extrapolálásakor.
Emelje fel kutatásait a C2C12 sejtekkel
A C2C12 sejtvonal kutatási alkalmazásai
Fedezze fel a C2C12 egérsejtvonal változatos kutatási alkalmazásait.
Az izombiológia tanulmányozása: A C2C12 sejtek robusztus in vitro modellként szolgálnak az izombiológiai kutatásokhoz, lehetővé téve az izomfejlődés, az anyagcsere és a differenciálódás vizsgálatát. Ezek a sejtek képesek izomszerű sejtekké differenciálódni, betekintést nyújtva a miotubusok kialakulásába és az izomregenerációs mechanizmusokba. Egy figyelemre méltó tanulmány kiemelte a TGF-β1 és a microRNS-22 szerepét a C2C12 sejtek működésében, hangsúlyozva a sejtek proliferációjára és differenciálódására gyakorolt szabályozó hatásukat.
Gyógyszerszűrés és toxicitásvizsgálat: A C2C12 sejtvonal fontos szerepet játszik az izombetegségek potenciális terápiáinak értékelésében. Platformot kínál az izomsejtek anyagcseréjére és differenciálódására gyakorolt gyógyszerhatások értékeléséhez. Kutatások kimutatták a Cnidoscolus aconitifolius levélkivonat jótékony hatását a C2C12 sejtekre, fokozva a zsírsav-oxidációt és a mitokondriális bioenergetikát, míg a Moringa oleifera levélkivonatról megállapították, hogy megvédi a C2C12 myotubusokat az oxidatív stressztől. A C2c12 sejtek felbecsülhetetlen értékűek az olyan epigenetikai gyógyszerek szűrésében, amelyek hatással lehetnek az izomdifferenciálódásra vagy a myofilamentumfehérje-koncentrációra. Az epigenetikai gyógyszermodell lehetővé teszi a kutatók számára, hogy megfigyeljék a follistatin expresszióját és a smad1 foszforilációját, amelyek kulcsfontosságú tényezők az izom őssejtek érésében és regenerációjában.
- 3D szövetkonstrukciók és vázizom szövetek fejlesztése: A tudósok a c2c12 myoblast tenyésztőközeget felhasználva sikeresen tenyésztettek myoblasztokat és myotubusokat olyan dimenzionális sejtkultúrákban, amelyek a vázizomszövet szerkezetét és működését utánozzák. Ezek a 3D-s szövetkonstrukciók részletes modellt kínálnak a szarkomeraképződés, az izomösszehúzódás alapegységének tanulmányozására. Azáltal, hogy háromdimenziós keretet biztosítanak, az ilyen konstrukciók jelentősen hozzájárulnak a miogenezis és a különböző izomfenotípusok kialakulásának megértéséhez, és fényt derítenek az egyéb fehérjék és a kontraktilis fehérjetartalom összetett összehangolására az izomképződés során.
Vázizomsejtek előállítása: A végső cél továbbra is e kutatás gyakorlati alkalmazása az in vivo izomérlelésre és a vázizomsejtek előállítására, amelynek célja a sérült szövetek helyreállítása vagy pótlása klinikai körülmények között. A szatellitsejtek tenyésztése a hagyományos szérumpótlásos tenyésztéssel kombinálva megteremti az alapjait olyan terápiák kifejlesztésének, amelyek forradalmasíthatják az izommal kapcsolatos betegségek kezelését.
Szarkomer-képződés és kontraktilis funkció: A C2C12 sejtekből származó myotubusok szarkomer-képződése a kutatók elsődleges érdeklődési területe. A szarkomerek az izomsejtek alapvető kontraktilis egységei, és megfelelő összeépülésük döntő fontosságú az izomműködés szempontjából. E struktúrák tanulmányozása értékes információkkal szolgál a kontraktilis fehérjetartalomról és az izom általános egészségéről, különösen akkor, ha a C2C12 sejteket különböző gyógyszereknek vetik alá, amelyek befolyásolhatják ezeket a folyamatokat.
C2C12 sejtek transzfekciós protokollja
Szükséges anyagok:
C2C12 myoblaszt sejtek
Növekedési táptalaj: DMEM 10-20% FBS-szel
Transzfekciós reagens (pl. Lipofectamine)
Plazmid DNS vagy siRNS
Opti-MEM vagy hasonló szérummentes közeg
6 lyukú lemezek vagy tenyésztőedények
37°C-ra, 5% CO2-ra állított inkubátor
Eljárás:
Sejtek beültetése:
Egy nappal a transzfekció előtt ültessük a C2C12 sejteket egy 6 lyukú lemezbe, hogy a transzfekció idején 70-80%-os konfluens arányban legyenek.
DNS-reagens keverék:
Hígítsuk a plazmid DNS-t vagy siRNS-t Opti-MEM-ben (szérum nélkül) olyan végső térfogatra, amely lehetővé teszi az optimális DNS-reagens arányt.
Keverje össze a transzfekciós reagenst Opti-MEM-mel egy külön csőben, és inkubálja szobahőmérsékleten 5 percig.
Egyesítse a DNS és a reagens keverékét, és inkubálja 20 percig szobahőmérsékleten, hogy a komplexképződés lehetővé váljon.
Transzfekció:
Vegye ki a sejtekből a növekedési tápfolyadékot, és cserélje ki azt az Opti-MEM-ben lévő DNS-reagens komplexre.
Inkubálja a sejteket a transzfekciós keverékkel 4-6 órán át az inkubátorban.
Közegcsere:
Az inkubáció után cserélje ki a transzfekciós keveréket friss növekedési táptalajra, és helyezze vissza a sejteket az inkubátorba.
Expresszióelemzés:
Elemezze a transzfekció hatékonyságát 24-48 óra elteltével a transzfektált gén expressziójának vagy a siRNS hatásának ellenőrzésével.
Differenciálási protokoll a C2C12 sejtekhez
Szükséges anyagok:
C2C12 myoblast sejtek
Növesztőközeg: DMEM 10-20% FBS-szel
Differenciáló táptalaj: DMEM 2% lószérummal
6 lyukú lemezek vagy tenyésztőedények
Inkubátor 37 °C-on, 5% CO2-nak megfelelő hőmérsékleten
Eljárás:
Sejtek beültetése:
C2C12 sejteket ültessünk 6 lyukú lemezbe vagy tenyésztőedénybe, és növesszük őket növekedési tápfolyadékban, amíg el nem érik a teljes összefolyást.
Differenciálódás indukciója:
Amint a sejtek konfluensek, szívjuk le a növekedési tápfolyadékot, és cseréljük ki differenciáló tápfolyadékra.
Az alacsony szérumkoncentráció döntő fontosságú a differenciálódás beindításához.
Karbantartás:
A differenciáló tápfolyadékot naponta cserélje, hogy friss tápanyagot biztosítson és eltávolítsa a sejttörmeléket.
A differenciálódás nyomon követése:
Naponta figyelje meg a sejteket mikroszkóp alatt. 1-2 napon belül látnia kell, hogy a myoblasztok egymáshoz igazodnak és összeolvadnak, hogy myotubusokat alkossanak.
A teljes differenciálódás és a miotubusok kialakulása általában 3-5 napon belül következik be.
Elemzés:
A differenciált myotubusok 5-7 nap elteltével készen állnak az olyan downstream alkalmazásokhoz, mint az immunfluoreszcencia vagy a fehérjeexpressziós elemzés.
Megjegyzés: A transzfekció és a differenciálás pontos feltételei (mint például a transzfekciós reagens koncentrációja vagy a szérum százalékos aránya a differenciáló médiumban) változhatnak, és azokat a konkrét kísérleti igények alapján kell optimalizálni. Az optimális feltételekről mindig tájékozódjon a termék adatlapjain vagy a tudományos irodalomban.
Források a C2C12 sejtvonalhoz: C1212 C12C technológia: Protokollok, videók és egyéb
Fedezze fel a C2C12 sejtvonal értékes forrásait:
C2C12 transzfekciós protokoll: C2C12 sejtek in vitro transzfekcióját részletesen bemutató átfogó videós oktatóanyag.
C2C12 mioblasztok: Ez a protokoll útmutató a C2C12 izomsejtek passzázsának és transzfektálásának alapvető fontosságú elemeit tartalmazza.
C2C12 kultúra: A C2C12 sejtek tenyésztéséhez és differenciálásához nyújt kulcsfontosságú betekintést.
C2C12 differenciálás: Ez a dokumentum részletes útmutatót nyújt a C2C12 sejtek fagyasztott kultúrákból történő tenyésztéséhez és differenciálásához.
C2C12 sejtek: C12C12 C12C: Kutatási publikációk
Az alábbiakban a C2C12 sejtekkel foglalkozó jelentős publikációkat emeljük ki:
Interleukin-6 a JAK2-STAT3 jelátvitelen keresztül indukálja a miogén differenciálódást: Az International Journal of Molecular Sciences 2019-es tanulmánya az IL-6 szerepét vizsgálja a C2C12 sejtek miogén differenciálódásában, és fényt derít a mögöttes JAK2/STAT3 jelátviteli útvonalra.
A Rubus Anatolicus levélkivonat hatása a glükóz anyagcserére: A 2023-ban közzétett kutatás a Rubus Anatolicus által a glükózanyagcsere modulációját vizsgálja C2C12 és más sejtvonalakban, ami arra utal, hogy a glikogenezis fokozásában rejlik benne potenciál.
A miosztatin csökkentett hatása a C2C12 sejtek differenciálódására: Ez a 2020 Biomolecules című cikk azt tárgyalja, hogy a C2C12 sejtek differenciálódása jelentősen csökkenti a miosztatin hatását az intracelluláris jelátvitelre, új betekintést nyújtva az izomfejlődésbe.
A genistein hatása az inzulin útvonalhoz kapcsolódó génekre: A Folia Histochemica et Cytobiologica 2018-as tanulmánya differenciált C2C12 sejtek felhasználásával a genistein inzulin útvonal génjeire gyakorolt hatásának felmérésére.
A Moringa Oleifera szerepe az oxidatív anyagcserében: Ez a Phytomedicine Plus (2021) kutatás azt állítja, hogy a Moringa Oleifera levélkivonat a SIRT1-PPARα útvonalon keresztül elősegíti a mitokondriális biogenezist a C2C12 myotubokban.
Gyakran ismételt kérdések a C2C12 sejtekről
Hivatkozások
- Denes, L.T., et al., C2C12 myotube-k tenyésztése mikroformázott zselatin-hidrogéleken felgyorsítja a myotube érését. Skeletal muscle, 2019. 9(1): p. 1-10.
- Wong, C.Y., H. Al-Salami és C.R. Dass, C2C12 sejtmodell: szerepe az inzulinrezisztencia molekuláris szintű megértésében és a preklinikai gyógyszerfejlesztésben. J Pharm Pharmacol, 2020. 72(12): p. 1667-1693.
- Wang, H., et al., A miR-22 szabályozza a C2C12 myoblastok proliferációját és differenciálódását a TGFBR1 célpontjának megcélzásával. European Journal of Cell Biology, 2018. 97(4): p. 257-268.
- Avila-Nava, A., et al., Chaya (Cnidoscolus aconitifolius (Mill.) IM Johnst) levélkivonatok szabályozzák a mitokondriális bioenergetikát és a zsírsav-oxidációt C2C12 myotubokban és primer hepatocitákban. Journal of Ethnopharmacology, 2023. 312: p. 116522.
- Ceci, R., et al., Moringa oleifera levélkivonat védi a C2C12 myotubusokat a H2O2 által kiváltott oxidatív stresszel szemben. Antioxidants, 2022. 11(8): p. 1435.