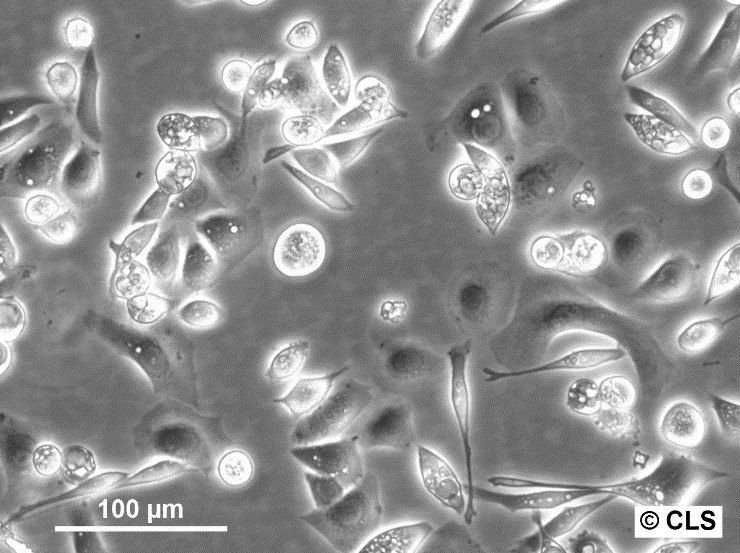
AGS sejtek - A gyomor adenokarcinóma AGS sejtek vizsgálata a rákkutatásban
Az AGS sejtek egy humán gyomor adenokarcinóma sejtvonalat alkotnak, amelyet széles körben használnak az orvosbiológiai kutatásokban. Különösen a gyomorrák biológiájának tanulmányozására használják, beleértve a tumor növekedését, fejlődését, progresszióját és a terápiás beavatkozásokat. Emellett a gazdatest-patogén kölcsönhatások vizsgálatára is használják.
Ez a cikk a gyomor epiteliális AGS sejtek alapjait tárgyalja. Különösen a következőkre tér ki:
- Az AGS sejtek általános jellemzői és eredete
- Az AGS sejtvonalra vonatkozó tenyésztési információk
- AGS sejtvonal: Előnyök és korlátok
- Az AGS sejtek alkalmazása
- Az AGS-sejtvonallal kapcsolatos kutatási publikációk
- Az AGS-sejtvonal forrásai: Jegyzőkönyvek, videók és még sok más
1.az AGS sejtek általános jellemzői és eredete
Egy sejtvonal eredetének és általános jellemzőinek ismerete szükséges, mielőtt elkezdene vele dolgozni. Ez a szakasz a következőkkel foglalkozik: Mik azok az AGS sejtek? Mi az AGS sejtek eredete? Milyen az AGS rákos sejtvonal morfológiája?
- Az AGS sejtvonal egy 54 éves kaukázusi nő gyomor adenokarcinómában szenvedő gyomorszövetéből származik. Izolálására 1979-ben került sor [1].
- Az AGS sejtek epithelszerű morfológiával rendelkeznek.
- A gyomor epithelialis AGS sejtek hiperdiploidok. Az AGS sejtek modális kromoszómaszáma 49, ami a sejtek közel 60%-ában fordul elő. A sejtek körülbelül 3,6%-ában poliploidia is előfordul.
2.az AGS sejtvonalra vonatkozó tenyésztési információk
Egy sejtvonal megfelelő kezeléséhez és menedzseléséhez ismernie kell a sejtvonal alapvető tenyésztési fogalmait. Különösen a következőket kell megtanulnia: Mi az AGS sejtek megduplázódási ideje? Mi az AGS sejtmédia? Hogyan kell az AGS sejteket szubkultiválni? Milyen fagyasztási közegeket használnak a gyomor epiteliális AGS sejtek esetében?
Az AGS sejtek tenyésztésének legfontosabb pontjai
|
Megduplázódási idő: |
Az AGS sejtek megduplázódási ideje 24 és 48 óra között van. |
|
Adhezív vagy szuszpenzióban: |
Az AGS sejtek tapadnak. Monoréteggé nőnek. |
|
Ültetési sűrűség: |
Az AGS sejteket 1 x104 sejt/cm2-es sejtsűrűséggel vetik be. A sejtek ennél a sűrűségnél 3-5 nap alatt konfluens monoréteget képeznek. A régi táptalaj eltávolítása után a sejteket 1 x PBS-szel öblítjük, és Accutase disszociációs oldattal inkubáljuk. A levált sejteket tenyészközegben reszuszpendáltuk és centrifugáltuk. A sejtpelletet ismét reszuszpendáltuk, és az AGS sejtek megszámlálása után új lombikba adagoltuk őket a növekedéshez. |
|
Növesztőközeg: |
Az AGS sejtek tenyésztéséhez DMEM táptalajt használunk, amely 10% FBS-t, 4 mM L-Glutamint, 4,5 g/L glükózt, 1,5 g/L NaHCO3-t és 1,0 mM nátrium-piruvátot tartalmaz. A táptalajt hetente 2-3 alkalommal kell cserélni. |
|
Növekedési feltételek: |
Az AGS sejteket párásított inkubátorban (37°C-os hőmérsékleten) tartjuk, 5%-os CO2-ellátás mellett. |
|
Tárolás: |
A fagyasztott AGS sejteket hosszabb ideig elektromos fagyasztóban, -150°C alatti hőmérsékleten vagy folyékony nitrogén gőzfázisában tartják. |
|
Fagyasztási folyamat és közeg: |
Az AGS-sejtek fagyasztásához CM-1 vagy CM-ACF közeget használnak. A sejtek fagyasztása lassú fagyasztási eljárással történik, amely percenként csak 1°C-os hőmérsékletcsökkenést tesz lehetővé, és védi a sejtek életképességét. |
|
Felolvasztási folyamat: |
A fagyasztott gyomorhámsejteket 37 °C-os vízfürdőben 40-60 másodpercig gyorsan mozgatjuk. A felolvasztott sejteket friss táptalajban reszuszpendáljuk, és új lombikokba öntjük a növekedéshez. A 24 órás inkubáció után a tápfolyadékot megújítjuk, hogy eltávolítsuk a fagyasztó tápközeg összetevőit. Ezzel ellentétben a felolvasztott sejteket centrifugáljuk, és a fagyasztó közeg elemeit eltávolítjuk. Ezután a begyűjtött sejteket ismét reszuszpendálják és a táptalajt tartalmazó lombikba adagolják. |
|
Biológiai biztonsági szint: |
Az AGS sejttenyésztéshez elengedhetetlenek a 2. biológiai biztonsági szintű laboratóriumi körülmények. |
3.aGS sejtvonal: AGS AGS AGS: Előnyök és korlátok
Ez a cikkrész az AGS sejtekkel kapcsolatos néhány kulcsfontosságú előnyre és korlátra világít rá.
Előnyök
A gyomor epiteliális AGS sejtek fő előnyei a következők:
|
Könnyen tenyészthető |
Az AGS gyomorcarcinoma sejtvonal könnyen fenntartható a sejttenyésztő laboratóriumokban. Nincsenek bonyolult és kényes sejttenyésztési követelményei. Ezenkívül jó növekedési tulajdonságokkal rendelkezik, így ideális választás a gyomorrák biológiájának tanulmányozására. |
|
Jelentősége a gyomorrák szempontjából |
Az AGS sejtek emberi gyomor adenokarcinómából származnak, így széles körben használják a gyomorrák biológiájának és a terápiás beavatkozásoknak a tanulmányozására. |
Korlátozások
Az AGS-sejtvonalhoz kapcsolódó korlátozás:
|
In vitro sejtmodell |
Az AGS sejteket biomedicinális kutatólaboratóriumokban mesterséges körülmények között tenyésztik. Ezért előfordulhat, hogy nem teljesen reprodukálják az in vivo gyomorrákos mikrokörnyezetet és más sejt- és molekuláris kölcsönhatásokat. |
4.az AGS sejtek alkalmazása
Az AGS sejteket kifejezetten a gyomorrák biológiájának tanulmányozására használják. Számos más ígéretes alkalmazásuk is van az orvosbiológiai területen. Az AGS sejtek néhány érdekes kutatási alkalmazása a következő:
- Gyomorrák tanulmányozása: Az AGS-sejtek kiváló kutatási eszköz a gyomorrák növekedésének, metasztázisának és inváziójának hátterében álló sejt- és molekuláris mechanizmusok vizsgálatára. A kutatók a gyomor epiteliális AGS sejteket a gyomorrák kialakulásában szerepet játszó különböző sejtfolyamatok, genetikai mutációk és jelátviteli útvonalak tanulmányozására is alkalmazzák. Az Oncology Reports (2019) tanulmánya szerint a microRNS-183-5p.1 a Bcl 2/P53 jelátviteli kaszkád gátlásával ösztönzi a tumorsejtek proliferációját, migrációját és invázióját. Emellett a TPM1 gént is lefelé szabályozza, hogy kifejtse ezeket a hatásokat. Így mind a mikroRNS, mind a TPM1 hatékony molekuláris célpontként javasolt a célzott gyomorrákellenes terápiák kifejlesztéséhez [2].
- Gyógyszeres szűrés: Az AGS-sejteket gyakran használják új és hatékony gyomorrákellenes gyógyszerek szűrésére. A kutatók a potenciális gyógyszerek citotoxicitását és hatékonyságát az AGS-sejtvonal segítségével értékelik. Vizsgálatokat végeztek új molekuláris célpontok azonosítására és új célzott terápiák kifejlesztésére is a gyomorrák elleni küzdelem érdekében. A 2021-ben végzett kutatásban AGS gyomorráksejteket használtak fel, és a paclitaxel hatóanyag terápiás hatását vizsgálták. Az eredmények azt mutatták, hogy a paclitaxel mitotikus katasztrófát, az apoptózis vagy a sejthalál szerves mechanizmusát idézi elő az AGS sejtekben. Emellett elősegítette az autofágiát is a gyomorrákos sejtekben [3].
- Gazdapatogén kölcsönhatások: Az AGS rákos sejtvonal a gazdatest-patogén kölcsönhatásokat is vizsgálja. Ez segít a kutatóknak megérteni a fertőzésben részt vevő sejtmechanizmusokat és válaszokat. Például egy 2020-ban végzett tanulmány megfigyelte, hogy a Helicobacter pylori külső membránvezikuláiban jelen lévő kis nem kódoló RNS-ek csökkentik az interleukin 8 szekrécióját a humán AGS sejtekben [4].
5.aGS sejtvonallal kapcsolatos kutatási publikációk
A cikknek ez a része néhány érdekes és legtöbbet idézett kutatási publikációval foglalkozik, amelyekben AGS sejtek szerepelnek.
A Biomedicine & Pharmacotherapy (2020) című szaklapban megjelent tanulmány azt javasolta, hogy a szalidrozid, egy természetes vegyület, a PI3K/AKT/mTOR jelátviteli útvonal modulációján keresztül védő autofágiát és sejthalált indukál a gyomor epiteliális AGS sejtekben.
Ez a tanulmány a Biomedicine & Pharmacotherapy (2018) című folyóiratban jelent meg. Az asztragalusz poliszacharid és az apatinib hatóanyag szinergista rákellenes hatásait vizsgálta AGS sejtekben. A vizsgálat eredményei azt mutatták, hogy az asztragalus az AKT-szignálfolyamat elnyomása révén fokozza az apatinib tumorellenes hatását.
A Journal of Ethnopharmacology (2018) című folyóiratban megjelent kutatás azt javasolta, hogy a Curcuma zedoaria Roscoe növényből származó természetes vegyület, a curcuzedoalid hozzájárul az AGS-sejtekkel szembeni citotoxicitási potenciálhoz.
A FOXA1 overexpressziója gátolja a humán gyomorrákos AGS sejtek sejtproliferációját és EMT-jét
Ez a Gene (2018) című szaklapban megjelent publikáció azt javasolta, hogy a FOXA1 upregulációja elnyomja az AGS gyomor adenokarcinóma sejtek proliferációját és az epiteliális-mesenchymális átmenetet (EMT) és az inváziót.
Ez a kutatási cikk az International Journal of Medical Microbiology 2020-as számában jelent meg. Ebben a tanulmányban AGS sejteket alkalmaztak a gazdatest-patogén kölcsönhatások tanulmányozására. Az eredmények azt mutatták, hogy a Helicobacter pylori külső membránvezikuláiban bizonyos nem kódoló RNS-t tartalmaz, amely befolyásolja az IL-8 szintjét az AGS sejtekben.
6.az AGS sejtvonal forrásai: Az AGS AGS AGS: protokollok, videók és még sok más
Az alábbiakban néhány forrás található, amelyekben az AGS sejtek szerepelnek.
- AGS sejt transzfekciós protokoll: Ez a videó egy lépésről lépésre történő útmutató a gyomor epiteliális AGS sejtek transzfekciós protokolljának megtanulásához.
Az alábbi link tartalmazza az AGS sejttenyésztési protokollt.
- AGS sejttenyésztési protokoll: Ez a weboldal hasznos információkat tartalmaz az AGS sejtmédiumokról és a sejttenyésztési protokollokról. Röviden, protokollt nyújt a gyomor epiteliális AGS sejtek szubkultúrázásához és a proliferáló és kriokonzervált AGS kultúrák kezeléséhez.
- AGS sejtek szubkultiválása: Ez az oldal részletesen ismerteti az AGS-sejtek szubkultiválási eljárását.
Hivatkozások
- Phuc, B.H., et al., Comparative genomics of two Vietnamese Helicobacter pylori strains, CHC155 from a non-cardia gastric cancer patient and VN1291 from a duodenal ulcer patient. Scientific Reports, 2023. 13(1): p. 8869.
- Lin, J., et al., miRNS-183-5p. 1 elősegíti a gyomorrák AGS-sejtek migrációját és invázióját a TPM1 célba vételével Helyesbítés in/10.3892/or. 2020.7902. Onkológiai jelentések, 2019. 42(6): p. 2371-2381.
- Khing, T.M., et al., A paclitaxel hatása az apoptózisra, az autofágiára és a mitotikus katasztrófára AGS sejtekben. Scientific Reports, 2021. 11(1): p. 23490.
- Zhang, H., et al., Helicobacter pylori külső membrán vezikulák által csomagolt sncRNS-ek csillapítják az IL-8 szekréciót emberi sejtekben. International Journal of Medical Microbiology, 2020. 310(1): p. 151356.