Células HaCaT









Datos esenciales sobre las células Hacat
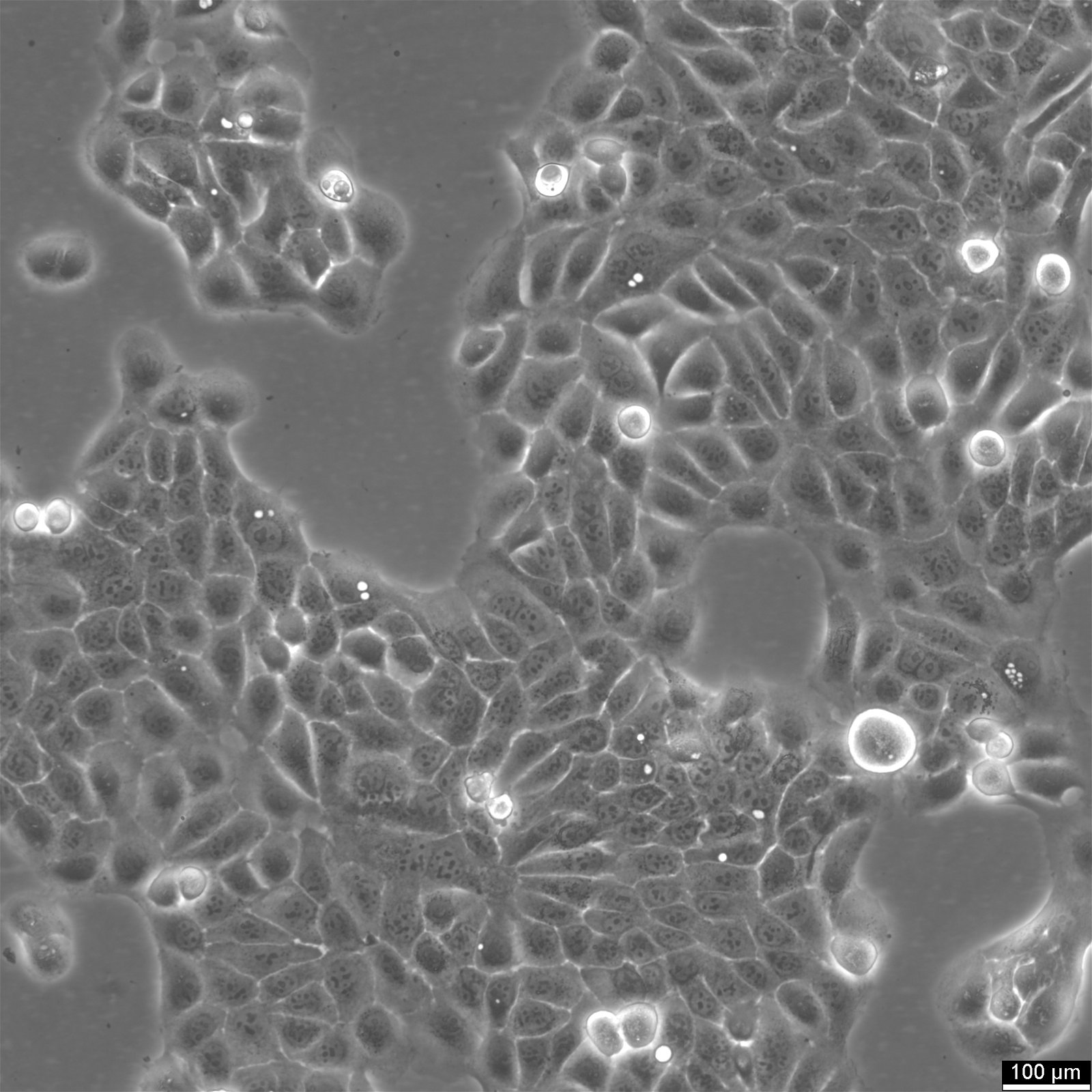
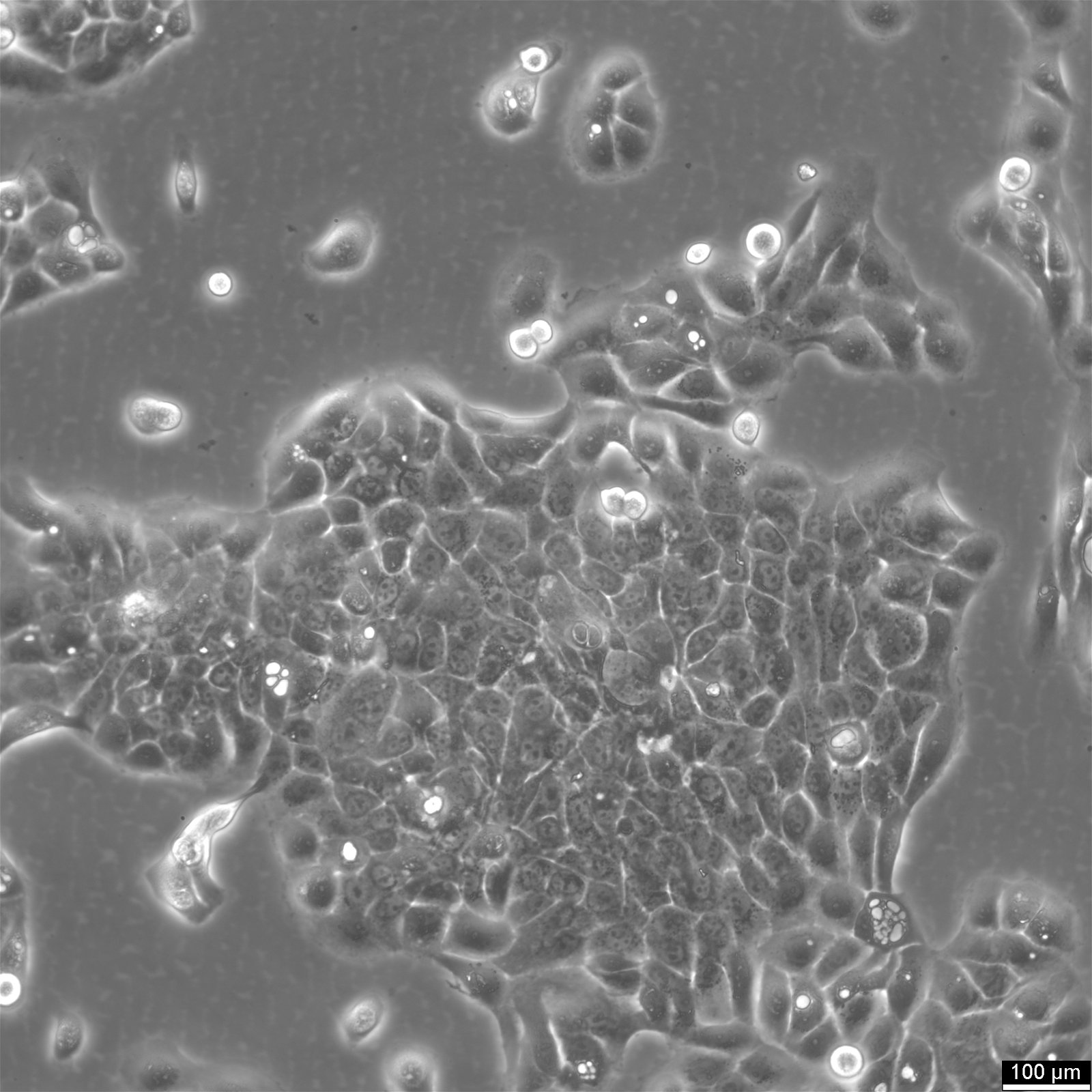
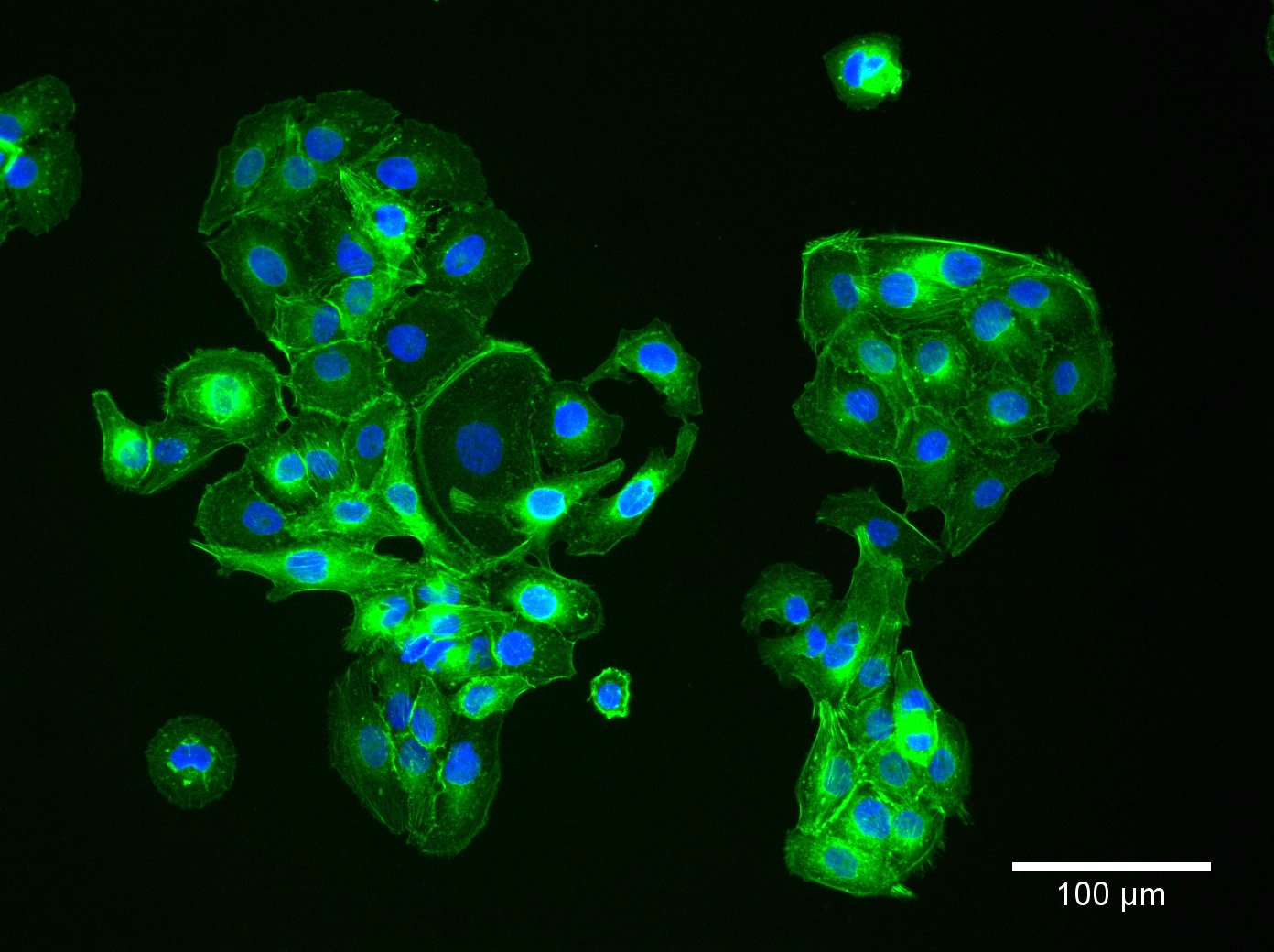
| Descripción | Las células HaCaT son un modelo fundamental en la investigación dermatológica, ya que permiten comprender los complejos mecanismos de la biología y la patología de la piel. La línea celular HaCaT espontáneamente inmortalizada procede de células epidérmicas humanas adultas y conserva la capacidad de proliferar y diferenciarse, de forma similar a los queratinocitos basales in vivo. Las células HaCaT sirven como plataforma robusta para investigar el proceso de diferenciación epidérmica y estudiar los marcadores de diferenciación epidérmica esenciales para mantener la integridad de la piel. La susceptibilidad de las células HaCaT a la apoptosis y su sensibilidad a los agentes inductores de apoptosis se estudian ampliamente, en particular en el contexto de agentes citotóxicos como la RIPL. Los investigadores evalúan las citotoxicidades de estos agentes y el grado de citotoxicidad utilizando células HaCaT, empleando técnicas como la microscopía de fluorescencia para visualizar los cambios celulares. Los investigadores han aprovechado las células HaCaT para examinar los efectos de diversos agentes, incluidos los sustratos antimicrobianos y su influencia en la viabilidad celular. Estas células son un sustrato excelente para probar biomateriales antimicrobianos y sustratos de atelocolágeno antimicrobiano, cruciales para la reparación de la piel y las aplicaciones médicas. La línea epidérmica HaCaT también desempeña un papel crucial en el estudio de la senescencia celular, las citoquinas y los perfiles de expresión génica relacionados con el envejecimiento y las enfermedades crónicas. Los perfiles transcripcionales de las células HaCaT, incluido el papel de κB y los microARN, permiten conocer los mecanismos de regulación a nivel molecular. La línea de queratinocitos HaCaT, con sus características de queratinocitos epidérmicos, ofrece un sistema manejable para diseccionar la intrincada interacción entre las células epidérmicas y el sistema inmunitario, en concreto el papel de los queratinocitos en los estados patológicos. Permiten explorar las modificaciones epigenéticas y su influencia en la diferenciación de los queratinocitos, incluida la formación de la envoltura cornificada, una característica clave en la función de barrera de la piel. En resumen, las células HaCaT son un modelo indispensable en la investigación dermatológica, ya que facilitan una comprensión más profunda de la biología y la patología de la piel gracias a su parecido con los queratinocitos basales y a su capacidad para experimentar crecimiento y diferenciación celular. Su aplicación abarca desde el estudio de la diferenciación epidérmica y los efectos antimicrobianos hasta la exploración de respuestas celulares como la apoptosis, lo que las convierte en piedra angular de la biología celular y la investigación biomédica. |
|---|---|
| Organismo | Humano |
| Tejido | Piel |
Detalles
| Edad | 62 años |
|---|---|
| Género | Hombre |
| Etnia | Caucásico |
| Tipo de célula | Queratinocitos con un diámetro de 20-25 micrómetros. |
| Propiedades de crecimiento | Adherente |
Documentación
| Cita | HaCaT (número de catálogo 300493 de Cytion) |
|---|---|
| Nivel de bioseguridad | 1 |
| NCBI_TaxID | 9606 |
| CellosaurusAccesión | CVCL_0038 |
| Depositante | DKFZ, Heidelberg |
Genética de la línea celular de queratinocitos HaCaT
| Tumorígeno | No |
|---|---|
| Cariotipo | Aneuploide (hipotetraploide) |
Manipulación de la línea celular Hacat
| Medio de cultivo | DMEM, w: 4,5 g/L de glucosa, w: 4 mM de L-glutamina, w: 3,7 g/L de NaHCO3, w: 1,0 mM de piruvato sódico (número de artículo de Cytion 820300a) |
|---|---|
| Suplementos | Complementar el medio con un 10% de FBS |
| Reactivo de disociación | La mezcla 1:1 de EDTA (stock. 0,05%) y tripsina (stock: 0,1%) debe prepararse cada vez antes de separar las células utilizando PBS sin Ca2+ y Mg2+ para proporcionar una osmolaridad fisiológica. No se recomiendan las mezclas de tripsina/EDTA listas para su uso, ya que pueden provocar la formación de grumos celulares. Como alternativa, puede utilizarse TrypLE Express (Life Technologies) en lugar de tripsina/EDTA. Debe seguirse el protocolo del fabricante. |
| Tiempo de duplicación | El tiempo de duplicación de las células HaCaT es de 28 horas. |
| Subcultivo |
|
| Ratio de división | Se recomienda una proporción de 1:5 a 1:10 |
| Densidad de siembra | 1 x 104 células/cm2 |
| Renovación de fluidos | 2 veces por semana |
| Medio de congelación | Como medio de criopreservación, utilizamos el medio de crecimiento completo (incluido FBS) + 10% DMSO para una viabilidad adecuada tras la descongelación, o CM-1 (número de catálogo 800100 de Cytion), que incluye osmoprotectores optimizados y estabilizadores metabólicos para mejorar la recuperación y reducir el estrés crioinducido. |
| Descongelación y cultivo de células |
|
| Atmósfera de incubación | 37°C, 5%CO2, atmósfera humidificada. |
| Recubrimiento de matraces | Para una fijación y viabilidad óptimas tras la descongelación, recomendamos utilizar matraces o placas recubiertos de colágeno. |
| Procedimiento de congelación | Las líneas celulares crioconservadas se envían en hielo seco en envases validados y aislados con suficiente refrigerante para mantener aproximadamente -78 °C durante el tránsito. A la recepción, inspeccione el envase inmediatamente y transfiera los viales sin demora al almacenamiento adecuado. |
| Condiciones de envío | Las líneas celulares crioconservadas se envían en hielo seco en envases validados y aislados con suficiente refrigerante para mantener aproximadamente -78 °C durante el tránsito. A la recepción, inspeccione el envase inmediatamente y transfiera los viales sin demora al almacenamiento adecuado. |
| Condiciones de almacenamiento | Para la conservación a largo plazo, coloque los viales en nitrógeno líquido en fase vapor a una temperatura aproximada de -150 a -196 °C. El almacenamiento a -80 °C sólo es aceptable como breve paso intermedio antes de la transferencia al nitrógeno líquido. |
Garantía de calidad
| Esterilidad | La contaminación por micoplasma se excluye utilizando tanto ensayos basados en la PCR como métodos de detección de micoplasma basados en la luminiscencia. Para garantizar la ausencia de contaminación bacteriana, fúngica o por levaduras, los cultivos celulares se someten a inspecciones visuales diarias. |
|---|---|
| Perfil de STR |
Amelogenina: x,x
CSF1PO: 9,11
D13S317: 10,12
D16S539: 9,12
D5S818: 12
D7S820: 9,11
TH01: 9.3
TPOX: 11,12
vWA: 16,17
D3S1358: 16
D21S11: 28,30.2
D18S51: 12
Penta E: 7,12
Penta D: 11,13
D8S1179: 14
FGA: 24
D1S1656: 11,12
D2S1338: 17,25
D12S391: 18,23
D19S433: 13,14
|
| Alelos HLA |
A*: '31:01:02
B*: '40:01:02, '51:01:01
C*: '03:04:01, '15:02:01
DRB1*: '04:01:01, '15:01:01
DQA1*: '01:02:01, '03:03:01
DQB1*: '03:01:01, '06:02:01
DPB1*: '03:01:01, '04:01:01
E: '01:03:01, '01:03:02
|
Certificado de análisis (CdA)
| Número de lote | Tipo de certificado | Fecha | Número de catálogo |
|---|---|---|---|
| 300493-250324 | Certificado de análisis | 23. May. 2025 | 300493 |
| 300493-190723 | Certificado de análisis | 23. May. 2025 | 300493 |
| 300493-190124 | Certificado de análisis | 23. May. 2025 | 300493 |
| 300493-170225SF | Certificado de análisis | 23. May. 2025 | 300493 |
| 300493-170225 | Certificado de análisis | 23. May. 2025 | 300493 |
| 300493-040424 | Certificado de análisis | 23. May. 2025 | 300493 |
