Células B95-8

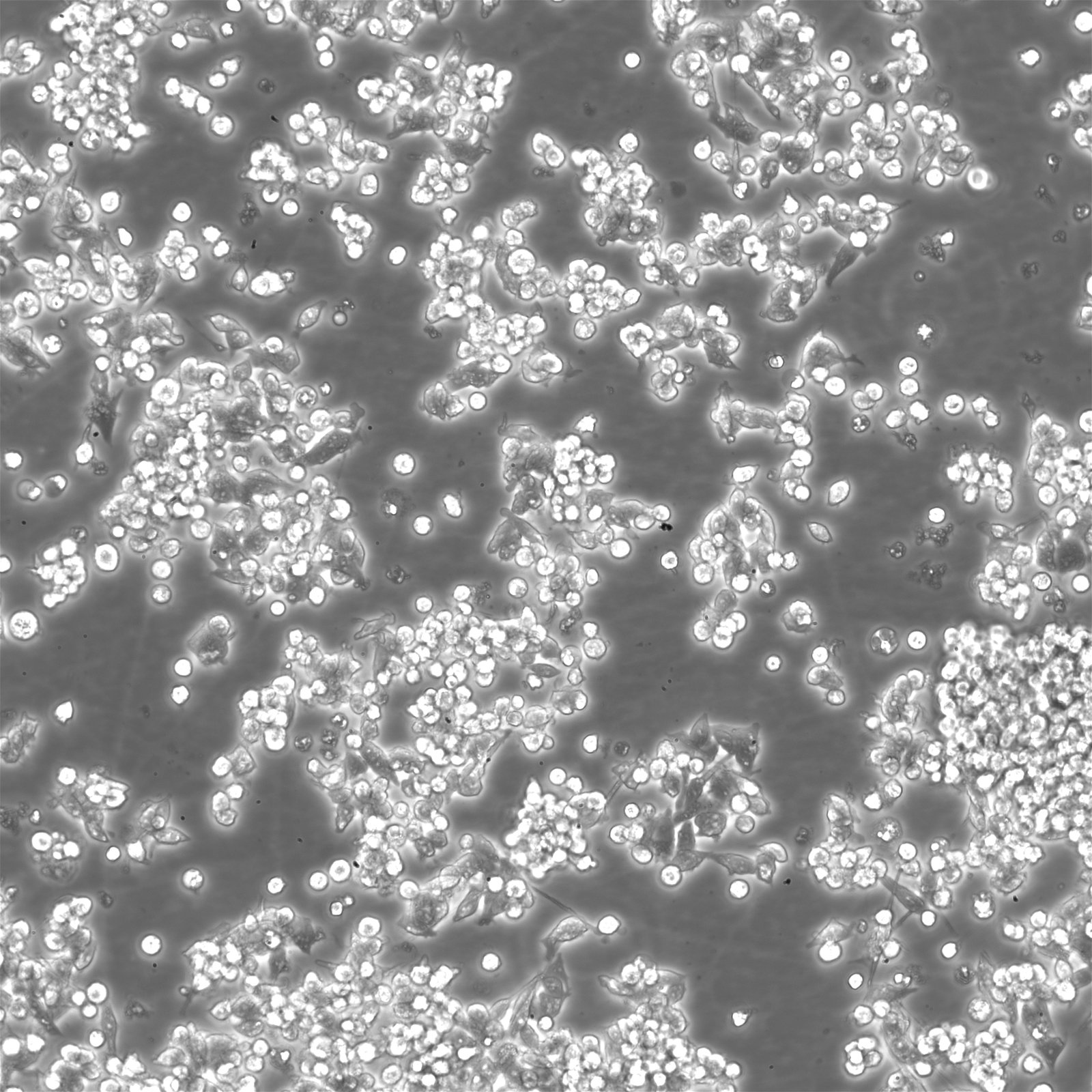






Información general
| Descripción | La línea celular B95-8 es una línea linfoblastoide B inmortalizada de tití, derivada de los leucocitos de sangre periférica de un tití cabeza de algodón (Saguinus oedipus). Esta línea celular se estableció mediante la infección con el virus de Epstein-Barr (VEB), que es un método habitual para inmortalizar células B. La presencia del VEB es fundamental para la utilidad de la línea B95-8 en la investigación, en particular para estudios relacionados con la oncología vírica, las interacciones virus-huésped y la biología del propio VEB. Las células B95-8 se utilizan con frecuencia como fuente del virus de Epstein-Barr en la investigación virológica. Producen partículas de virus infecciosas, lo que las convierte en una herramienta inestimable para la propagación del VEB y para experimentos que requieren virus activos. Además, esta línea celular ha sido fundamental en el desarrollo de vacunas y estrategias terapéuticas contra enfermedades asociadas al VEB, como el linfoma de Burkitt y el linfoma de Hodgkin. Las células también son relevantes en el estudio de la respuesta inmunitaria al VEB, ya que pueden utilizarse para modelizar la transformación de los linfocitos B y comprender los mecanismos de la tumorigénesis inducida por el VEB. |
|---|---|
| Organismo | Tití cabeza de algodón |
| Tejido | Sangre |
| Sinónimos | B95.8, B 95.8, B 95-8, B-95-8, B958, GM07404, GM07404A, GM07404D |
Características
| Género | Mujer |
|---|---|
| Morfología | Linfoblasto |
| Propiedades de crecimiento | Suspensión |
Datos reglamentarios
| Cita | B95-8 (número de catálogo Cytion 601102) |
|---|---|
| Nivel de bioseguridad | 2 |
| NCBI_TaxID | 9490 |
| CellosaurusAccesión | CVCL_1953 |
Datos biomoleculares
Manejo de
| Medio de cultivo | RPMI 1640, con: 2,0 mM de glutamina estable, con: 2,0 g/L de NaHCO3 (número de artículo de Cytion 820700a) |
|---|---|
| Suplementos | Complementar el medio con un 10% de FBS |
| Subcultivo | Homogeneice suavemente la suspensión celular en el matraz pipeteando hacia arriba y hacia abajo, y luego tome una muestra representativa para determinar la densidad celular por ml. Diluya la suspensión para alcanzar una concentración celular de 1 x 105 células/ml con medio de cultivo fresco, y divida la suspensión ajustada en nuevos matraces para su posterior cultivo. |
| Ratio de división | 1:2 a 1:4 |
| Renovación de fluidos | de 2 a 3 veces por semana |
| Medio de congelación | Como medio de criopreservación, utilizamos el medio de crecimiento completo (incluido FBS) + 10% DMSO para una viabilidad adecuada tras la descongelación, o CM-1 (número de catálogo 800100 de Cytion), que incluye osmoprotectores optimizados y estabilizadores metabólicos para mejorar la recuperación y reducir el estrés crioinducido. |
| Descongelación y cultivo de células |
|
| Atmósfera de incubación | 37°C, 5%CO2, atmósfera humidificada. |
| Recubrimiento de matraces | Para una fijación y viabilidad óptimas tras la descongelación, recomendamos utilizar matraces o placas recubiertos de colágeno. |
| Procedimiento de congelación | Las líneas celulares crioconservadas se envían en hielo seco en envases validados y aislados con suficiente refrigerante para mantener aproximadamente -78 °C durante el tránsito. A la recepción, inspeccione el envase inmediatamente y transfiera los viales sin demora al almacenamiento adecuado. |
| Condiciones de envío | Las líneas celulares crioconservadas se envían en hielo seco en envases validados y aislados con suficiente refrigerante para mantener aproximadamente -78 °C durante el tránsito. A la recepción, inspeccione el envase inmediatamente y transfiera los viales sin demora al almacenamiento adecuado. |
| Condiciones de almacenamiento | Para la conservación a largo plazo, coloque los viales en nitrógeno líquido en fase vapor a una temperatura aproximada de -150 a -196 °C. El almacenamiento a -80 °C sólo es aceptable como breve paso intermedio antes de la transferencia al nitrógeno líquido. |
Control de calidad / Perfil genético / HLA
| Esterilidad | La contaminación por micoplasma se excluye utilizando tanto ensayos basados en la PCR como métodos de detección de micoplasma basados en la luminiscencia. Para garantizar la ausencia de contaminación bacteriana, fúngica o por levaduras, los cultivos celulares se someten a inspecciones visuales diarias. |
|---|
Certificado de análisis (CdA)
| Número de lote | Tipo de certificado | Fecha | Número de catálogo |
|---|---|---|---|
| 601102-150125 | Certificado de análisis | 23. Jan. 2026 | 601102 |
Acuerdo de transferencia de material
Si tiene intención de utilizar las líneas celulares Cytion exclusivamente para investigación interna en un único centro de investigación, rellene y firme nuestro Acuerdo de transferencia de material (MTA) y envíelo junto con su pedido.
Para cualquier aplicación comercial, incluyendo, entre otras, trabajos remunerados, pruebas de control de calidad, lanzamiento de productos, uso diagnóstico o estudios normativos, rellene el formulario de uso previsto para que podamos preparar un acuerdo adecuado a su proyecto.
Tenga en cuenta que el MTA solo se aplica a determinadas líneas celulares. Si este aviso y el documento MTA aparecen en la página de un producto, el acuerdo es aplicable. En el caso de las líneas celulares no cubiertas por el MTA, no se mostrará ninguna referencia al acuerdo. El MTA no es válido para clientes de América, China o Taiwán. Póngase en contacto con nuestra entidad en EE. UU. para recibir el acuerdo correspondiente.
