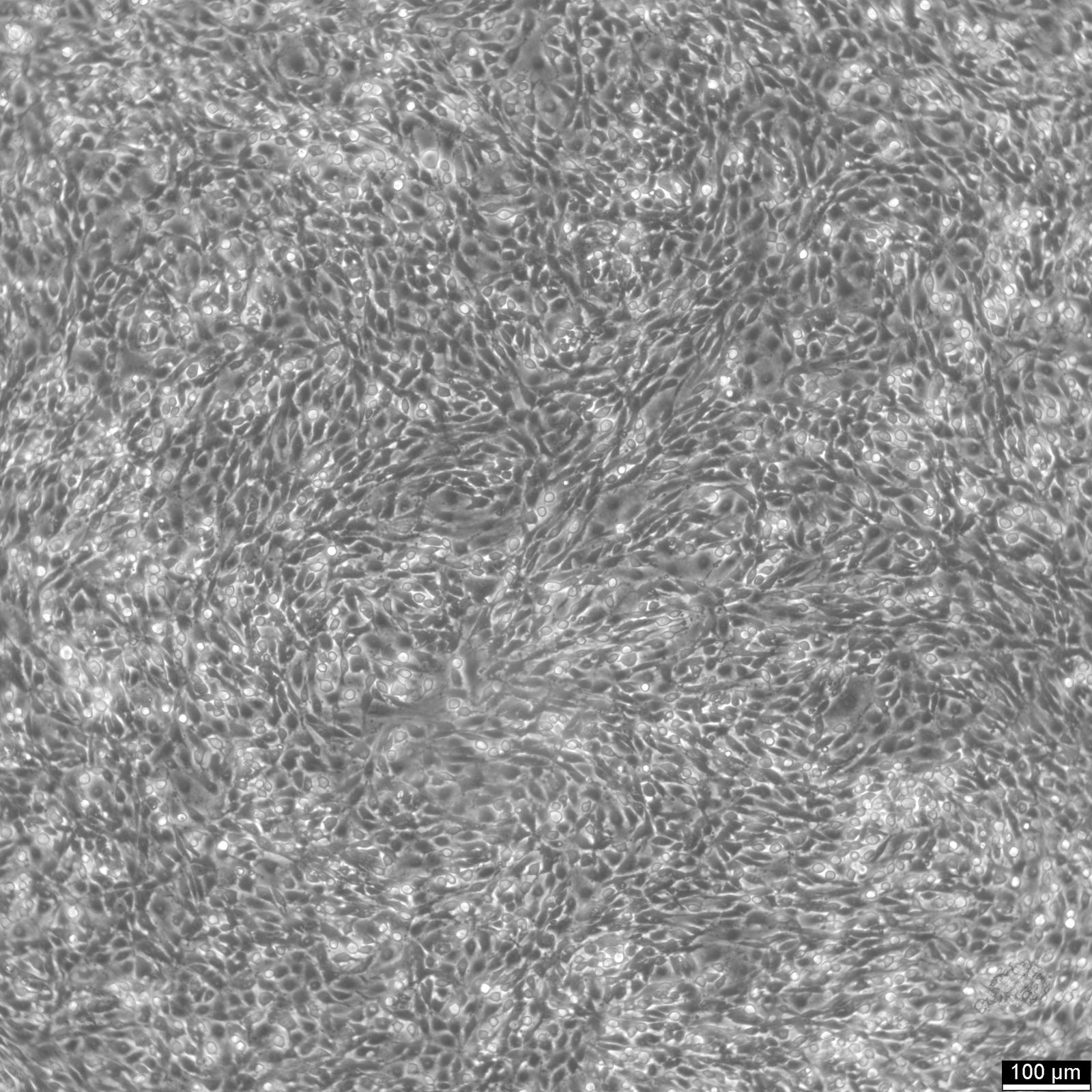
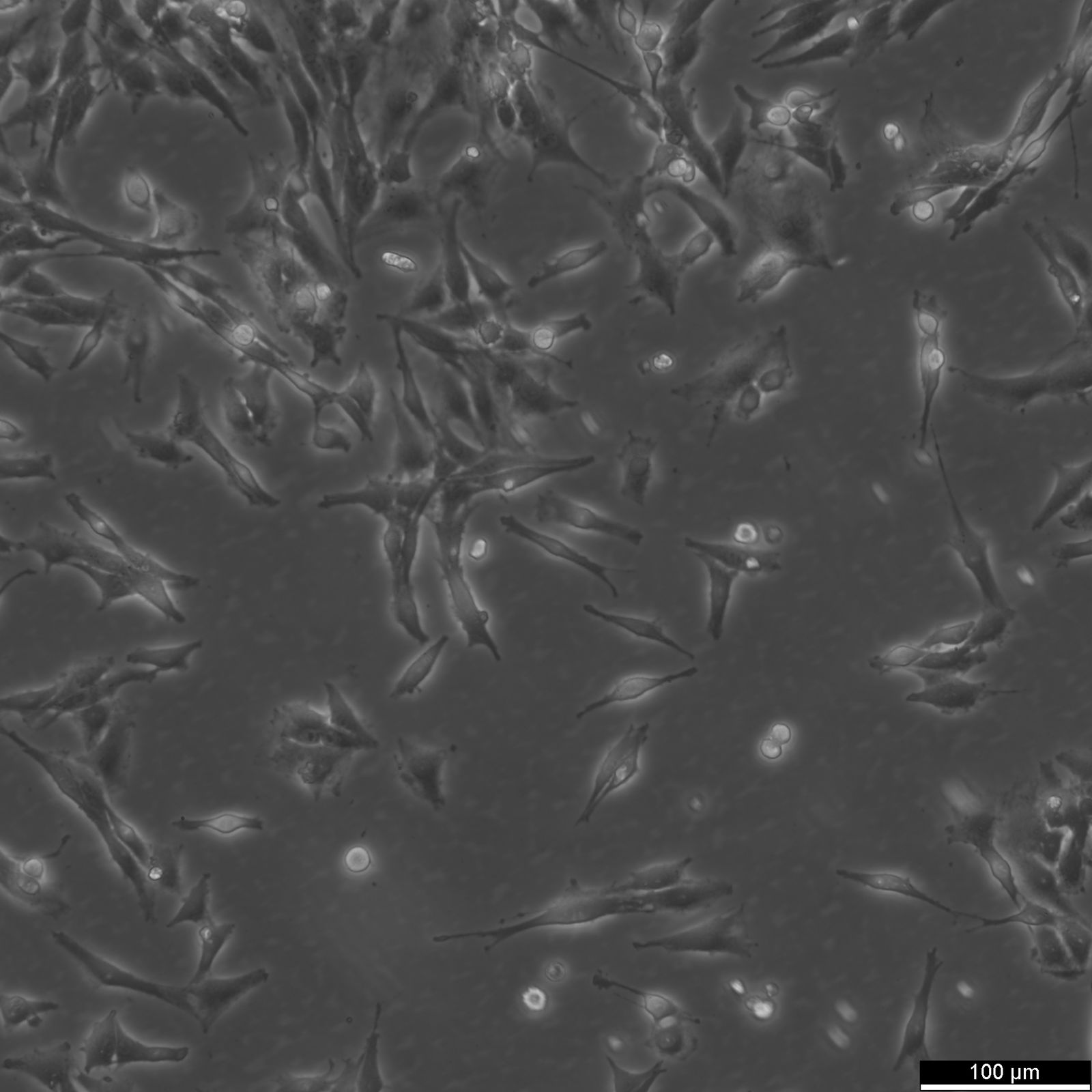
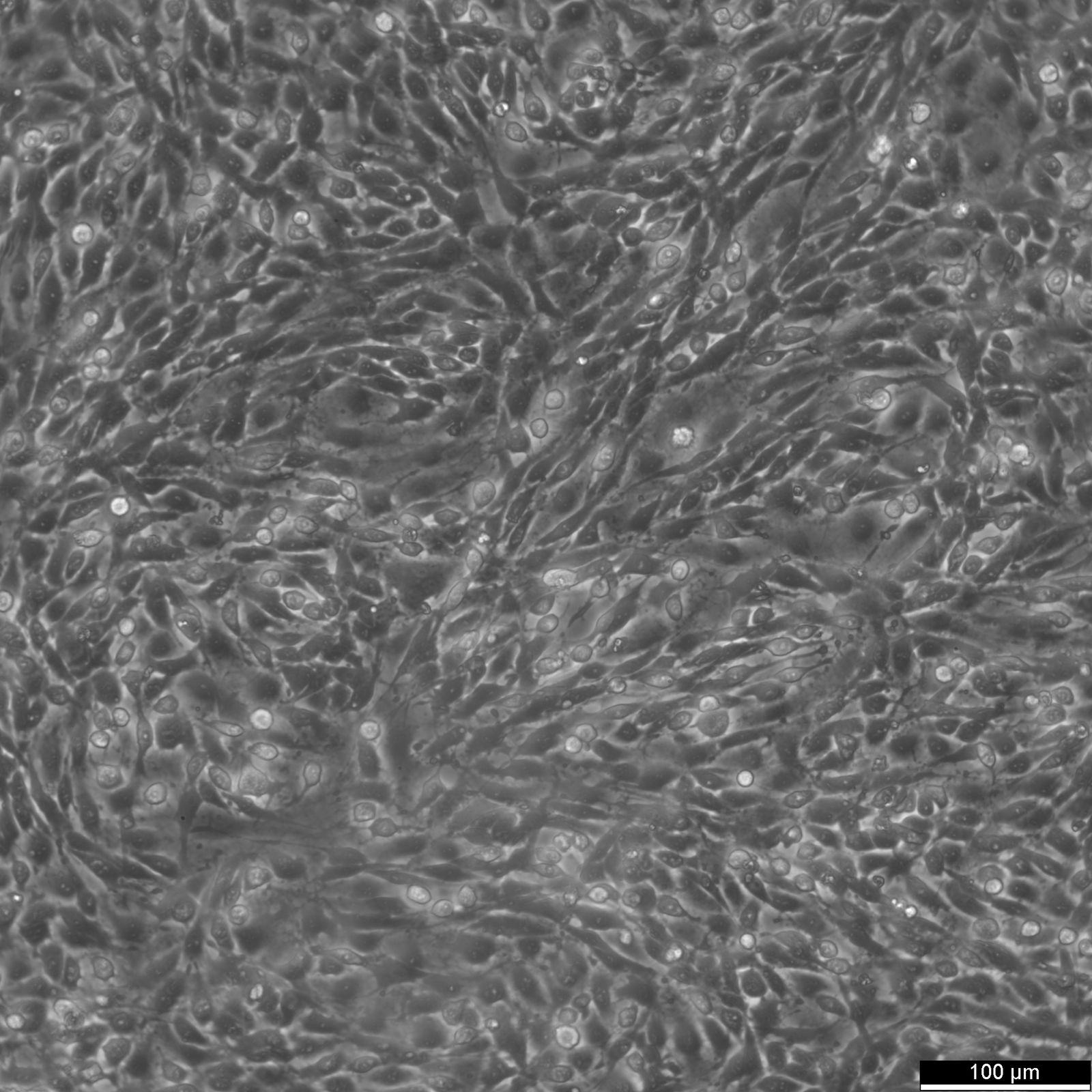
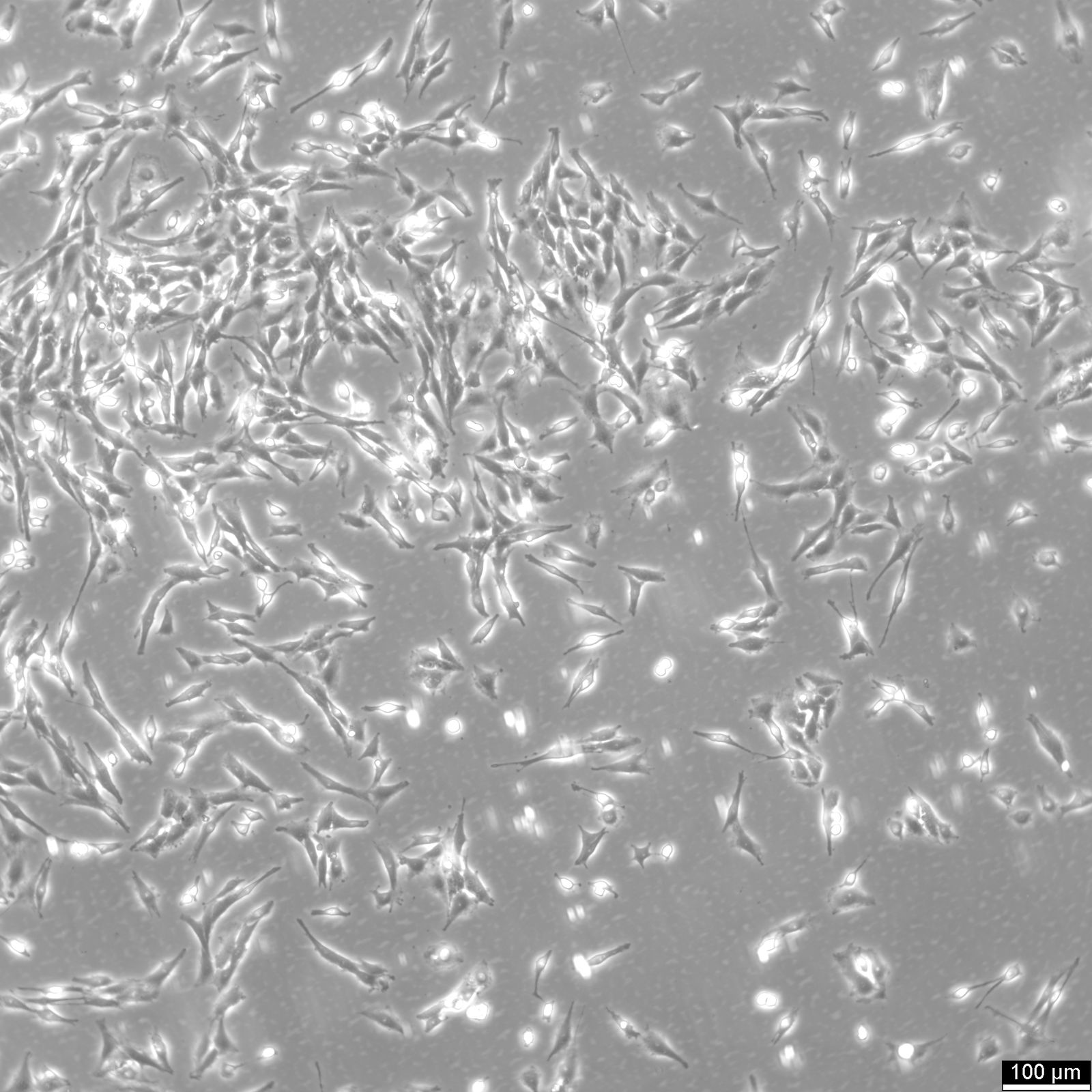
C6-Zellen












430,00 €*
Die Produkte werden tiefgefroren in Trockeneis in Kryoröhrchen versandt. Jedes Kryoröhrchen enthält in der Regel 3 × 10 6 Zellen für adhärente Linien oder 5 × 106 Zellen für Suspensionslinien (Einzelheiten finden Sie im Chargenzertifikat).
Allgemeine Informationen
| Beschreibung | Die C6-Zelllinie unterhält einen Gliazelltyp mit Fibroblastenmorphologie und stammt von einem Gliom einer Wisthar-Furth-Ratte. Das Gliom wurde durch eine Exposition gegenüber N-Nitrosomethylharnstoff ausgelöst, wobei zahlreiche Zyklen mit wechselnden Kultur- und Tierpassagen folgten. Die C6-Gliom-Zelllinie wird häufig in der neuroonkologischen Forschung verwendet, um Tiermodelle zu schaffen, die die Eigenschaften menschlicher Gliome genau nachahmen und so die Entwicklung neuer therapeutischer Wirkstoffe und Strategien unterstützen. Sie ist besonders effektiv in der 3D-Zellkultur und im Hochdurchsatz-Screening. C6-Zellen sind genetisch vielfältig und besitzen ein Wildtyp-p53-Gen, eine erhöhte Rb-Genexpression und einen mutierten p16/Cdkn2a/Ink4a-Locus, aber keine mRNA-Expression von p16 und p19ARF. Sie überexprimieren auch mehrere Gene in menschlichen Gliomen, wie PDGFβ, IGF-1, EGFR und Erb3/Her3-Vorläuferproteine. Die Expression von IGF-2, FGF-9 und FGF-10 ist jedoch reduziert, während die MMP-7 Genexpression unverändert bleibt. Wie menschliche Gliome zeigen auch C6-Zellen eine erhöhte Aktivität der Gene des Ras-Signalwegs, die durch die erhöhte Expression des Ras-Guanintriphosphat-Aktivatorproteins reguliert wird. Die C6-Zelllinie wurde in verschiedenen Studien verwendet. So wurde beispielsweise die Fähigkeit von 2-(2,4-Dihydroxyphenyl)thieno-1,3-thiazin-4-on (BChTT) untersucht, die Vermehrung von Krebszellen zu stoppen und die an diesem Prozess beteiligten Mechanismen zu erforschen. In einer anderen Studie wurden die zytotoxischen und antioxidativen Eigenschaften des superkritischen CO2-Extrakts (SCE) aus dem Bart des alten Mannes (Usnea barbata) mit C6-Zellen untersucht. Interessanterweise wurde berichtet, dass diese Zellen als Reaktion auf Glucocorticoide eine erhöhte Glycerinphosphat-Dehydrogenase-Aktivität aufweisen. |
|---|---|
| Organismus | Ratte |
| Gewebe | Gehirn |
| Krankheit | Gliom |
| Synonyme | C-6, C 6, RGC-6, RGC6, RGc6 |
Merkmale
| Alter | Nicht spezifiziert |
|---|---|
| Geschlecht | Männlich |
| Morphologie | Fibroblastenähnlich |
| Zelltyp | Gliazellen |
| Wachstumseigenschaften | Adhärent |
Regulatorische Daten
| Zitat | C6 (Cytion Katalognummer 500142) |
|---|---|
| Biosicherheitsstufe | 1 |
| NCBI_TaxID | 10116 |
| CellosaurusAccession | CVCL_0194 |
Biomolekulare Daten
| Exprimierte Rezeptoren | Glucocorticoid |
|---|---|
| Viren | Positiv auf LCMV |
| Virusanfälligkeit | Vesikuläre Stomatitis (Indiana), Vaccinia, Herpes simplex |
| Virusresistenz | Polio-Virus 3 |
| Reverse Transkriptase | Negativ |
| Produkte | S-100-Protein, Produktion von Glycerinphosphat-Dehydrogenase als Reaktion auf Glukokortikoide, Somatotropin. |
Handhabung
| Nährboden | RPMI 1640, w: 2,0 mM stabiles Glutamin, w: 2,0 g/L NaHCO3 (Cytion-Artikelnummer 820700a) |
|---|---|
| Supplemente | Ergänzen Sie das Medium mit 10% FBS |
| Dissoziationsreagenz | Accutase |
| Verdopplungszeit | 24 Stunden |
| Subkultivierung | Entfernen Sie das alte Medium von den adhärenten Zellen und waschen Sie sie mit PBS, das kein Kalzium und Magnesium enthält. Für T25-Kolben 3-5 ml PBS und für T75-Kolben 5-10 ml verwenden. Anschließend werden die Zellen vollständig mit Accutase bedeckt, wobei 1-2 ml für T25-Kolben und 2,5 ml für T75-Kolben verwendet werden. Lassen Sie die Zellen 8-10 Minuten bei Raumtemperatur inkubieren, um sie abzulösen. Nach der Inkubation mischen Sie die Zellen vorsichtig mit 10 ml Medium, um sie zu resuspendieren, und zentrifugieren sie dann 3 Minuten lang bei 300xg. Den Überstand verwerfen, die Zellen in frischem Medium resuspendieren und in neue Kolben überführen, die bereits frisches Medium enthalten. |
| Splitverhältnis | Empfohlen wird ein Verhältnis von 1:2 bis 1:3 |
| Aussaatdichte | 1 x 104 Zellen/cm² ergeben in etwa 4 Tagen eine konfluente Schicht. |
| Medienwechsel | 2 bis 3 Mal pro Woche |
| Erholung nach dem Tauwetter | Nach dem Auftauen die Zellen mit einer Dichte von 5 x 104 Zellen/cm² ausplattieren und die Zellen mindestens 24 Stunden lang vom Gefrierprozess erholen und adhärieren lassen. |
| Einfriermedium | Als Kryokonservierungsmedium verwenden wir komplettes Wachstumsmedium (einschließlich FBS) + 10 % DMSO für eine angemessene Lebensfähigkeit nach dem Auftauen oder CM-1 (Cytion Katalognummer 800100), das optimierte Osmoprotektoren und Stoffwechselstabilisatoren enthält, um die Erholung zu verbessern und kryoinduzierten Stress zu reduzieren. |
| Auftauen und Kultivierung von Zellen |
|
| Inkubationsatmosphäre | 37°C, 5%CO2, befeuchtete Atmosphäre. |
| Kolbenbeschichtung | Keine |
| Verfahren zum Einfrieren | Kryokonservierte Zelllinien werden auf Trockeneis in einer validierten, isolierten Verpackung mit ausreichend Kühlmittel versandt, um während des gesamten Transports eine Temperatur von etwa -78 °C aufrechtzuerhalten. Prüfen Sie den Behälter bei Erhalt sofort und bringen Sie die Fläschchen unverzüglich in ein geeignetes Lager. |
| Versandbedingungen | Kryokonservierte Zelllinien werden auf Trockeneis in einer validierten, isolierten Verpackung mit ausreichend Kühlmittel versandt, um während des gesamten Transports eine Temperatur von etwa -78 °C aufrechtzuerhalten. Prüfen Sie den Behälter bei Erhalt sofort und bringen Sie die Fläschchen unverzüglich in ein geeignetes Lager. |
| Lagerungsbedingungen | Zur Langzeitkonservierung werden die Fläschchen in flüssigem Stickstoff bei etwa -150 bis -196 °C gelagert. Eine Lagerung bei -80 °C ist nur als kurzer Zwischenschritt vor der Überführung in flüssigen Stickstoff akzeptabel. |
Qualitätskontrolle / Genetisches Profil / HLA
| Sterilität | Eine Kontamination mit Mykoplasmen wird sowohl durch PCR-basierte Assays als auch durch lumineszenzbasierte Mykoplasmen-Nachweisverfahren ausgeschlossen. Um sicherzustellen, dass keine Kontamination mit Bakterien, Pilzen oder Hefen vorliegt, werden die Zellkulturen täglich visuell überprüft. |
|---|---|
| STR-Profil |
Ratte_D1Wox31: 104
Ratte_D2Wox37: 156
Rat_D19Wox11: 220,228
Rat_D10Wox8: 266
Rat_D4Wox7: 145
Ratte_D2Wox27: 207,215
Ratte_D5Rat33: 122
Rat_D10Wox11: 156,171
Rat_D1Wox23: 214
Ratte_D12Wox1: 406
Ratte_D6Wox2: 104
Rat_D8Wox7: 182
Ratte_D6Cebr1: 233,239
SRY: x,Y
|
Analysezertifikat (CoA)
| Losnummer | Zertifikat Typ | Date | Katalognummer |
|---|---|---|---|
| 500142-615-130624 | Analysezertifikat | 23. May. 2025 | 500142 |
| 500142-34-140624 | Analysezertifikat | 23. May. 2025 | 500142 |
Materialübertragungsvertrag
Wenn Sie die Cytion-Zelllinien ausschließlich für interne Forschungszwecke an einem einzigen Forschungsstandort verwenden möchten, füllen Sie bitte unsere Materialübertragungsvereinbarung (MTA) aus, unterschreiben Sie sie und reichen Sie sie zusammen mit Ihrer Bestellung ein.
Für alle kommerziellen Anwendungen – einschließlich, aber nicht beschränkt auf Dienstleistungen gegen Entgelt, Qualitätskontrolltests, Produktfreigaben, diagnostische Anwendungen oder behördliche Studien – füllen Sie bitte das Formular zur beabsichtigten Verwendung aus, damit wir eine auf Ihr Projekt zugeschnittene Vereinbarung vorbereiten können.
Bitte beachten Sie: Die MTA gilt nur für bestimmte Zelllinien. Wenn dieser Hinweis und das MTA-Dokument auf einer Produktseite erscheinen, ist die Vereinbarung anwendbar. Für Zelllinien, die nicht unter die MTA fallen, wird kein Verweis auf die Vereinbarung angezeigt. Die MTA gilt nicht für Kunden in Amerika, China oder Taiwan. Bitte wenden Sie sich an unsere US-Niederlassung, um die entsprechende Vereinbarung zu erhalten.
-
Erforderliche Produkte
Erforderliche Produkte
Gefriermedium CM-1 - 50 mlVarianten von Kryokonservierungsmedien: 50 mlDas Gefriermedium CM-1 von Cytion ist ein hochmodernes Kryokonservierungsmedium, das ein Höchstmaß an Lebensfähigkeit und Funktionalität der Zellen nach dem Auftauen gewährleistet. Dieses vielseitige Medium eignet sich für ein breites Spektrum von Zelltypen, einschließlich menschlicher und tierischer Zellen, was es zu einem unverzichtbaren Werkzeug für verschiedene Forschungsanwendungen macht. Freeze Medium CM-1 enthält eine sorgfältig ausgewogene Kombination von Kryoprotektoren und essentiellen Nährstoffen und minimiert die Bildung von Eiskristallen und den zellulären Stress während des Einfriervorgangs, so dass die zelluläre Integrität erhalten bleibt.
Zu den wichtigsten Eigenschaften von Freeze Medium CM-1 gehören:
Breite Kompatibilität: Wirksam für eine breite Palette von Zelltypen, einschließlich Primärzellen, Stammzellen und etablierte Zelllinien.
Hohe Lebensfähigkeit: Optimiert, um die Wiederherstellung und Lebensfähigkeit von Zellen nach dem Auftauen zu maximieren und zuverlässige Versuchsergebnisse zu gewährleisten.
Fertig zum Gebrauch: Praktisch vorbereitet und sterilisiert für die sofortige Anwendung, wodurch die Vorbereitungszeit und das Kontaminationsrisiko reduziert werden.
Erhöhte Stabilität: Bewahrt eine gleichbleibende Leistung unter Standard-Kryokonservierungsbedingungen und gewährleistet reproduzierbare Ergebnisse.
Lange Haltbarkeitsdauer: CM-1 ist ein serumhaltiges, gebrauchsfertiges Kryokonservierungsmedium, das bis zu einem Jahr im Kühlschrank aufbewahrt werden kann.
Verwendung von CM-1 zum Einfrieren von Zellen
Gehen Sie wie folgt vor, um CM-1 für das Einfrieren von adhärenten und Suspensionszellen zu verwenden
Bei adhärenten Zellen waschen Sie diese und lösen sie vom Kultursubstrat. Bei Suspensionszellen fahren Sie direkt mit dem nächsten Schritt fort.
Zählen Sie die Zellen, um sicherzustellen, dass sie die richtige Konzentration haben.
Zentrifugieren Sie die Zellen, um sie zu pelletieren, und resuspendieren Sie sie dann in CM-1-Gefriermedium.
Überführen Sie die resuspendierten Zellen in Kryogefäße.
Verwenden Sie eine langsame Gefriermethode, bevor Sie die Zellen in die Langzeitlagerung überführen
Methode
Beschreibung
Schritte
❄️
Manuelles Einfrieren
Eine schrittweise Methode, bei der die Temperatur schrittweise gesenkt wird, um die Lebensfähigkeit der Zellen zu gewährleisten
1️⃣ Zellen in Gefriermedium für 40 Minuten in einen 4°C Gefrierschrank legen.
2️⃣ Für 24 Stunden in einen Gefrierschrank mit -80°C transferieren.
3️⃣ Lagern Sie die Zellen zur langfristigen Konservierung in flüssigem Stickstoff
❄️
Verwendung von Mr. Frosty
Ein praktisches Gerät, das kontrollierte Einfrierraten ohne elektrische Energie ermöglicht
1️⃣ Zellen in Kryo-Gefäßen mit Gefriermedium vorbereiten.
2️⃣ Kryovials in den Mr. Frosty-Behälter stellen.
3️⃣ Lagern Sie die Zellen bei -80°C für 24 Stunden, bevor Sie sie in flüssigen Stickstoff umfüllen
❄️
Controlled-Rate Freezer
Ein hochpräziser Gefrierschrank von Thermo Fisher oder anderen Herstellern, der für eine kontrollierte Temperaturabsenkung ausgelegt ist
1️⃣ Programmieren Sie das Gerät so, dass die Temperatur schrittweise gesenkt wird.
2️⃣ Legen Sie die vorbereiteten Zellen in den Gefrierschrank.
3️⃣ Überführen Sie die Zellen nach dem Gefrierzyklus in flüssigen Stickstoff
Lagern Sie die Kryoflaschen bei Temperaturen unter -130°C oder in flüssigem Stickstoff zur langfristigen Aufbewahrung.
Inhaltsstoffe
Enthält FBS, DMSO, Glucose, Salze
Pufferkapazität: pH = 7,2 bis 7,6
Cytion's Freeze Medium CM-1 bietet eine zuverlässige Lösung für die Kryokonservierung, die eine hohe Lebensfähigkeit und Funktionalität der Zellen nach dem Auftauen für eine Vielzahl von Forschungsanwendungen gewährleistet.59,00 €*RPMI 1640, w: 2,0 mM stabiles Glutamin, w: 2,0 g/L NaHCO3RPMI 1640 Medium, auch bekannt als RPMI-Medium, ist ein äußerst vielseitiges Zellkulturmedium, das in der biologischen Forschung zur Kultivierung verschiedener Säugetierzellen verwendet wird. Dieses Medium wurde 1966 von George E. Moore, Robert E. Gerner und H. Addison Franklin am renommierten Roswell Park Comprehensive Cancer Center entwickelt und hat seinen Namen von seinem Ursprung am Roswell Park Memorial Institute (RPMI).
Ursprünglich für das Wachstum menschlicher Leukämiezellen in Suspensions
- und Monolayerkulturen konzipiert, hat sich RPMI 1640 Medium durch Modifikationen von Forschern und kommerziellen Anbietern weiterentwickelt und ist heute für eine Vielzahl von Säugetierzellen geeignet. Es ist außergewöhnlich kompatibel mit Zelllinien wie HeLa, Jurkat, MCF-7, PC12, PBMC, Astrozyten und Karzinomen.
RPMI 1640 Medium hebt sich von anderen Zellkulturmedien durch seine einzigartige Zusammensetzung ab. Es enthält eine erhebliche Menge an Phosphat, Aminosäuren und Vitaminen. Insbesondere enthält es Biotin, Vitamin B12 und PABA, die in Eagle's Minimal Essential Medium oder Dulbecco's Modified Eagle Medium nicht vorhanden sind. Außerdem weist RPMI 1640 Medium deutlich erhöhte Konzentrationen der Vitamine Inositol und Cholin auf. Es enthält jedoch keine Proteine, Lipide oder Wachstumsfaktoren. Daher ist in der Regel eine Ergänzung mit 10 % fötalem Rinderserum (FBS) erforderlich, um optimale Bedingungen für das Zellwachstum zu schaffen.
Das Puffersystem von RPMI 1640 Medium basiert auf Natriumbicarbonat und erfordert eine 5-10%ige CO2-Umgebung, um einen physiologisch angemessenen pH-Wert zu erhalten. Durch die Zugabe des Reduktionsmittels Glutathion unterscheidet sich dieses Medium weiter von anderen.
Qualitätskontrolle
Steril gefiltert
Lagerung und Haltbarkeit
Vor Licht geschützt bei +2°C bis +8°C lagern.
Nach dem Öffnen bei 4°C lagern und innerhalb von 6-8 Wochen aufbrauchen.
Versandbedingungen
Umgebungstemperatur
Pflege
Gekühlt bei +2°C bis +8°C im Dunkeln aufbewahren. Vermeiden Sie Einfrieren und häufiges Erwärmen auf +37°C, da dies die Produktqualität beeinträchtigt.
Erwärmen Sie das Medium nicht über 37°C und verwenden Sie keine unkontrollierten Wärmequellen wie Mikrowellengeräte.
Wenn nur ein Teil des Mediums verwendet werden soll, entnehmen Sie die erforderliche Menge und erwärmen Sie sie vor der Verwendung auf Raumtemperatur.
Zusammensetzung
Kategorie
Bestandteile
Konzentration (mg/L)
Aminosäuren
Glycin
10.00
L-Alanyl-L-Glutamin
434.40
L-Arginin
200.00
L-AsparaginH2O
56.82
L-Asparaginsäure
20.00
L-Cystin 2HCl
65.20
L-Glutaminsäure
20.00
L-Histidin HClH2O
20.27
L-Hydroxy-L-Prolin
20.00
L-Isoleucin
50.00
L-Leucin
50.00
L-Lysin HCl
40.00
L-Methionin
15.00
L-Phenylalanin
15.00
L-Prolin
20.00
L-Serin
30.00
L-Threonin
20.00
L-Tryptophan
5.00
L-Tyrosin 2Na 2H2O
28.83
L-Valin
20.00
Vitamine
p-Amino-Benzoesäure
1.00
D-Biotin
0.20
Cholinchlorid
3.00
D-Calciumpantothenat
0.25
Folsäure
1.00
myo-Inositol
35.00
Nicotinamid
1.00
Pyridoxin HCl
1.00
Riboflavin
0.20
Thiamin HCl
1.00
Vitamin B12
0.005
Anorganische Salze
Ca(NO3)2 4H2O
100.00
KCl
400.00
MgSO4 7H2O
100.00
NaCl
6000.00
NaHCO3
2000.00
Na2HPO4
800.00
Andere Bestandteile
D-Glucose
2000.00
L-Glutathion Reduziert
1.00
Phenolrot Natriumsalz
5.3025,00 €*AccutaseVarianten: 100 mlAccutase Zelldissoziationsreagenz
- eine schonende Alternative zu Trypsin
Accutase ist eine Zellablösungslösung, die die Zellkulturindustrie revolutioniert. Es ist eine Mischung aus proteolytischen und kollagenolytischen Enzymen, die die Wirkung von Trypsin und Kollagenase nachahmt. Im Gegensatz zu Trypsin enthält Accutase keine Säugetier
- oder Bakterienbestandteile und ist sehr viel schonender für die Zellen, was es zu einer idealen Lösung für die routinemäßige Ablösung von Zellen von Standardplastikgefäßen für die Gewebekultur und adhäsionsbeschichteten Plastikgefäßen macht. In diesem Blogbeitrag gehen wir auf die Vorteile und Einsatzmöglichkeiten von Accutase ein und zeigen, wie es die Zellkultur verändert.
Vorteile von Accutase
Accutase hat mehrere Vorteile gegenüber herkömmlichen Trypsinlösungen. Erstens kann es immer dann eingesetzt werden, wenn eine sanfte und effiziente Ablösung von adhärenten Zelllinien erforderlich ist, und ist somit ein direkter Ersatz für Trypsin. Zweitens funktioniert Accutase sehr gut bei embryonalen und neuronalen Stammzellen, und es hat sich gezeigt, dass die Lebensfähigkeit dieser Zellen nach der Passage erhalten bleibt. Drittens bewahrt Accutase die meisten Epitope für die anschließende durchflusszytometrische Analyse, was es ideal für die Analyse von Zelloberflächenmarkern macht.
Außerdem muss Accutase bei der Passage von adhärenten Zellen nicht neutralisiert werden. Durch die Zugabe weiterer Medien nach der Zellteilung wird die Accutase verdünnt, so dass sie nicht mehr in der Lage ist, Zellen abzulösen. Dadurch entfällt der Schritt der Inaktivierung, und die Zellkulturtechniker sparen Zeit. Schließlich muss Accutase nicht aliquotiert werden, und eine Flasche ist im Kühlschrank 2 Monate lang haltbar.
Anwendungen von Accutase
Accutase ist ein direkter Ersatz für Trypsinlösung und kann für die Passage von Zelllinien verwendet werden. Darüber hinaus eignet sich Accutase gut zum Ablösen von Zellen für die Analyse vieler Zelloberflächenmarker mittels Durchflusszytometrie und für die Zellsortierung. Andere nachgeschaltete Anwendungen der Accutase-Behandlung umfassen die Analyse von Zelloberflächenmarkern, Viruswachstumstests, Zellproliferation, Tumorzellmigrationsassays, routinemäßige Zellpassage, Produktionsskalierung (Bioreaktor) und Durchflusszytometrie.
Zusammensetzung von Accutase
Accutase enthält keine Bestandteile von Säugetieren oder Bakterien und ist eine natürliche Enzymmischung mit proteolytischer und kollagenolytischer Enzymaktivität. Es ist in einer viel niedrigeren Konzentration als Trypsin und Kollagenase formuliert, wodurch es weniger toxisch und sanfter, aber genauso wirksam ist.
Wirksamkeit von Accutase
Accutase ist nachweislich effizient bei der Ablösung von Primär
- und Stammzellen und erhält die hohe Lebensfähigkeit der Zellen im Vergleich zu Enzymen tierischen Ursprungs wie Trypsin. 100 % der Zellen werden nach 10 Minuten zurückgewonnen, und dank der Selbstverdauung von Accutase ist es unbedenklich, Zellen bis zu 45 Minuten in Accutase zu belassen.
Zusammenfassung
Zusammenfassend lässt sich sagen, dass Accutase eine leistungsstarke Lösung ist, die das Spiel in der Zellkultur verändert. Mit seiner sanften Natur, Effizienz und Vielseitigkeit ist Accutase die ideale Alternative zu Trypsin. Wenn Sie nach einer zuverlässigen und effizienten Lösung für die Zellablösung suchen, ist Accutase die richtige Lösung für Sie.75,00 €*Antibiotika/Antimykotika-Lösung (100x)Produktübersicht
Volumen: 100 ml Lagerung: ≤-15°C Sterilität: Steril-gefiltert
Antibiotika-/Antimykotika-Lösung (100x) ist ein steriles, gebrauchsfertiges Konzentrat zur Verringerung des Risikos einer mikrobiellen Kontamination in Zellkulturen und ähnlichen Laboranwendungen. Diese 100-fache Lösung enthält eine bewährte Kombination aus Penicillin, Streptomycin und Amphotericin B, die ein breites antimikrobielles Wirkungsspektrum gegen grampositive und gramnegative Bakterien, Hefen und filamentöse Pilze bietet. Die Formulierung eignet sich für den Einsatz in eukaryotischen Zellkulturen, bakteriellen Medien und anderen kontaminationsanfälligen Systemen und unterstützt saubere und konsistente Laborabläufe.
Anwendung und Vorteile Diese Lösung wurde für routinemäßige Forschungsprotokolle optimiert und wird häufig zur Aufrechterhaltung aseptischer Bedingungen in Zellkultur-Workflows verwendet. Sie bietet zuverlässige Leistung in kontaminationsanfälligen Umgebungen und hilft Forschern, das Risiko einer mikrobiellen Überwucherung zu reduzieren, ohne die Gesundheit der Zellen oder die Reproduzierbarkeit der Experimente zu beeinträchtigen. Die steril gefilterte Formulierung macht zusätzliche Solubilisierungsschritte überflüssig, unterstützt eine rationalisierte Medienvorbereitung und reduziert die Variabilität in den täglichen Laborabläufen.
Verwendung und Kompatibilität Um Standard-Arbeitskonzentrationen zu erreichen, verdünnen Sie die Lösung 1:100 in Ihr komplettes Kulturmedium. Das Produkt ist mit einer breiten Palette von Säugetierzelllinien und Basalmedien kompatibel. Dank der konstanten Verfügbarkeit der Vorräte profitieren Forscher von einer zuverlässigen Lieferkontinuität und einer vereinfachten Logistikplanung. Die Lösung sollte bei ≤ -15 °C gelagert und vor wiederholten Gefrier-Auftau-Zyklen geschützt werden, um die Stabilität zu erhalten. Nur für den Forschungsgebrauch. Nicht zur Verwendung in diagnostischen oder therapeutischen Verfahren. Nicht zur Anwendung bei Menschen oder Tieren.45,00 €*PBSPhosphatgepufferte Kochsalzlösung (PBS)
Phosphatgepufferte Kochsalzlösung (PBS) ist eine weit verbreitete Pufferlösung in der biologischen und chemischen Forschung. Sie spielt eine entscheidende Rolle bei der Aufrechterhaltung des pH-Gleichgewichts und der Osmolarität während verschiedener experimenteller Verfahren, einschließlich Gewebeverarbeitung und Zellkultur. Unsere PBS-Lösung wird sorgfältig mit hochreinen Inhaltsstoffen formuliert, um Stabilität und Zuverlässigkeit bei jedem Experiment zu gewährleisten. Die Osmolarität und die Ionenkonzentration unserer PBS-Lösung sind denen des menschlichen Körpers sehr ähnlich, so dass sie isotonisch und für die meisten Zellen ungiftig ist.
Zusammensetzung unserer PBS-Lösung
Unsere PBS-Lösung ist eine pH-angepasste Mischung aus hochreinen Phosphatpuffern und Kochsalzlösungen. Bei einer 1fachen Arbeitskonzentration enthält sie:
8000 mg/L Natriumchlorid (NaCl)
200 mg/L Kaliumchlorid (KCl)
1150 mg/L Natriumphosphat dibasisch wasserfrei (Na2HPO4)
200 mg/L Kaliumphosphat einbasig wasserfrei (KH2PO4)
Diese Zusammensetzung gewährleistet ein optimales pH
- und Ionengleichgewicht und eignet sich für eine breite Palette biologischer Anwendungen.
Anwendungen unserer PBS-Lösung
Unsere PBS-Lösung ist ideal für verschiedene Anwendungen in der biologischen Forschung. Aufgrund ihrer isotonischen und ungiftigen Eigenschaften eignet sie sich für die Verdünnung von Substanzen und die Spülung von Zellbehältern. PBS-Lösungen, die EDTA enthalten, sind wirksam, um anhaftende und verklumpte Zellen abzulösen. Zweiwertige Metalle wie Zink sollten jedoch nicht zu PBS hinzugefügt werden, da dies zu Ausfällungen führen kann. In solchen Fällen werden Good's Puffer empfohlen. Außerdem ist unsere PBS-Lösung eine akzeptable Alternative zu viralen Transportmedien für den Transport und die Lagerung von RNA-Viren, einschließlich SARS-CoV-2.
Qualitätskontrolle
Steril gefiltert
Lagerung und Haltbarkeit
Vor Licht geschützt bei +2°C bis +25°C lagern.
Nach dem Öffnen bei 2°C bis 25°C lagern und innerhalb von 24 Monaten verbrauchen.
Versandbedingungen
Umgebungstemperatur
Pflege
Gekühlt bei +2°C bis +8°C im Dunkeln aufbewahren. Vermeiden Sie Einfrieren und häufiges Erwärmen auf +37°C, da dies die Produktqualität beeinträchtigt.
Erwärmen Sie das Medium nicht über 37°C und verwenden Sie keine unkontrollierten Wärmequellen wie Mikrowellengeräte.
Wenn nur ein Teil des Mediums verwendet werden soll, entnehmen Sie die erforderliche Menge und erwärmen Sie sie vor der Verwendung auf Raumtemperatur.
Zusammensetzung
Kategorie
Bestandteile
Konzentration (mg/L)
Salze
Kaliumchlorid
200
Kaliumphosphat monobasisch wasserfrei
200
Natriumchlorid
8000
Natriumphosphat zweibasisch wasserfrei
115020,00 €*





