الخلايا الجذعية الوسيطة اللحمية البشرية - نخاع العظام (HMSC-BM)

























معلومات عامة
| الوصف | تمثل الخلايا الجذعية الوسيطة البشرية المشتقة من نخاع العظم (HMSC-BM) أداة قوية ومتعددة الاستخدامات للبحوث المختبرية. تتمتع هذه الخلايا الوسيطة المتعددة القدرات (MSCs) بقدرة فريدة على التجدد الذاتي والتمايز إلى مجموعة واسعة من أنواع الخلايا، بما في ذلك الخلايا الدهنية والخلايا العظمية والخلايا الغضروفية. تم توثيق قدرة HMSC-BM على التمايز إلى هذه السلالات الثلاث الرئيسية بشكل جيد، مما يجعلها ذات قيمة لا تقدر بثمن للدراسات التي تركز على الطب التجديدي وهندسة الأنسجة ومسارات التمايز الخلوي. يتم زراعة هذه الخلايا الجذعية الوسيطة في ظل ظروف صارمة، مما يضمن تعدد قدراتها وقابليتها العالية للحياة بعد الذوبان. إحدى السمات المميزة لخلايا HMSC-BM مقارنة بالخلايا الجذعية المتعددة القدرات المشتقة من مصادر أخرى، مثل الأنسجة الدهنية أو الحبل السري، هي قدرتها الفائقة على التمايز العظمي. وهذا يجعلها مفيدة بشكل خاص في بيولوجيا العظام وأبحاث جراحة العظام، حيث يعد فهم الآليات الجزيئية التي تحكم تكوين العظام وإصلاحها أمرًا بالغ الأهمية. بالإضافة إلى ذلك، تتميز الخلايا الجذعية الوسيطة النخاعية العظمية (HMSC-BM) بخصائص مناعية قوية، مما يجعلها نموذجًا ممتازًا لدراسة التفاعلات المناعية والاستجابات الالتهابية. هذه الخصائص الفريدة تجعل الخلايا الجذعية الوسيطة النخاعية العظمية (HMSC-BM) الخيار المفضل للدراسات ما قبل السريرية التي تستكشف البيئة الدقيقة لنخاع العظم، وتكوين الدم، والفيزيولوجيا المرضية للأمراض المرتبطة بنخاع العظم. تحتوي كل أنبوبة تبريد من HMSC-BM على ما لا يقل عن 1 × 106 خلية، مع معدلات قابلية للحياة تتراوح بين 92٪ و 95٪، وفقًا لاختبار استبعاد صبغة Trypan Blue. هذه الخلايا مشتقة من نخاع العظم المأخوذ من متبرعين بالغين أصحاء، وقد قدموا جميعًا موافقة مستنيرة. لضمان أعلى المعايير، تخضع كل دفعة لاختبارات صارمة لمراقبة الجودة لتقييم تحديد الخلايا ونقاوتها وقوتها وقابليتها للحياة. تضمن هذه الاختبارات الشاملة أن الخلايا الجذعية المتعددة القدرات (MSCs) تفي بمعايير صارمة، مما يجعلها مناسبة لمجموعة واسعة من التطبيقات البحثية، بما في ذلك دراسات بيولوجيا الخلايا واكتشاف الأدوية ودراسة الاستجابات الخلوية لمختلف المحفزات. هذه الخلايا غير مخصصة للاستخدامات العلاجية أو التطبيقات الحية، ويقتصر استخدامها على الأغراض البحثية في بيئة مختبرية خاضعة للرقابة. |
|---|---|
| كائن حي | الإنسان |
| الأنسجة | النخاع العظمي |
| التطبيقات | اختبار الأدوية، والطب التجديدي، وأبحاث الأمراض |
الخصائص
| العمر | يُرجى الاستفسار |
|---|---|
| الجنس | يُرجى الاستفسار |
| العرق | قوقازي |
| علم الصرف | مورفولوجيا شبيهة بالأرومة الليفية ذات الشكل المغزلي المنتشر بشكل جيد خلال 5 ممرات على الأقل. يُظهر أقل من 2% من الخلايا مورفولوجيا شبيهة بالأرومة الليفية العضلية العفوية خلال كل ممر. |
| نوع الخلية | الخلايا الجذعية |
| خصائص النمو | ملتزم |
البيانات التنظيمية
| اقتباس | الخلايا الجذعية الوسيطة اللُّحمية البشرية، نخاع العظم (HMSC-BM) (كتالوج سيتيون رقم 300665) |
|---|---|
| مستوى السلامة البيولوجية | 1 |
| NCBI_TaxID | 9606 |
البيانات الجزيئية الحيوية
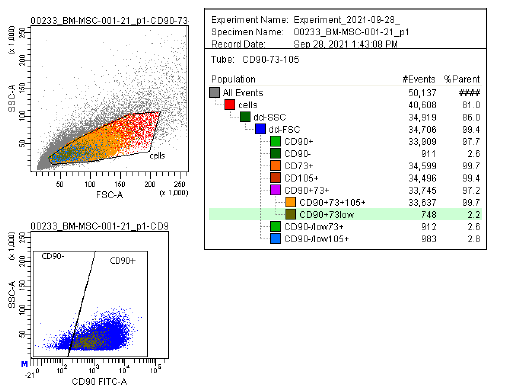
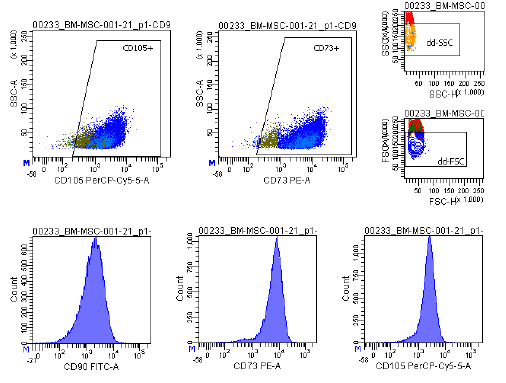
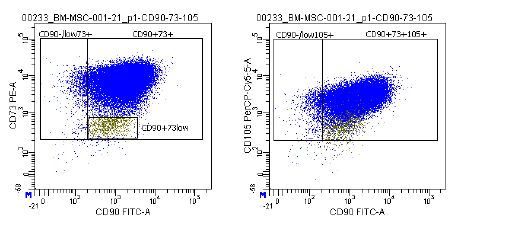
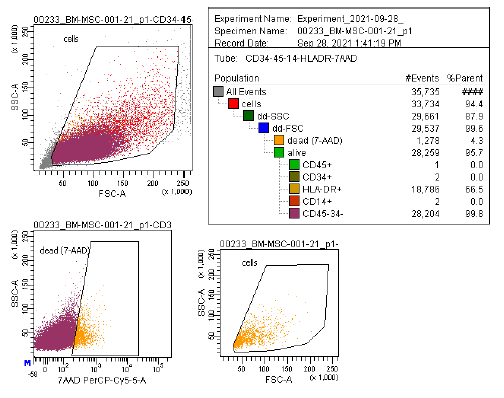
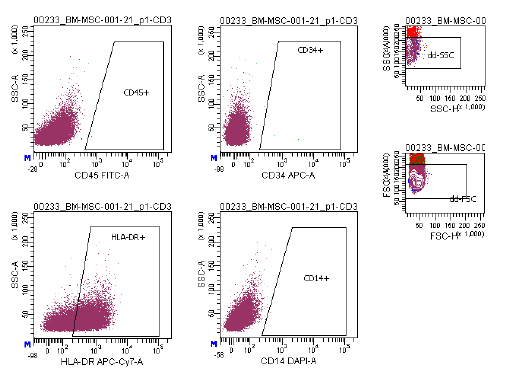
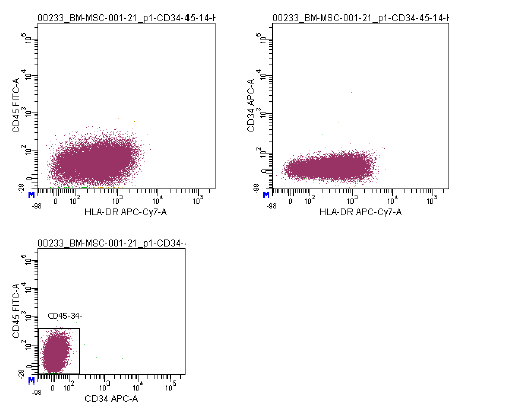
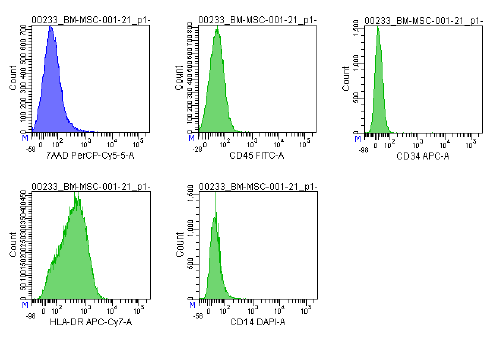
| التعبير عن المستضد | تُستخدم مجموعة شاملة من الواسمات، بما في ذلك CD73/CD90/CD105 (إيجابية) وCD14/CD34/CD34/CD45/HLA-DR (سلبية)، في تحليل قياس التدفق الخلوي لتحديد الخلايا الجذعية الصلبة المستزرعة (P2-P3) قبل الحفظ بالتبريد. هذه العلامات موصى بها من قبل لجنة الخلايا الجذعية الصلبة متعددة الخلايا التابعة للمعهد الدولي لتكنولوجيا الخلايا الجذعية الصلبة. |
|---|---|
| الفيروسات | لا يوجد لدى المتبرع فيروس التهاب الكبد BV (تفاعل البوليميراز المتسلسل) وفيروس التهاب الكبد BV (تفاعل البوليميراز المتسلسل) وفيروس نقص المناعة البشري-1/2 (IFA). الخلايا سلبية لفيروس التهاب الكبد BV وفيروس التهاب الكبد C وفيروس التهاب الكبد C وفيروس HSV1 وفيروس HSV2 وفيروس التهاب الكبد CMV وفيروس التهاب الكبد CMV وفيروس التهاب الكبد EBV وفيروس HHV6 وفيروس HHV6 والتوكسوبلازما جوندي والتريبونيما الشاحبة والمتدثرة الحثرية واليوريا اليورياليتكوم واليوريا البارفومية. |
المناولة
| الوسط الثقافي | Alpha MEM، ث: 2.0 مللي مولار جلوتامين مستقر، ث / س: ريبونوكليوسيدات، ث: 1.0 ميلي مولار بيروكليوسيدات الصوديوم: ديوكسي ريبونوكليوسيدات، ث: 1.0 ملي مولار بيروفات الصوديوم، ث: 2.2 جم/لتر NaHCO3 |
|---|---|
| المكملات الغذائية | يُضاف إلى الوسط 10٪ FBS، و2 نانوغرام/ملل من عامل النمو الجيني الوراثي bFGF |
| كاشف التفكك | التربسين-إدتا |
| الاستزراع الفرعي | لمزرعة الخلايا الملتصقة الروتينية: اشفط وسط المزرعة القديم من الخلايا الملتصقة، واغسلها بمحلول PBS لإزالة أي وسط متبقي. بعد شفط PBS، أضف الكمية المناسبة من محلول التربسين/إيدتا بناءً على حجم وعاء المزرعة (على سبيل المثال، 1 مل لقارورة T25، و3 مل لقارورة T75) واحتضانها في درجة حرارة الغرفة أو 37 درجة مئوية حتى تنفصل الخلايا (5-10 دقائق). راقب الانفصال تحت المجهر، واضغط برفق على الوعاء إذا لزم الأمر لتحرير الخلايا. بمجرد الانفصال، أضف وسطًا كاملاً لتعطيل التريبسين/إيدتا، وأعد ترسيب الخلايا برفق وانقل كمية قليلة من معلق الخلايا إلى وعاء مستنبت جديد يحتوي على وسط جديد. ضع الوعاء في حاضنة مضبوطة على 37 درجة مئوية مع 5% من ثاني أكسيد الكربون، وقم بتغيير الوسط كل 2-3 أيام. |
| كثافة البذر | 1 إلى 3 × 104 خلية/سم2 |
| تجديد السوائل | أول تجديد للسوائل بعد 24 ساعة، ثم كل يومين إلى 3 أيام. |
| وسيط التجميد | كوسيط للحفظ بالتبريد، نستخدم 80% من FBS + 10% وسط قاعدي + 10% DMSO للحفاظ على الحيوية أو CM-1 (كتالوج Cytion رقم 800100) للحماية الفائقة بالتبريد، مما يمنع التمايز غير المرغوب فيه مع الحفاظ على تعدد القدرات. |
| إذابة الخلايا وزراعتها |
|
| أجواء الاحتضان | 37 درجة مئوية، و5% من ثاني أكسيد الكربون في جو مرطب. |
| طلاء القارورة | للحصول على التعلق الأمثل والصلاحية المثلى بعد الذوبان، نوصي باستخدام قوارير أو أطباق مغطاة بالكولاجين. |
| إجراء التجميد | يتم شحن سلالات الخلايا المحفوظة بالتبريد على ثلج جاف في عبوات معزولة وموثوقة مع مبرد كافٍ للحفاظ على درجة حرارة -78 درجة مئوية تقريبًا طوال فترة النقل. عند الاستلام، افحص الحاوية على الفور وانقل القوارير دون تأخير إلى المخزن المناسب. |
| شروط الشحن | يتم شحن سلالات الخلايا المحفوظة بالتبريد على ثلج جاف في عبوات معزولة وموثوقة مع مبرد كافٍ للحفاظ على درجة حرارة -78 درجة مئوية تقريبًا طوال فترة النقل. عند الاستلام، افحص الحاوية على الفور وانقل القوارير دون تأخير إلى المخزن المناسب. |
| ظروف التخزين | للحفظ طويل الأمد، ضع القوارير في نيتروجين سائل في مرحلة البخار عند درجة حرارة تتراوح بين -150 و -196 درجة مئوية تقريباً. يُقبل التخزين عند درجة حرارة -80 درجة مئوية فقط كخطوة مؤقتة قصيرة قبل النقل إلى النيتروجين السائل. |
مراقبة الجودة / الملف الوراثي / HLA
| العقم | يُستبعد التلوث بالميكوبلازما باستخدام كل من المقايسات القائمة على تفاعل البوليميراز المتسلسل (PCR) وطرق الكشف عن الميكوبلازما القائمة على الإنارة. ولضمان عدم وجود تلوث بكتيري أو فطري أو خميرة يتم إخضاع مزارع الخلايا للفحص البصري اليومي. |
|---|
شهادة التحليل (CoA)
| رقم القطعة | نوع الشهادة | التاريخ | رقم الكتالوج |
|---|---|---|---|
| 300665-240423P1 | شهادة التحليل | 26. Mar. 2026 | 300665 |
اتفاقية نقل المواد
إذا كنت تنوي استخدام خطوط الخلايا Cytion حصريًا لأغراض البحث الداخلي في موقع بحثي واحد، يرجى ملء وتوقيع اتفاقية نقل المواد (MTA) الخاصة بنا وإرسالها مع طلبك.
لأي تطبيقات تجارية - بما في ذلك على سبيل المثال لا الحصر الأعمال مقابل أجر، واختبارات مراقبة الجودة، وإطلاق المنتجات، والاستخدام التشخيصي، أو الدراسات التنظيمية - يرجى ملء نموذج الاستخدام المقصود حتى نتمكن من إعداد اتفاقية مناسبة ومصممة خصيصًا لمشروعك.
يرجى ملاحظة: تنطبق اتفاقية نقل المواد (MTA) على سلالات خلوية معينة فقط. إذا ظهر هذا الإشعار ووثيقة اتفاقية نقل المواد (MTA) على صفحة المنتج، فإن الاتفاقية تكون سارية. بالنسبة للسلالات الخلوية التي لا تشملها اتفاقية نقل المواد (MTA)، لن تظهر أي إشارة إلى الاتفاقية. اتفاقية نقل المواد (MTA) غير صالحة للعملاء في الأمريكتين أو الصين أو تايوان. يرجى الاتصال بكياننا في الولايات المتحدة للحصول على الاتفاقية المناسبة.
