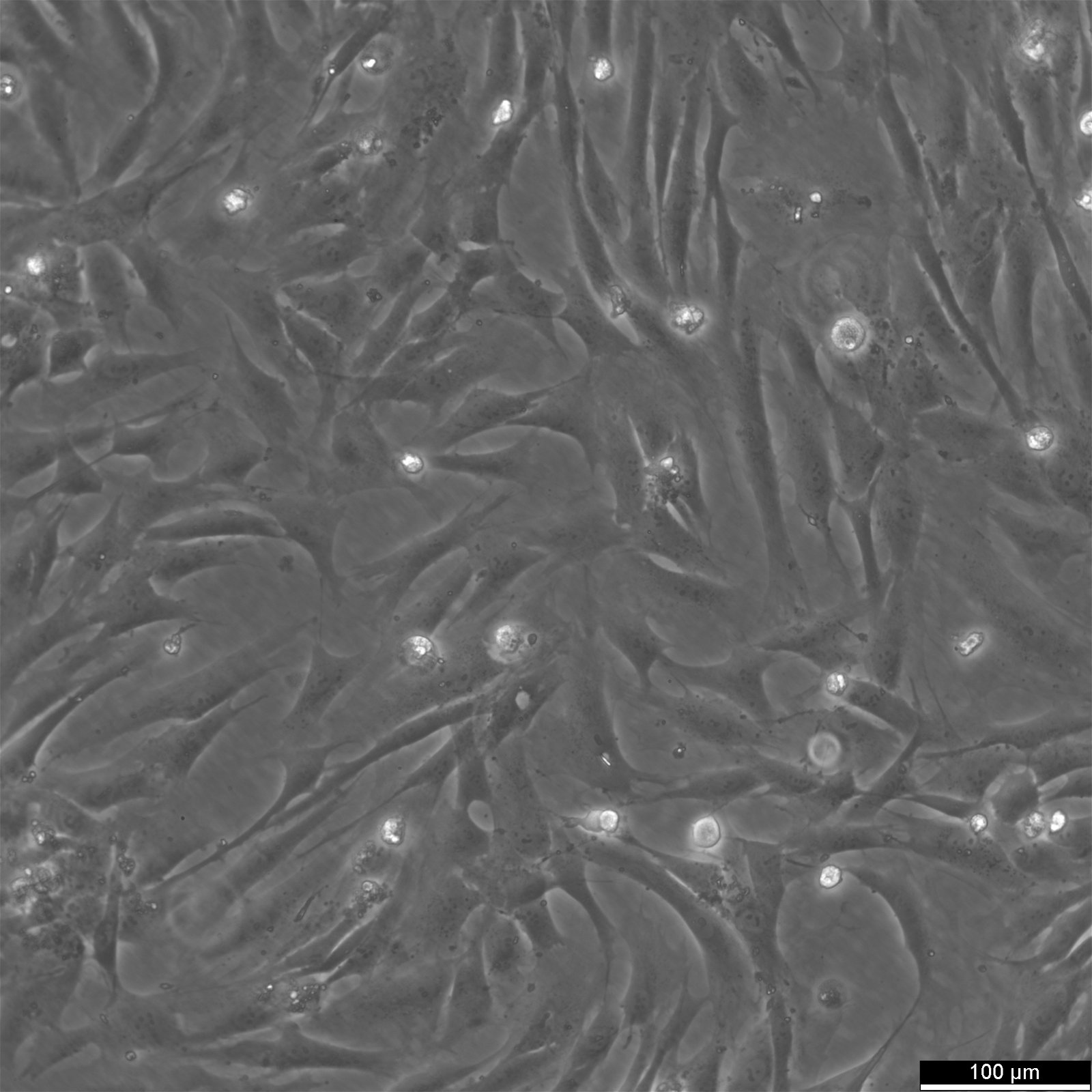
الخلايا الأولية البشرية
توفر Cytion مجموعة مختارة من الخلايا الأولية البشرية المستمدة من أنسجة ومتبرعين متنوعين. تم تصميم هذه النماذج ذات الصلة الفسيولوجية لدعم البحوث التحويلية واختبارات السمية والطب التجديدي والدراسات المتقدمة في المختبر. يتم تحضير كل مزرعة في ظروف خاضعة للرقابة وتخضع لرقابة صارمة على الجودة لضمان هويتها وتعقيمها وأدائها المتسق.
نماذج ذات صلة فسيولوجية للبحوث المتقدمة
تتضمن مجموعة الخلايا الأولية لدينا مجموعات من الخلايا البطانية والظهارية والليفية والخلوية الجذعية من أنسجة بشرية متعددة. تحافظ هذه النماذج على الخصائص الوظيفية الرئيسية للأنسجة التي نشأت منها، مما يوفر أنظمة موثوقة لنمذجة الأمراض وفحص الأدوية وتطبيقات هندسة الأنسجة.
ما هي الخلايا الأولية البشرية؟
الخلايا الأولية هي أنقى تمثيل للأنسجة الخاصة بها. يتم عزلها من الأنسجة ومعالجتها بحيث يمكن أن تنشأ في بيئة مستنبتة في ظروف مثالية. وهي تحاكي بشكل أكبر الحالة في الجسم الحي وتُظهر فسيولوجيا طبيعية لأنها مشتقة من الأنسجة بدلاً من تعديلها. ولهذا السبب، يمكن أن تكون بمثابة نماذج مفيدة للأبحاث في علم الأدوية الخلوية وعلم السموم وعلم وظائف الأعضاء (بما في ذلك دراسات الأيض والشيخوخة ونقل الإشارات). ضع في اعتبارك أن الخلايا الأولية أكثر صعوبة في الاستزراع والحفاظ عليها من خط الخلايا المستمر لأن عمرها الافتراضي أقصر وستتوقف عن الانقسام (أو الشيخوخة) بعد عدد معين من الانقسامات الخلوية. تتعقد دراسات مسارات الإشارات الخلوية بسبب التباين المتأصل في الخلايا الأولية التي يتم الحصول عليها من المتبرعين ومن خلال ممارسات الزراعة الفرعية. قبل البدء بدراسات الإشارات، غالبًا ما يجري الباحثون فحصًا لتحديد ما إذا كانت الخلايا تستجيب للمحفزات الشائعة الاستخدام أم لا. لتجنب إهدار الوقت والمال، يمكن تحفيز الخلايا الأولية لتنشيط مسارات الإشارات الرئيسية قبل فحصها.
لماذا استخدام الخلايا الأولية البشرية؟
تُستخدم خطوط الخلايا الخالدة بشكل شائع كمقايسة للخلايا. على الرغم من اعتراف العلماء بأن التغيرات البيولوجية الناتجة عن خطوط الخلايا قد تكون ضارة في دراسة أهميتها الفسيولوجية. يحسّن استخدام الخلايا الأولية البشرية من القيمة الفسيولوجية للبيانات التي يتم الحصول عليها من خلال مزارع الخلايا، ويُنظر إليها بشكل متزايد على أنها مهمة لدراسة العمليات البيولوجية وتطور الأمراض وتطوير الأدوية.
تُستخدم الخلايا الأولية البشرية على نطاق واسع في الدراسات المختبرية للتواصل بين الخلايا وداخل الخلايا، وبيولوجيا النمو، والآليات الكامنة وراء السرطان، ومرض باركنسون، ومرض السكري، من بين العديد من مجالات البحوث البيولوجية قبل السريرية والاستقصائية الأخرى. لطالما استخدم الباحثون خطوط الخلايا غير الخالدة لدراسة وظيفة الأنسجة؛ ومع ذلك، قد لا تكون خطوط الخلايا ذات الطفرات الواضحة والتشوهات الكروموسومية بدائل جيدة للخلايا الطبيعية وتطور المرض في مراحله المبكرة. يمكن الآن التوصل إلى نموذج أكثر دقة لنوع معين من خلايا الأنسجة باستخدام خلايا بشرية أولية معزولة من ذلك النسيج ومحفوظة في وسائط ومكملات زراعة الخلايا الأولية.
ما هي زراعة الخلايا الأولية؟
بدلاً من استخدام سلالات الخلايا الخالدة، تتضمن زراعة الخلايا الأولية زراعة خلايا مباشرة من كائن حي متعدد الخلايا خارج الجسم. ويوجد اعتراف قانوني في بعض البلدان، مثل المملكة المتحدة، بحقيقة أن مزارع الخلايا الأولية أكثر تمثيلاً للأنسجة في الجسم الحي من خطوط الخلايا. ومع ذلك، تحتاج الخلايا الأولية إلى الركيزة والمغذيات المناسبة للنمو، وبعد عدد معين من الانقسامات، تتطور إلى نمط ظاهري شيخوخة يجعلها تتوقف عن الانقسام بشكل دائم. هذان العاملان يحفزان إنشاء خطوط الخلايا. يمكن زراعة كل من الخلايا الأولية غير الخالدة بشكل طبيعي (مثل خلايا هيلا) والخلايا الأولية غير الخالدة اصطناعيًا (مثل خلايا HEK) إلى أجل غير مسمى في مزرعة خلوية.
الخلايا الأولية البشرية حسب أنواع الأنسجة
تعتبر الخلايا الظهارية والخلايا الليفية والخلايا الكيراتينية والخلايا الصباغية والخلايا البطانية والخلايا العضلية والخلايا المناعية والخلايا الجذعية مثل الخلايا الجذعية الوسيطة من بين الخلايا الأولية البشرية الأكثر استخدامًا في الدراسة العلمية. بادئ ذي بدء، تكون المستنبتات غير متجانسة (تمثل مزيجًا من أنواع الخلايا الموجودة في الأنسجة)، ولا يمكن الاحتفاظ بها حية في المختبر إلا لفترة زمنية محددة. التحويل هو عملية في المختبر تسمح بالتلاعب بالخلايا الأولية البشرية لزراعات فرعية غير محدودة. يمكن أن يحدث التحول بشكل طبيعي، أو يمكن تحفيزه بواسطة مواد كيميائية أو فيروسات. بعد الخضوع للتحول الجيني، يمكن أن تنقسم المزرعة الأولية إلى أجل غير مسمى إلى سلالة خلايا ثانوية خالدة إذا ما أُعطيت ما يكفي من العناصر الغذائية والمساحة.
الخلايا البطانية
إن علاج السرطان والتئام الجروح وأبحاث الإشارات الخلوية والفحص عالي الإنتاجية وعالي المحتوى وفحص السموم ليست سوى بعض المجالات التي يمكن أن تستفيد من استخدام الخلايا البطانية الأولية كأداة بحثية.
الخلايا الكيراتينية
تلعب الخلايا الكيراتينية، المشتقة من بشرة جلد الإنسان البالغ أو قلفة حديثي الولادة، دوراً حاسماً في دراسة الأمراض الجلدية مثل الصدفية والسرطان.
الخلايا الظهارية
أثبتت الخلايا الظهارية الأولية، بدءاً من دراسات السرطان ووصولاً إلى الدراسات السمية أنها موارد لا تقدر بثمن لنمذجة الدفاعات الطبيعية للجسم.
الخلايا الليفية
إن تحفيز الخلايا الجذعية متعددة القدرات (iPS) ودراسة التئام الجروح ليست سوى عدد قليل من الاستخدامات العديدة للخلايا الليفية الأولية.
الخلايا المناعية
الخلايا أحادية النواة في الدم المحيطي، أو اختصاراً PBMC، هي خلايا أحادية النواة في الدم ذات نواة خلية مستديرة. وهي تشمل بشكل أساسي الخلايا اللمفاوية والخلايا الأحادية النواة التي تقوم بوظائف مهمة في سياق الاستجابة المناعية. وغالباً ما تُستخدم خلايا الدم المحيطية أحادية النواة لتشخيص حالات العدوى أو للكشف عن الحماية المحتملة من التطعيم. وغالباً ما تكون النظرة الثاقبة للاستجابة المناعية الخلوية التي تتوسطها الخلايا التائية حاسمة.
الخلايا الصبغية
تُعد الخلايا الصباغية، وهي خلايا الجلد المتخصصة التي تنتج صبغة الميلانين، مفيدة كنماذج للبحث في مواضيع مثل التئام الجروح والسمية والورم الميلانيني واستجابة الجلد للأشعة فوق البنفسجية (UV) والأمراض الجلدية ومستحضرات التجميل.
الخلايا الجذعية
تمتلك الخلايا الجذعية القدرة على التمايز إلى مجموعة متنوعة من أنواع الخلايا. ونظراً لقدرتها على التمايز، فإنها توفر فرصاً جديدة لنمذجة الأنسجة البشرية والحالات الصحية.
الخلايا الجذعية الوسيطة
يمكن الحصول على الخلايا الجذعية الوسيطة اللُّحمية الوسيطة، والمعروفة أيضاً باسم الخلايا الجذعية اللحمية الوسيطة، من مصادر بشرية مختلفة مثل نخاع العظم والدهون (الأنسجة الدهنية) وأنسجة الحبل السري (هلام وارتون) والسائل الأمنيوسي (السائل المحيط بالجنين) ويمكن توسيعها في المختبر. تتمتع هذه الخلايا الجذعية اللحمية البالغة بالقدرة على التطور إلى مجموعة متنوعة من أنواع الخلايا. وتشمل بعض أنواع هذه الخلايا خلايا العظام وخلايا الغضاريف وخلايا العضلات والخلايا العصبية وخلايا الجلد وخلايا القرنية.
خلايا العضلات الملساء
داخل الأعضاء المجوفة، تُبطّن خلايا العضلات الملساء الأولية (SMCs) داخل الأعضاء وتتوسط الانقباض. وبالإضافة إلى السرطان والأمراض الأخرى، يمكن استخدام خلايا العضلات الملساء الأولية لنمذجة التليف الناتج عن ارتفاع ضغط الدم.
الخلايا الأولية وخطوط الخلايا
إما عن طريق الطفرة التلقائية، كما هو الحال في خطوط الخلايا السرطانية المتحولة، أو من خلال التغيير المتعمد، كما هو الحال في الإنتاج الاصطناعي للجينات السرطانية، اكتسبت خطوط الخلايا المستمرة القدرة على التكاثر إلى ما لا نهاية (خالدة). وكقاعدة عامة، تعتبر خطوط الخلايا المستمرة أكثر موثوقية وملاءمة للتعامل معها من الخلايا الأولية. ويمكن أن تتوسع إلى أجل غير مسمى وتوفر إمكانية الوصول السريع إلى البيانات الأساسية. ينطوي استخدام خطوط الخلايا المستمرة على بعض القيود، بما في ذلك حقيقة أنها معدلة وراثياً/متحولة وراثياً، مما قد يغير السمات الفسيولوجية ولا يتطابق مع الحالة في الجسم الحي، ويمكن أن يتغير ذلك مع مرور الوقت مع مرور الوقت مع مرور الوقت مع مرور فترة طويلة من الزمن.
التقدم في زراعة الخلايا الأولية
تشتهر الخلايا الأولية بصعوبة التعامل معها. ومع ذلك، أصبحت هذه العملية أسهل من أي وقت مضى بفضل التطورات في زراعة الخلايا الأولية، وتوافر الخلايا الأولية التجارية مع بروتوكولات محسنة بالكامل، وتقنيات التحليل الجديدة التي تتطلب مدخلات أقل.
ويعتبر التحول من زراعة الخلايا ثنائية الأبعاد إلى زراعة الخلايا ثلاثية الأبعاد علامة فارقة في هذا المجال. قد يتم إضعاف البنية الخاصة بالأنسجة والتفاعلات بين الخلايا والخلايا والإشارات الميكانيكية/البيوكيميائية الحيوية في مزرعة ثنائية الأبعاد. وبالتالي، هناك سقف للقيمة البيولوجية لهذه المزارع.
من ناحية أخرى، تتيح مزرعة الخلايا ثلاثية الأبعاد للخلايا التمدد والتفاعل مع إطار خارج خلوي ثلاثي الأبعاد. وهذا يسمح للخلايا بالتفاعل مع بعضها البعض ومع المصفوفة خارج الخلية، مما يجعل المزارع ثلاثية الأبعاد أكثر ملاءمة من الناحية الفسيولوجية. وقد جعلت دقة هذه الطريقة في التنبؤ بالاستجابات في الجسم الحي من هذه الطريقة ثورية في مجالات مثل اكتشاف الأدوية وتطويرها. ولهذا السبب، توفر التقنيات الحديثة، مثل الخلايا العضوية المشتقة من المرضى والأعضاء على رقاقة، نماذج سياقية للغاية لفحص الأدوية وتطويرها.
يُعتبر توليد الخلايا الأولية عنق الزجاجة في المستنبتات الأولية. وعادة ما تكون هناك حاجة إلى حجم أكبر من الأنسجة للتغلب على هذه المشكلة، وهو ما قد يكون من الصعب تحقيقه. ومع ذلك، توفر الحساسية التحليلية المحسنة وسيلة للمضي قدمًا. على سبيل المثال، يتم تقليل الحاجة إلى زراعة كميات كبيرة من الخلايا الأولية باستخدام تقنية الخلية الواحدة، والتي تشمل التسلسل والنشاف الغربي وقياس الكتلة الخلوية.
آفاق واعدة لزراعة الخلايا الأولية
يتم التخفيف من الصعوبات العامة لزراعة الخلايا الأولية من خلال التقدم التكنولوجي. وفي المقابل، تحل هذه الطريقة بسرعة محل الطرق الأخرى باعتبارها المعيار الذهبي في دراسة وممارسة البيولوجيا الخلوية والجزيئية. ومن المتوقع أن يستفيد تصنيع اللقاحات، واستبدال الأعضاء، والعلاجات بالخلايا الجذعية، وأبحاث السرطان، وغير ذلك الكثير من التطورات المستمرة في زراعة الخلايا الأولية.
نصائح وحيل زراعة الخلايا الأولية
احتياجات توسيع الخلايا
الطريقتان الأكثر شيوعًا لزراعة الخلايا الأولية هما في معلق أو على سطح (ثنائي الأبعاد). تستطيع بعض الخلايا أن تطفو بحرية في مجرى الدم دون أن تلتصق بسطح (على سبيل المثال تلك المستمدة من الدم المحيطي). وقد تم تصميم سلالات خلوية مختلفة لتزدهر في مزارع معلقة حيث يمكن أن تصل إلى كثافات لا يمكن تحقيقها في ظروف نمو ثنائية الأبعاد. وتسمى الخلايا الأولية التي تحتاج إلى التثبيت لتنمو في المختبر بالخلايا الملتصقة وتشمل تلك الموجودة في الأنسجة الصلبة. ولتحسين خصائص الالتصاق وتوفير إشارات أخرى مطلوبة للنمو والتمايز، عادةً ما يتم استزراع هذه الخلايا في وعاء بلاستيكي مسطح غير مطلي ولكن في بعض الأحيان يتم زرعها في ناقل دقيق. قد يكون هذا الخيار الأخير مغلفًا ببروتينات المصفوفة خارج الخلية (مثل الكولاجين واللامينين). تتكون الوسائط المستخدمة في زراعة الخلايا من وسط أساسي تم استكماله بعوامل النمو والسيتوكينات المناسبة. الحاضنة الخلوية هي نوع خاص من الحاضنات المختبرية المستخدمة لزراعة الخلايا والحفاظ عليها عند درجة حرارة محددة وخليط غازي معين (عادةً 37 درجة مئوية، و5% من ثاني أكسيد الكربون لخلايا الثدييات). واعتماداً على نوع الخلية التي تتم زراعتها، يمكن أن تكون الظروف المثلى مختلفة جداً. واعتمادًا على أنواع الخلايا التي تتم زراعتها، سيكون لوسط النمو الأمثل مزيج فريد من العوامل، بما في ذلك على سبيل المثال لا الحصر الأس الهيدروجيني وتركيز الجلوكوز وعوامل النمو ووجود مغذيات أخرى.
تُعد المضادات الحيوية في وسط النمو ضرورية أثناء إنشاء المزرعة الأولية لمنع التلوث من الأنسجة المضيفة. وتتميز بعض نظم المضادات الحيوية بمزيج من الجنتاميسين والبنسلين والستربتومايسين والأمفوتريسين ب. ومع ذلك، لا يُنصح باستخدام المضادات الحيوية لفترة طويلة من الزمن، لأن بعض الكواشف (مثل الأمفوتريسين ب) قد تكون سامة للخلايا على المدى الطويل.
وتمر معظم الخلايا الأولية بمرحلة الشيخوخة وتتوقف عن الانقسام بعد عدد معين من تضاعف عدد الخلايا، مما يجعل من الضروري إبقاؤها على قيد الحياة بعد العزل. تتطلب قابلية بقاء الخلايا على المدى الطويل تقنيات زراعة الخلايا الخبيرة وظروف الاستزراع المثالية (بما في ذلك الوسط المناسب، ودرجة الحرارة المناسبة، وخليط الغازات المناسب، والأس الهيدروجيني المناسب، والتركيز المناسب لعوامل النمو، ووجود المغذيات، ووجود الجلوكوز). ونظرًا لأن العديد من عوامل النمو المستخدمة لتكملة الوسائط يتم الحصول عليها من دم الحيوانات (المكونات المشتقة من الدم تنطوي على احتمالية التلوث)، فمن المستحسن تقليل استخدامها أو تجنبها تمامًا. ومن المهم أيضاً استخدام تقنية معقمة.
المزرعة الفرعية والصيانة
عندما تلتصق الخلايا المعزولة بسطح طبق المزرعة فإن ذلك يمثل بداية مرحلة الصيانة. ويحدث الالتصاق عادةً بعد 24 ساعة من بدء الزراعة. يجب أن تتم زراعة الخلايا تحت المزرعة عندما تصل إلى نسبة معينة من التماسك وتتكاثر بنشاط. نظرًا لأن الخلايا بعد التمايز قد تخضع للتمايز وتظهر تكاثرًا أبطأ بعد مرورها، فمن الأفضل إجراء زراعة فرعية للخلايا الأولية قبل أن تصل إلى نسبة 100٪ من التمايز.
تحافظ المزرعة الفرعية في وسائط جديدة على النمو الأسي للخلايا المعتمدة على الرسو. تؤدي الزراعة الفرعية للطبقات الأحادية إلى تعطيل التفاعلات بين الخلايا وداخل الخلايا. تُستخدم تركيزات منخفضة من الإنزيمات المحللة للبروتين، مثل التربسين/إيدتا، لاستخراج الخلايا الأولية الملتصقة من الطبقات الأحادية أو الأنسجة. بعد فصلها وتخفيفها في محلول أحادي الخلية، يتم عد الخلايا ونقلها إلى حاويات مزرعة جديدة لإعادة التصاقها وتكاثرها.
الحفظ بالتبريد والاستعادة
يحفظ الحفظ بالتبريد الخلايا الحية عن طريق تجميدها في درجات حرارة منخفضة. يمنع حفظ الخلايا الأولية البشرية بالتبريد وإذابتها بالتبريد موت الخلايا وتلفها أثناء التخزين والاستخدام. تُحفظ الخلايا الأولية البشرية بالتبريد باستخدام DMSO أو الجلسرين (عند درجة الحرارة الصحيحة وبمعدل تجميد مضبوط). يجب أن تكون عملية التجميد تدريجية، عند درجة حرارة -1 درجة مئوية كل دقيقة، لمنع تكون بلورات الثلج. يتطلب التخزين طويل الأمد نيتروجين سائل (-196 درجة مئوية) أو درجات حرارة أقل من -130 درجة مئوية.
إن غمر الخلايا المجمدة في حمام مائي بدرجة حرارة 37 درجة مئوية لمدة دقيقة إلى دقيقتين تقريباً هو كل ما يتطلبه الأمر لإذابة الخلايا المحفوظة بالتبريد. يجب عدم طرد الخلايا الأولية البشرية بالطرد المركزي بعد ذوبان الجليد من الثلاجة (لأنها حساسة للغاية للتلف أثناء التعافي من الحفظ بالتبريد). وهي مناسبة لطرح الخلايا مباشرةً بعد إذابة التجميد مباشرةً، كما أنها تعزز التعلق في المزارع خلال الـ 24 ساعة الأولى بعد الطرح. 1 بعد أن تعلق الخلايا الأولية المحفوظة بالتبريد، يجب إزالة الوسائط المستهلكة (حيث إن DMSO ضار بالخلايا الأولية وقد يتسبب في انخفاض قابلية البقاء بعد الذوبان).