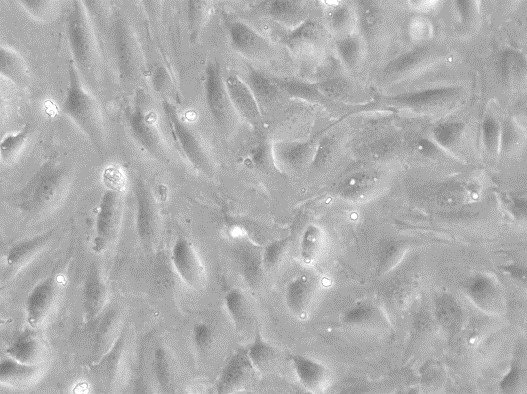
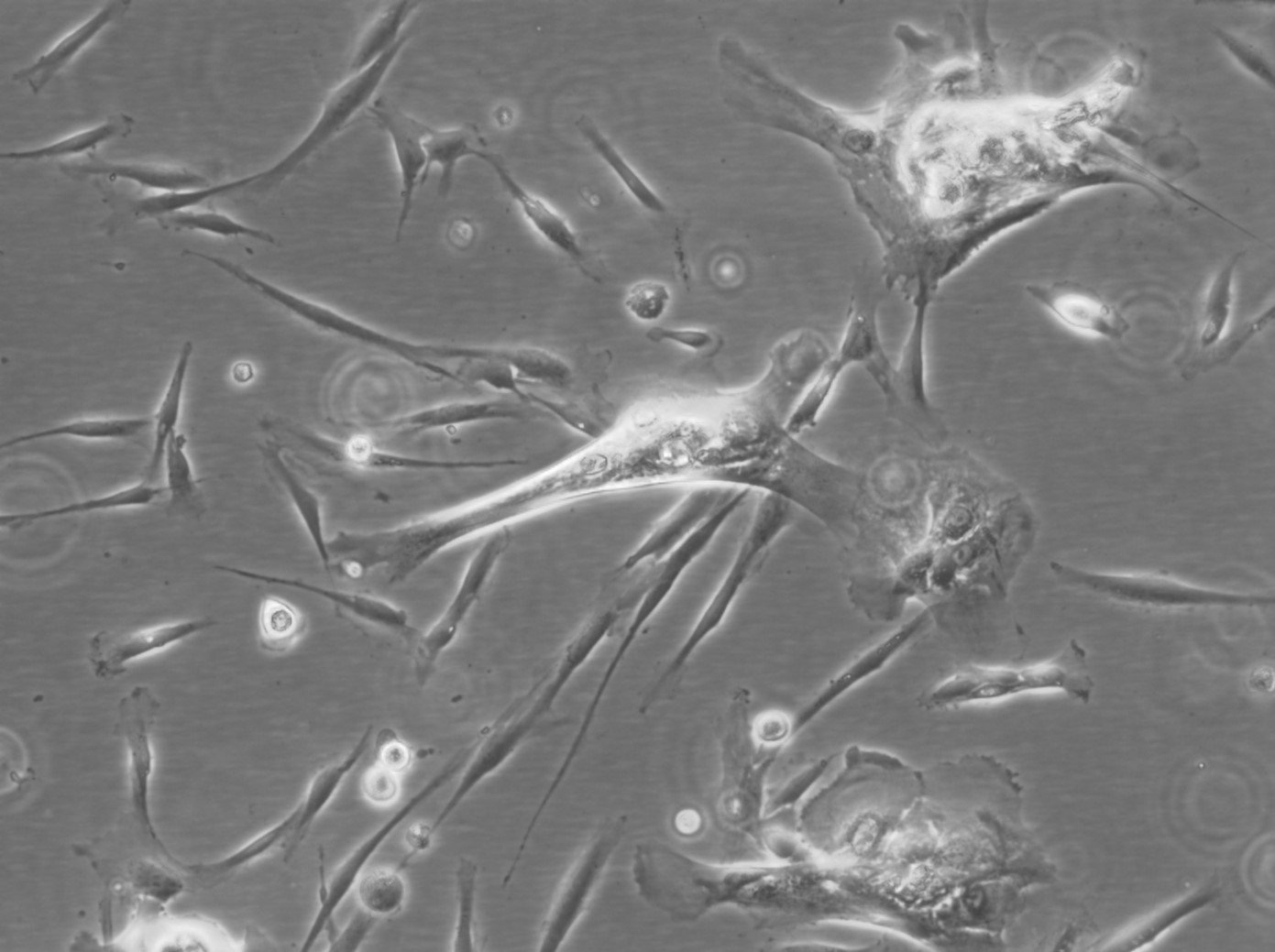
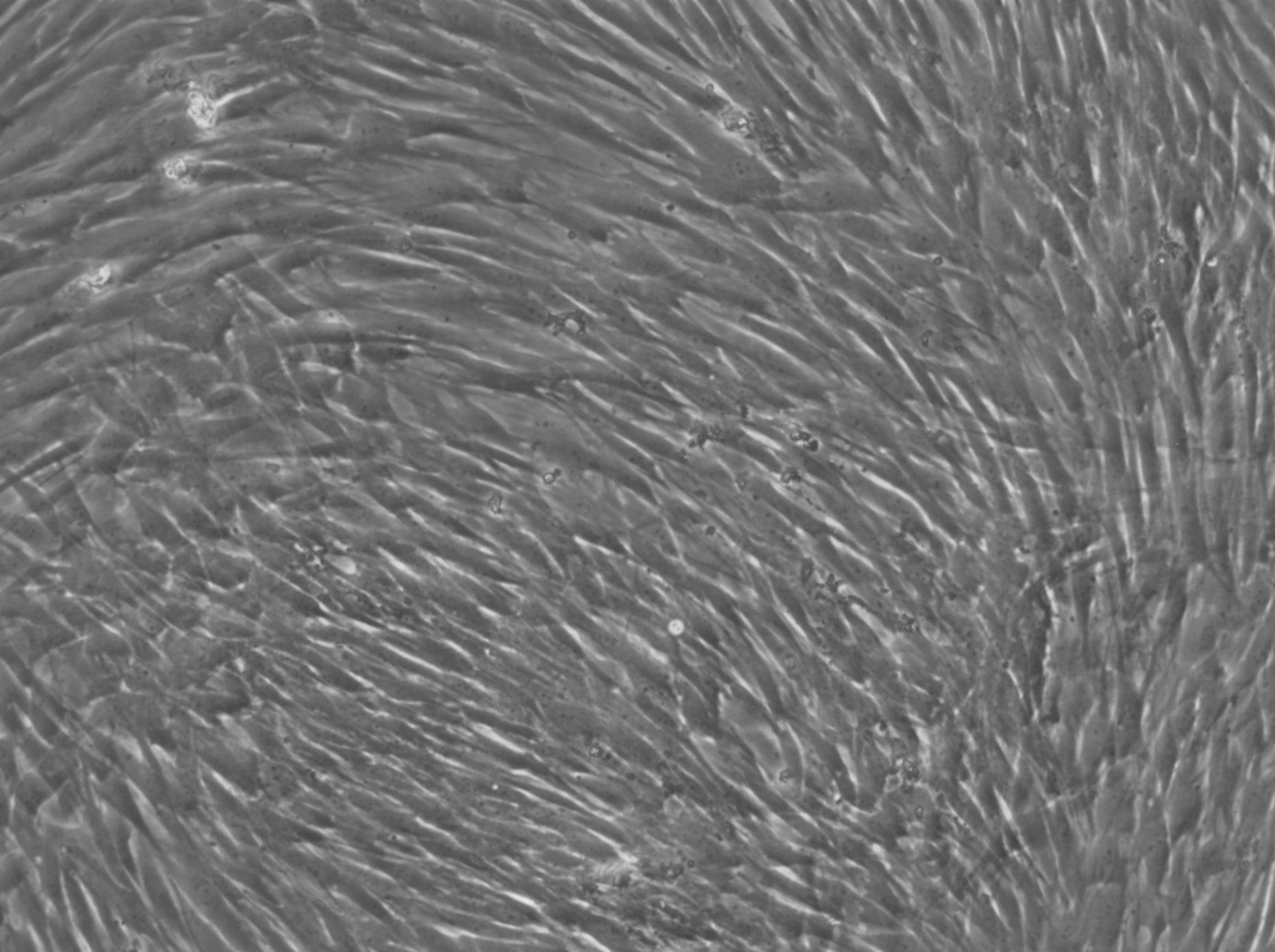
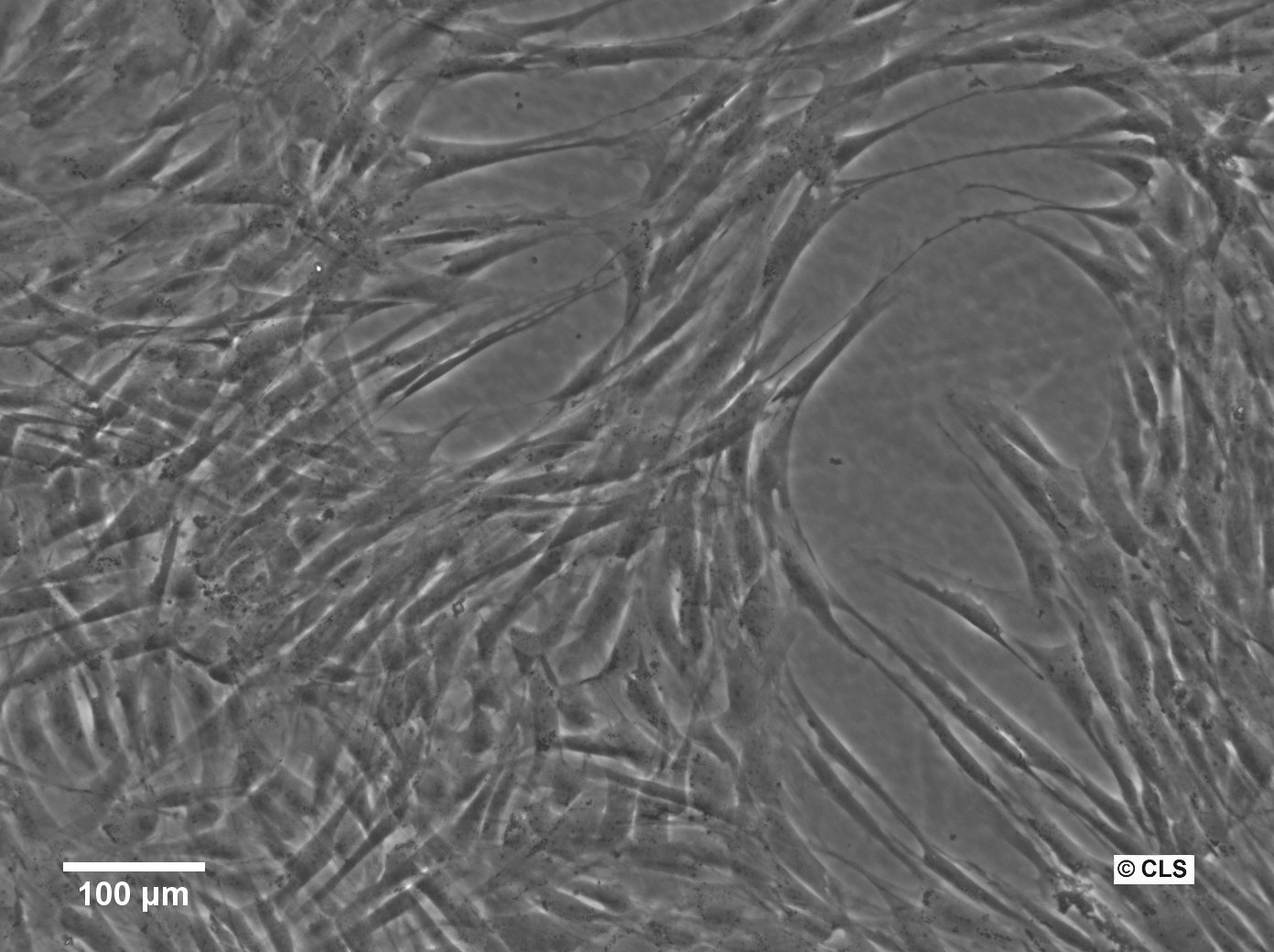
Ludzkie mezenchymalne komórki macierzyste - szpik kostny (HMSC-BM)

























690,00 €*
Produkty są wysyłane w stanie zamrożonym w suchym lodzie w probówkach kriogenicznych. Każda probówka kriogeniczna zawiera zazwyczaj 5 × 10 5 komórek dla pierwotnych linii komórkowych (szczegółowe informacje znajdują się w certyfikacie analizy partii).
Informacje ogólne
| Opis | Ludzkie mezenchymalne komórki macierzyste pochodzące ze szpiku kostnego (HMSC-BM) stanowią solidne i wszechstronne narzędzie do badań in vitro. Te multipotencjalne mezenchymalne komórki macierzyste (MSC) posiadają wyjątkową zdolność do samoodnawiania się i różnicowania w szerokie spektrum typów komórek, w tym adipocyty, osteoblasty i chondrocyty. Potencjał HMSC-BM do różnicowania się w te trzy kluczowe linie komórkowe został dobrze udokumentowany, co czyni je nieocenionymi w badaniach skupiających się na medycynie regeneracyjnej, inżynierii tkankowej i szlakach różnicowania komórkowego. Komórki MSC są hodowane w rygorystycznych warunkach, co zapewnia ich multipotencjalność i wysoką żywotność po rozmrożeniu. Jedną z cech wyróżniających HMSC-BM w porównaniu z MSC pochodzącymi z innych źródeł, takich jak tkanka tłuszczowa lub pępowina, jest ich doskonała zdolność do różnicowania osteogenicznego. Dzięki temu są one szczególnie przydatne w biologii kości i badaniach ortopedycznych, gdzie kluczowe znaczenie ma zrozumienie mechanizmów molekularnych regulujących tworzenie i naprawę kości. Ponadto komórki HMSC-BM wykazują silny profil immunomodulacyjny, co czyni je doskonałym modelem do badania interakcji immunologicznych i odpowiedzi zapalnych. Te wyjątkowe cechy sprawiają, że komórki HMSC-BM są preferowanym wyborem do badań przedklinicznych dotyczących mikrośrodowiska szpiku kostnego, hematopoezy i patofizjologii chorób związanych ze szpikiem kostnym. Każda krioprobówka HMSC-BM zawiera co najmniej 1 x 106 komórek, których żywotność wynosi od 92% do 95%, zgodnie z wynikiem testu wykluczenia barwnikiem błękitu trypanowego. Komórki te pochodzą ze szpiku kostnego pobranego od zdrowych dorosłych dawców, którzy wyrazili świadomą zgodę na pobranie. Aby zapewnić najwyższe standardy, każda partia poddawana jest rygorystycznym testom kontroli jakości w celu oceny identyfikacji komórek, czystości, mocy i żywotności. Te dokładne testy gwarantują, że MSC spełniają surowe kryteria, dzięki czemu nadają się do szerokiego zakresu zastosowań badawczych, w tym badań z zakresu biologii komórkowej, odkrywania leków i badania reakcji komórek na różne bodźce. Komórki te nie są przeznaczone do zastosowań terapeutycznych ani in vivo, a ich wykorzystanie ogranicza się do celów badawczych w kontrolowanym środowisku laboratoryjnym. |
|---|---|
| Organizm | Człowiek |
| Tkanka | Szpik kostny |
| Zastosowania | Testowanie leków, medycyna regeneracyjna, badania nad chorobami |
Charakterystyka
| Wiek | Prosimy o zapytanie |
|---|---|
| Płeć | Prosimy o zapytanie |
| Pochodzenie etniczne | Kaukaski |
| Morfologia | Dobrze rozprzestrzeniona wrzecionowata morfologia podobna do fibroblastów przez co najmniej 5 pasaży. Mniej niż 2% komórek wykazuje spontaniczną morfologię podobną do miofibroblastów w każdym pasażu. |
| Typ komórki | Komórki macierzyste |
| Właściwości wzrostu | Adherent |
Dane regulacyjne
| Cytat | Ludzkie mezenchymalne komórki macierzyste szpiku kostnego (HMSC-BM) (numer katalogowy Cytion 300665) |
|---|---|
| Poziom bezpieczeństwa biologicznego | 1 |
| NCBI_TaxID | 9606 |
Dane biomolekularne
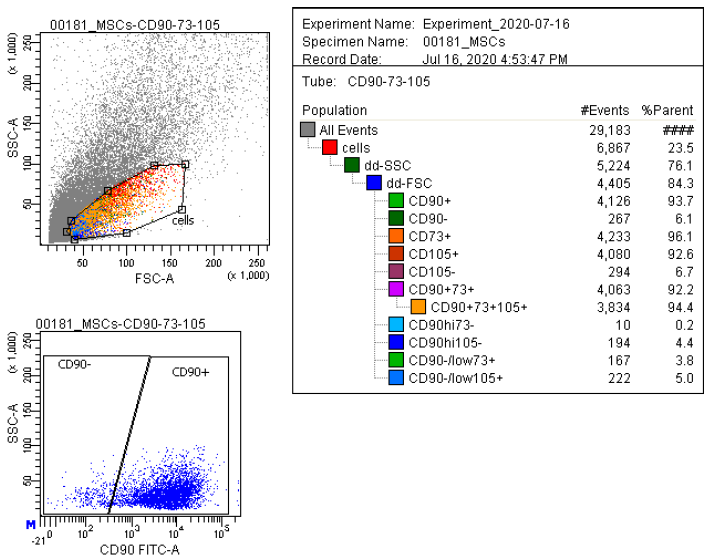
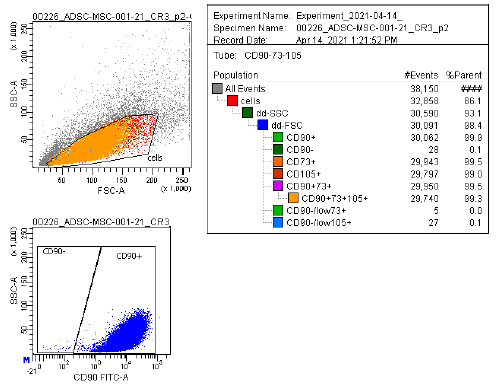
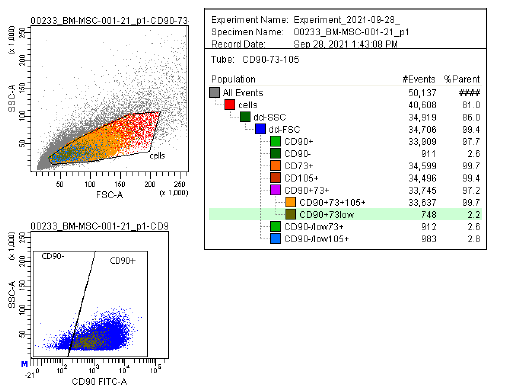
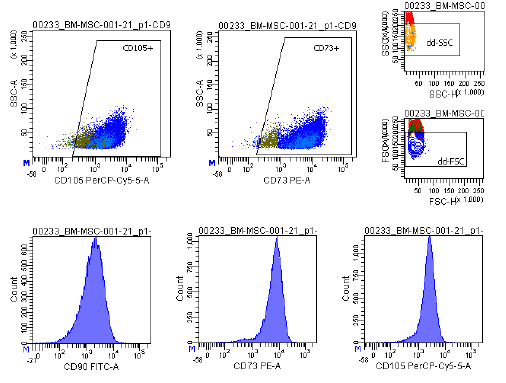
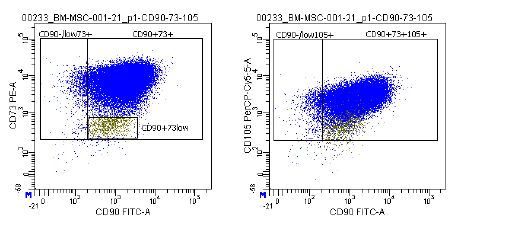
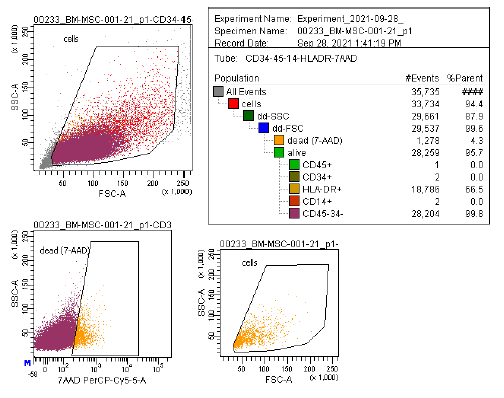
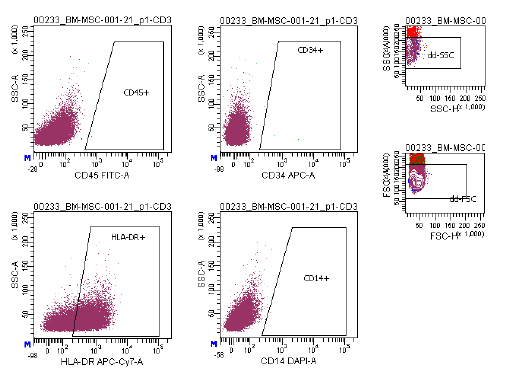
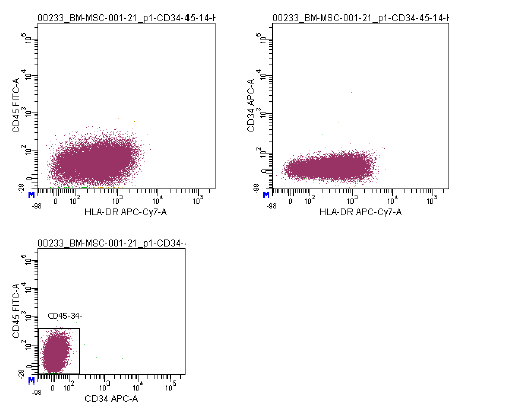
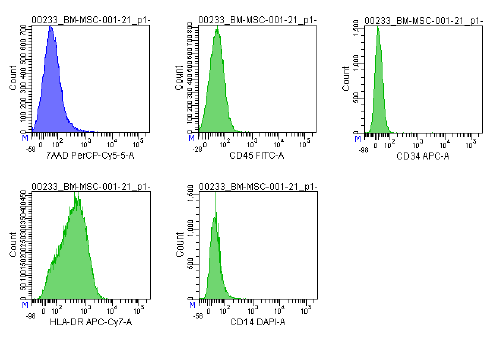
| Ekspresja antygenu | Kompleksowy panel markerów, w tym CD73/CD90/CD105 (pozytywny) i CD14/CD34/CD45/HLA-DR (negatywny), jest wykorzystywany w analizie cytometrii przepływowej do identyfikacji hodowanych MSC (P2-P3) przed kriokonserwacją. Markery te są zalecane przez komitet ISCT MSC. |
|---|---|
| Wirusy | Dawca jest ujemny w kierunku HBV (PCR), Treponema pallidum (PCR) i HIV-1/2 (IFA). Komórki są ujemne w kierunku HBV, HCV, HSV1, HSV2, CMV, EBV, HHV6, Toxoplasma gondii, Treponema pallidum, Chlamydia trachomatis, Ureaplasma urealyticum i Ureaplasma parvum. |
Obsługa
| Podłoże hodowlane | Alpha MEM, w: 2,0 mM stabilnej glutaminy, w/o: Rybonukleozydy, w/o: Deoksyrybonukleozydy, w: 1.0 mM Pirogronian sodu, w: 2.2g/L NaHCO3 |
|---|---|
| Suplementy | Uzupełnić pożywkę 10% FBS, 2 ng/ml bFGF |
| Odczynnik dysocjacyjny | Trypsyna-EDTA |
| Subkultury | W przypadku rutynowej hodowli komórek przylegających: Odessać starą pożywkę z przylegających komórek i przemyć je PBS w celu usunięcia pozostałości pożywki. Po odessaniu PBS, dodać odpowiednią objętość roztworu Trypsyna/EDTA w zależności od wielkości naczynia hodowlanego (np. 1 ml dla kolby T25, 3 ml dla kolby T75) i inkubować w temperaturze pokojowej lub 37°C do momentu odłączenia się komórek (5-10 minut). Monitoruj oderwanie pod mikroskopem i delikatnie postukaj w naczynie, jeśli to konieczne, aby uwolnić komórki. Po odłączeniu dodać pełną pożywkę w celu inaktywacji trypsyny/EDTA, delikatnie ponownie zawiesić komórki i przenieść porcję zawiesiny komórek do nowego naczynia hodowlanego zawierającego świeżą pożywkę. Umieść naczynie w inkubatorze ustawionym na 37°C z 5%CO2 i zmieniaj pożywkę co 2-3 dni. |
| Gęstość siewu | 1 do 3 x 104 komórek/cm2 |
| Odnawianie płynów | Pierwsze uzupełnienie płynów po 24 godzinach, a następnie co 2-3 dni. |
| Środek zamrażający | Jako pożywki do kriokonserwacji używamy 80% FBS + 10% pożywki podstawowej + 10% DMSO w celu utrzymania żywotności lub CM-1 (numer katalogowy Cytion 800100) dla lepszej krioprotekcji, zapobiegając niepożądanemu różnicowaniu przy jednoczesnym zachowaniu pluripotencji. |
| Rozmrażanie i hodowla komórek |
|
| Atmosfera inkubacji | 37°C, 5%CO2, nawilżona atmosfera. |
| Powłoka kolby | Brak |
| Procedura zamrażania | Linie komórkowe poddane kriokonserwacji są wysyłane w suchym lodzie w zatwierdzonych, izolowanych opakowaniach z wystarczającą ilością czynnika chłodniczego, aby utrzymać temperaturę około -78°C przez cały czas transportu. Po otrzymaniu przesyłki należy natychmiast sprawdzić pojemnik i bezzwłocznie przenieść fiolki do odpowiedniego miejsca przechowywania. |
| Warunki wysyłki | Linie komórkowe poddane kriokonserwacji są wysyłane w suchym lodzie w zatwierdzonych, izolowanych opakowaniach z wystarczającą ilością czynnika chłodniczego, aby utrzymać temperaturę około -78°C przez cały czas transportu. Po otrzymaniu przesyłki należy natychmiast sprawdzić pojemnik i bezzwłocznie przenieść fiolki do odpowiedniego miejsca przechowywania. |
| Warunki przechowywania | W celu długotrwałego przechowywania należy umieścić fiolki w ciekłym azocie w fazie lotnej w temperaturze od -150 do -196 °C. Przechowywanie w temperaturze -80 °C jest dopuszczalne tylko jako krótki etap przejściowy przed przeniesieniem do ciekłego azotu. |
Kontrola jakości / Profil genetyczny / HLA
| Sterylność | Zanieczyszczenie mykoplazmą jest wykluczane przy użyciu zarówno testów opartych na PCR, jak i metod wykrywania mykoplazmy opartych na luminescencji. Aby upewnić się, że nie ma zanieczyszczenia bakteriami, grzybami lub drożdżami, hodowle komórkowe są poddawane codziennym kontrolom wizualnym. |
|---|
Certyfikat analizy (CoA)
| Numer działki | Typ certyfikatu | Data | Numer katalogowy |
|---|---|---|---|
| 300665-240423P1 | Certyfikat analizy | 26. Mar. 2026 | 300665 |
Umowa transferu materiałów
Jeśli zamierzają Państwo wykorzystywać linie komórkowe Cytion wyłącznie do badań wewnętrznych w jednym ośrodku badawczym, prosimy o wypełnienie i podpisanie naszej umowy o transferze materiałów (MTA) oraz przesłanie jej wraz z zamówieniem.
W przypadku wszelkich zastosowań komercyjnych — w tym między innymi prac wykonywanych za wynagrodzeniem, testów kontroli jakości, wprowadzania produktów na rynek, zastosowań diagnostycznych lub badań regulacyjnych — prosimy o wypełnienie formularza przeznaczenia, abyśmy mogli przygotować umowę dostosowaną do Państwa projektu.
Uwaga: Umowa MTA dotyczy tylko niektórych linii komórkowych. Jeśli ta informacja i dokument MTA pojawiają się na stronie produktu, umowa ma zastosowanie. W przypadku linii komórkowych nieobjętych umową MTA nie będzie wyświetlana żadna informacja o umowie. Umowa MTA nie obowiązuje klientów z Ameryki, Chin i Tajwanu. Aby otrzymać odpowiednią umowę, skontaktuj się z naszym oddziałem w Stanach Zjednoczonych.
-
Wymagane produkty
Wymagane produkty
Medium zamrażające CM-1 - 50 mlWarianty nośników do kriokonserwacji: 50 mlCytion's Freeze Medium CM-1 to najnowocześniejsza pożywka do kriokonserwacji zaprojektowana w celu zapewnienia najwyższego poziomu żywotności i funkcjonalności komórek po rozmrożeniu. Ta wszechstronna pożywka jest odpowiednia dla szerokiego spektrum typów komórek, w tym zarówno ludzkich, jak i zwierzęcych, co czyni ją niezbędnym narzędziem do różnorodnych zastosowań badawczych. Dzięki starannie zbilansowanej kombinacji krioprotektantów i niezbędnych składników odżywczych, Freeze Medium CM-1 minimalizuje tworzenie się kryształków lodu i stres komórkowy podczas procesu zamrażania, zachowując w ten sposób integralność komórek.
Kluczowe cechy Freeze Medium CM-1 obejmują:
Szeroka kompatybilność: Skuteczny dla szerokiej gamy typów komórek, w tym komórek pierwotnych, komórek macierzystych i ustalonych linii komórkowych.
Wysoka żywotność: Zoptymalizowany w celu maksymalizacji odzysku i żywotności komórek po rozmrożeniu, zapewniając wiarygodne wyniki eksperymentów.
Gotowy do użycia: Wygodnie przygotowany i wysterylizowany do natychmiastowego zastosowania, skracając czas przygotowania i zmniejszając ryzyko zanieczyszczenia.
Zwiększona stabilność: Utrzymuje stałą wydajność w standardowych warunkach kriokonserwacji, zapewniając powtarzalne wyniki.
Długi okres trwałości: CM-1 to zawierająca surowicę, gotowa do użycia pożywka do kriokonserwacji, którą można przechowywać w lodówce przez okres do jednego roku.
Używanie CM-1 do zamrażania komórek
Aby użyć CM-1 do zamrażania zarówno komórek adherentnych, jak i zawiesinowych, należy wykonać następujące kroki
W przypadku komórek przylegających należy je umyć i oddzielić od podłoża hodowlanego. W przypadku komórek w zawiesinie przejdź bezpośrednio do następnego kroku.
Policzyć komórki, aby upewnić się, że mają odpowiednie stężenie.
Odwirować komórki, aby je osuszyć, a następnie ponownie zawiesić w pożywce do zamrażania CM-1.
Przenieś ponownie zawieszone komórki do fiolek.
Użyj metody powolnego zamrażania przed przeniesieniem komórek do długoterminowego przechowywania
Metoda
Opis
Kroki
❄️
Ręczne zamrażanie
Metoda krok po kroku polegająca na stopniowym obniżaniu temperatury w celu zapewnienia żywotności komórek
1️⃣ Umieścić komórki w pożywce do zamrażania w temperaturze 4°C na 40 minut.
2️⃣ Przenieść do zamrażarki o temperaturze -80°C na 24 godziny.
3️⃣ Przechowywać komórki w ciekłym azocie w celu długotrwałego przechowywania
❄️
Korzystanie z Mr. Frosty
Wygodne urządzenie umożliwiające kontrolowane zamrażanie bez zasilania elektrycznego
1️⃣ Przygotować komórki w kriofiolach z pożywką do zamrażania.
2️⃣ Umieścić kriofiole w pojemniku Mr. Frosty.
3️⃣ Przechowywać w temperaturze -80°C przez 24 godziny przed przeniesieniem do ciekłego azotu
❄️
Zamrażarka o kontrolowanej prędkości
Precyzyjna zamrażarka firmy Thermo Fisher lub innych producentów przeznaczona do kontrolowanego obniżania temperatury
1️⃣ Zaprogramuj urządzenie tak, aby stopniowo obniżało temperaturę.
2️⃣ Umieść przygotowane komórki w zamrażarce.
3️⃣ Po cyklu zamrażania przenieś komórki do ciekłego azotu
Przechowywać kriofiole w temperaturze poniżej -130°C lub w ciekłym azocie w celu długotrwałego przechowywania.
Składniki
Zawiera FBS, DMSO, glukozę, sole
Zdolność buforowania: pH = 7,2 do 7,6
Cytion's Freeze Medium CM-1 oferuje niezawodne rozwiązanie do kriokonserwacji, zapewniając wysoką żywotność komórek i funkcjonalność po rozmrożeniu w szerokim zakresie zastosowań badawczych.59,00 €*Roztwór do oddzielania komórek Accutase – 100 mlWarianty: 100 mlRoztwór do oddzielania komórek Accutase z EDTA i czerwienią fenolową – 100 ml
Accutase to gotowy do użycia, sterylnie filtrowany roztwór do oddzielania komórek, zaprojektowany jako delikatna alternatywa dla trypsyny/EDTA do rozdzielania przylegających komórek ssaków ze standardowych plastikowych naczyń do hodowli tkankowej i powierzchni pokrytych powłoką adhezyjną. Łączy on aktywność enzymów proteolitycznych i kolagenolitycznych w zrównoważonym roztworze soli, zapewniając skuteczne, ale kontrolowane rozdzielanie, zachowując białka powierzchniowe komórek oraz wspierając wysoką żywotność po pasażowaniu i szybkie ponowne przyleganie.
Formuła Accutase opiera się na buforowanym roztworze soli fizjologicznej Dulbecco (DPBS) z dodatkiem EDTA i czerwieni fenolowej jako wizualnego wskaźnika pH. Enzymy są pochodzenia nie-ssaczego i nie-bakteryjnego, co sprawia, że Accutase szczególnie dobrze nadaje się do badań nad komórkami macierzystymi, procesów związanych ze szczepionkami oraz wszelkich zastosowań, w których należy zminimalizować zanieczyszczenia pochodzenia zwierzęcego lub mikrobiologicznego. Roztwór ulega samoczynnej inhibicji w temperaturze 37 °C, więc po oddzieleniu komórek nie jest wymagany odczynnik neutralizujący ani pożywka zawierająca surowicę – komórki można przenieść bezpośrednio do świeżej pożywki.
Najważniejsze cechy
Gotowy do użycia 1x sterylnie filtrowany płyn – nie wymaga rozcieńczania ani rekonstytucji
Połączona aktywność enzymów proteolitycznych i kolagenolitycznych zapewnia delikatną dysocjację
Każda partia jest standaryzowana pod kątem określonej aktywności dysocjacyjnej, co zapewnia spójność między partiami
Enzymy pochodzenia nie-ssaczego i nie-bakteryjnego
Samoczynnie hamuje się w temperaturze 37 °C – nie jest potrzebny roztwór neutralizujący
Opracowany na bazie PBS Dulbecco z EDTA
Zawiera czerwień fenolową jako wizualny wskaźnik pH
pH 6,8–7,8
Typowe zastosowania
Accutase delikatnie rozdziela szeroką gamę przylegających i wrażliwych typów komórek, w tym ludzkie embrionalne komórki macierzyste (hESCs), ludzkie indukowane pluripotencjalne komórki macierzyste (iPSCs), komórki macierzyste układu nerwowego, pierwotne neurony oraz rutynowo hodowane linie przylegające, takie jak HeLa, HEK 293, CHO, MDCK, Vero, NIH/3T3, BHK-21 i A549. Typowe zastosowania obejmują:
Rutynową subkulturę i pasażowanie przylegających komórek ssaków
Delikatną dysocjację pojedynczych komórek hESCs, iPSCs i innych wrażliwych linii
Przygotowanie próbek do cytometrii przepływowej i analizy FACS
Analiza markerów powierzchniowych komórek, w przypadku których istotna jest integralność epitopu
Testy migracji, proliferacji i apoptozy komórek
Testy spoczynku komórkowego poprzez pozbawienie surowicy oraz badania transfekcji onkogenów
Testy migracji komórek nowotworowych i komórek grzebienia nerwowego
Zwiększanie skali produkcji w procesach bioreaktorowych
W przypadku rutynowych prac należy zastosować około 10 ml preparatu Accutase na 75 cm2 powierzchni hodowli i inkubować przez 5–10 minut w temperaturze pokojowej. Optymalny czas inkubacji należy określić dla każdej linii komórkowej i nie powinien on przekraczać jednej godziny. Przed dodaniem preparatu należy przepłukać warstwę komórek roztworem soli wolnym od Ca2+/Mg2+, takim jak DPBS bez wapnia i magnezu, w celu usunięcia resztek surowicy i kationów dwuwartościowych.
Postępowanie i przechowywanie
Nieotwartą butelkę należy przechowywać w stanie zamrożonym w temperaturze -15 °C lub niższej. Rozmrażać w temperaturze pokojowej lub przez noc w temperaturze od +2 °C do +8 °C. Nie rozmrażać preparatu Accutase w łaźni wodnej o temperaturze 37 °C, ponieważ podwyższona temperatura zmniejsza aktywność enzymu. Po rozmrożeniu roztwór można przechowywać do 2 miesięcy w temperaturze od +2 °C do +8 °C; nie przechowywać w temperaturze pokojowej. Nie należy wstępnie ogrzewać odczynnika do temperatury 37 °C przed zastosowaniem – należy go dodać bezpośrednio do przemytych komórek w temperaturze pokojowej. W celu zapewnienia długiego okresu przydatności do użycia zaleca się podział na porcje jednorazowego użytku, aby uniknąć powtarzających się cykli rozmrażania. Zawsze należy pracować w warunkach aseptycznych.
Jakość
Wyprodukowany zgodnie z rygorystycznymi normami jakości. Każda partia preparatu Accutase jest filtrowana sterylnie i badana pod kątem sterylności, pH, wyglądu i aktywności dysocjacyjnej w celu zapewnienia spójnej, powtarzalnej wydajności w poszczególnych partiach.
Specyfikacja produktu
Specyfikacja
Szczegóły
Rodzaj produktuOdczynnik do oddzielania/dysocjacji komórek
PojemnośćPłyn przefiltrowany sterylnie, gotowy do użycia
Pojemność100 ml
Stężenie robocze1x (gotowy do użycia)
Aktywność enzymatycznaPołączone działanie proteolityczne i kolagenolityczne
Pochodzenie enzymówNiepochodzące od ssaków i bakterii
Układ buforowyPBS Dulbecco z EDTA
Wskaźnik pHCzerwień fenolowa
Zakres pH6,8 – 7,8
WyglądPrzezroczysty roztwór o barwie od jasnoczerwonej do pomarańczowej
Temperatura przechowywania-15 °C lub niższa
Stabilność po rozmrożeniuDo 2 miesięcy w temperaturze od +2 °C do +8 °C
Zalecana objętość stosowania~10 ml na 75 cm² powierzchni hodowli
Typowy czas inkubacji5–10 minut w temperaturze pokojowej
Warunki transportuZamrożone w suchym lodzie
PrzeznaczenieWyłącznie do celów badawczych i dalszej produkcji
Skład (skład na litr)
Składnik
Stężenie (mg/l)
Sole nieorganiczne
Chlorek sodu (NaCl)8000,00
Wodorofosforan disodowy (Na₂HPO₄)1150,00
Chlorek potasu (KCl)200,00
Dihydrofosforan potasu (KH2PO4)200,00
Inne składniki
EDTA · 4Na (EDTA tetrasodowy)220,00
Czerwień fenolowa3,00
Zastrzeżona mieszanka enzymów (aktywność proteolityczna i kolagenolityczna)1x
Accutase jest zastrzeżonym znakiem towarowym firmy Innovative Cell Technologies, Inc.75,00 €*Roztwór antybiotyku/przeciwgrzybiczy (100x)Przegląd produktów
Pojemność: 100 ml Przechowywanie: ≤-15°C Sterylność: Sterylnie filtrowany
Antibiotic/Antimycotic Solution (100x) to sterylny, gotowy do użycia koncentrat zaprojektowany w celu zmniejszenia ryzyka skażenia mikrobiologicznego w hodowli komórkowej i powiązanych zastosowaniach laboratoryjnych. Roztwór 100x zawiera dobrze znane połączenie penicyliny, streptomycyny i amfoterycyny B, zapewniając szerokie spektrum działania przeciwdrobnoustrojowego przeciwko bakteriom Gram-dodatnim i Gram-ujemnym, drożdżom i grzybom nitkowatym. Preparat nadaje się do stosowania w hodowlach komórek eukariotycznych, pożywkach bakteryjnych i innych systemach wrażliwych na zanieczyszczenia, wspierając czyste i spójne operacje laboratoryjne.
Zastosowanie i korzyści Rozwiązanie to, zoptymalizowane pod kątem rutynowych protokołów badawczych, jest szeroko stosowane do utrzymywania aseptycznych warunków w procesach hodowli komórkowych. Zapewnia niezawodne działanie w środowiskach wrażliwych na zanieczyszczenia, pomagając naukowcom zmniejszyć ryzyko przerostu drobnoustrojów bez uszczerbku dla zdrowia komórek lub powtarzalności eksperymentów. Sterylnie filtrowana formuła eliminuje potrzebę dodatkowych etapów solubilizacji, wspierając usprawnione przygotowanie mediów i zmniejszając zmienność w codziennych procedurach laboratoryjnych.
Zastosowanie i kompatybilność Aby uzyskać standardowe stężenia robocze, należy rozcieńczyć roztwór w stosunku 1:100 w pełnym podłożu hodowlanym. Produkt jest kompatybilny z szeroką gamą linii komórkowych ssaków i pożywek podstawowych. Dzięki stałej dostępności produktu, badacze mogą korzystać z niezawodnej ciągłości dostaw i uproszczonego planowania logistycznego. Roztwór należy przechowywać w temperaturze ≤ -15 °C i chronić przed powtarzającymi się cyklami zamrażania i rozmrażania w celu zachowania stabilności. Wyłącznie do użytku badawczego. Nie stosować w procedurach diagnostycznych lub terapeutycznych. Nie stosować u ludzi ani zwierząt.45,00 €*PBSRoztwór soli fizjologicznej buforowanej fosforanami (PBS)
Sól fizjologiczna buforowana fosforanami (PBS) jest szeroko stosowanym roztworem buforowym w badaniach biologicznych i chemicznych. Odgrywa kluczową rolę w utrzymywaniu równowagi pH i osmolarności podczas różnych procedur eksperymentalnych, w tym przetwarzania tkanek i hodowli komórkowej. Nasz roztwór PBS jest starannie opracowany ze składników o wysokiej czystości, aby zapewnić stabilność i niezawodność w każdym eksperymencie. Osmolarność i stężenia jonów naszego PBS ściśle naśladują te występujące w ludzkim organizmie, dzięki czemu jest on izotoniczny i nietoksyczny dla większości komórek.
Skład naszego roztworu PBS
Nasz roztwór PBS to dostosowana pod względem pH mieszanka ultraczystych buforów fosforanowych i roztworów soli fizjologicznej. W stężeniu roboczym 1X zawiera:
8000 mg/l chlorku sodu (NaCl)
200 mg/l chlorku potasu (KCl)
1150 mg/L Bezwodny dwuzasadowy fosforan sodu (Na2HPO4)
200 mg/L Fosforan potasu jednozasadowy bezwodny (KH2PO4)
Taki skład zapewnia optymalne pH i równowagę jonową, odpowiednie do szerokiego zakresu zastosowań biologicznych.
Zastosowania naszego roztworu PBS
Nasz roztwór PBS jest idealny do różnych zastosowań w badaniach biologicznych. Jego izotoniczne i nietoksyczne właściwości sprawiają, że nadaje się do rozcieńczania substancji i płukania pojemników z komórkami. Roztwory PBS zawierające EDTA są skuteczne w odłączaniu przyczepionych i zbrylonych komórek. Do PBS nie należy jednak dodawać metali dwuwartościowych, takich jak cynk, ponieważ może to spowodować wytrącanie się osadów. W takich przypadkach zalecane są bufory Good's. Ponadto nasz roztwór PBS jest akceptowalną alternatywą dla wirusowego podłoża transportowego do transportu i przechowywania wirusów RNA, w tym SARS-CoV-2.
Kontrola jakości
Sterylnie filtrowany
Przechowywanie i okres trwałości
Przechowywać w temperaturze od +2°C do +25°C, chronić przed światłem.
Po otwarciu przechowywać w temperaturze od 2°C do 25°C i zużyć w ciągu 24 miesięcy.
Warunki wysyłki
Temperatura otoczenia
Konserwacja
Przechowywać w lodówce w temperaturze od +2°C do +8°C w ciemności. Unikać zamrażania i częstego podgrzewania do temperatury +37°C, ponieważ obniża to jakość produktu.
Nie podgrzewać nośnika powyżej 37°C ani nie używać niekontrolowanych źródeł ciepła, takich jak urządzenia mikrofalowe.
Jeśli ma być użyta tylko część pożywki, należy usunąć wymaganą ilość i ogrzać ją do temperatury pokojowej przed użyciem.
Skład
Kategoria
Składniki
Stężenie (mg/L)
Sole
Chlorek potasu
200
Fosforan potasu jednozasadowy bezwodny
200
Chlorek sodu
8000
Bezwodny dwuzasadowy fosforan sodu
115020,00 €* -
Powiązane produkty
Powiązane produkty
Ludzkie mezenchymalne komórki macierzyste - tkanka tłuszczowaOrganizm Człowiek Tkanka Tkanka tłuszczowa 690,00 €*Ludzkie komórki macierzyste z pęcherzyków zębowych (hDFSC)Organizm Człowiek Tkanka Stomatologia 800,00 €*Ludzkie komórki macierzyste z miazgi zębowej (hDPSC)Organizm Człowiek Tkanka Stomatologia 800,00 €*