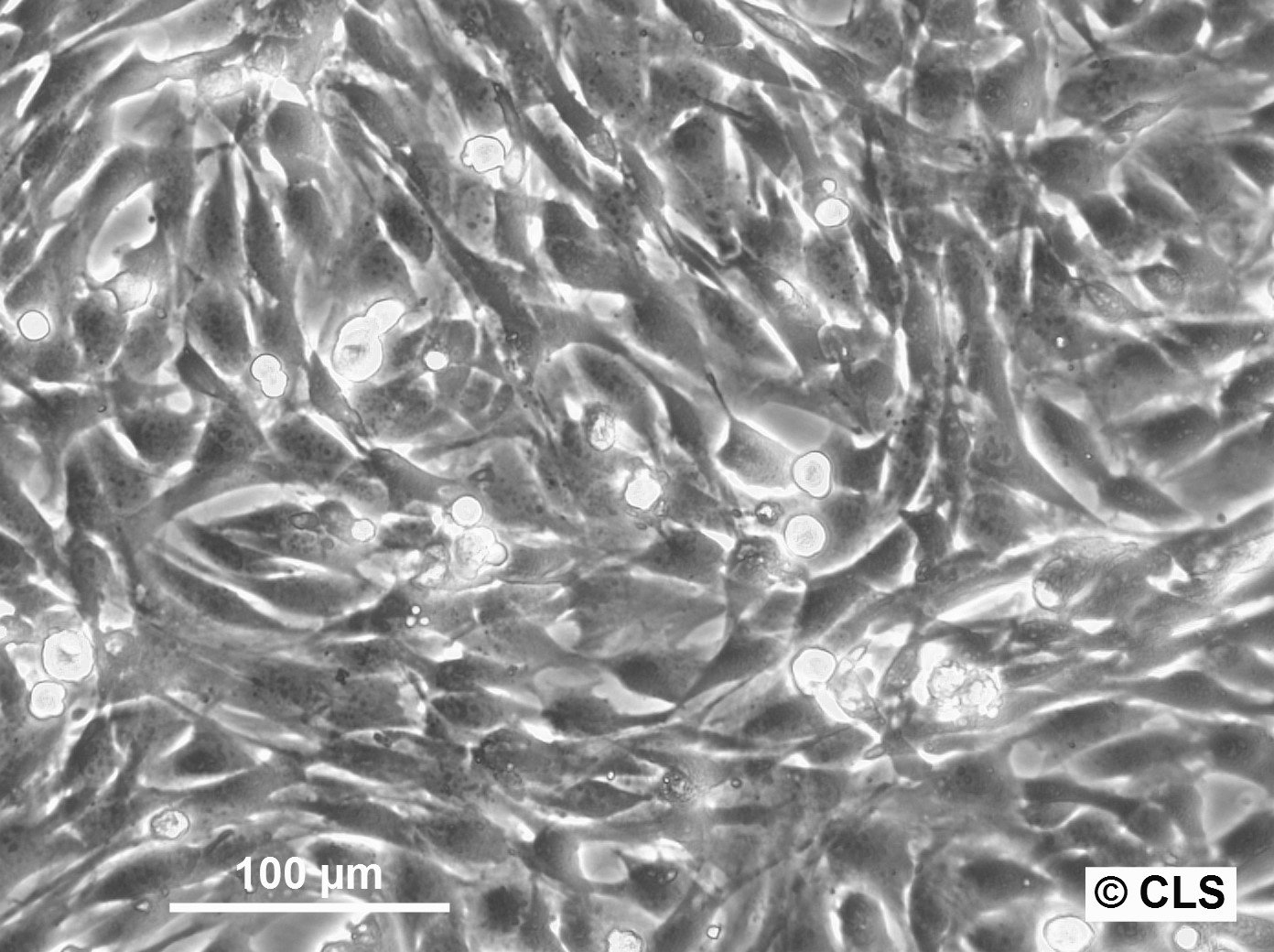
Komórki mioblastów C2C12: Pionierskie badania nad biologią i regeneracją mięśni
Znane w dziedzinie biologii i regeneracji mięśni, komórki mioblastów C2C12 służą jako niezastąpione narzędzie dla badaczy zagłębiających się w zawiłości tworzenia, różnicowania i dynamiki molekularnej mięśni szkieletowych. Ta mysia linia komórkowa oferuje solidną platformę do badania komórkowych i genetycznych podstaw funkcjonowania i naprawy mięśni.
Przed wyruszeniem w podróż z komórkami C2C12 ważne jest, aby zapoznać się z ich pochodzeniem, charakterystyką i zastosowaniami. Niniejszy przegląd zapewnia niezbędny wgląd w:
Odkrywanie podstaw komórek mioblastów C2C12
Zrozumienie pochodzenia komórek C2C12 i ich unikalnych właściwości ma fundamentalne znaczenie dla wykorzystania ich potencjału w badaniach. Ta sekcja rzuca światło na:
- Początki komórek C2C12 sięgają pionierskiej pracy Yaffe i Saxel w 1977 roku, którzy utworzyli tę linię z mięśnia uda 2-miesięcznej myszy C3H, po urazie zmiażdżenia. Ta historia pochodzenia podkreśla odporność i zdolność regeneracyjną tych komórek.
- W hodowli komórki C2C12 wykazują niezwykłą zdolność adaptacji, rozwijając się w warunkach wysokiej zawartości surowicy do proliferacji i przechodząc do tworzenia miotub, gdy są poddawane warunkom niskiej zawartości surowicy w systemach hodowli zastępujących surowicę, ulegają różnicowaniu, przechodząc od proliferujących mioblastów do dojrzałych miotub. Przejście to jest kierowane przez dobrze zaaranżowaną sieć sygnałów, od wewnątrzkomórkowych zmian metabolicznych po zmiany w transporterach błonowych, zapewniając okno na adaptację i specjalizację komórkową.
- Charakterystyczna morfologia komórek C2C12 przypominająca mioblasty, charakteryzująca się promienistym rozgałęzieniem i wydłużonymi włóknami, stanowi dynamiczny model do badania zachowania i interakcji komórek mięśniowych.
- Utrzymując status diploidalnych chromosomów, komórki C2C12 oferują stabilne tło genetyczne dla eksperymentów, zapewniając spójność i wiarygodność wyników badań.
Wyrusz w podróż badawczą z komórkami mioblastów C2C12, aby odkryć nowe wymiary biologii i regeneracji mięśni, wykorzystując ich potencjał do lepszego zrozumienia chorób mięśni i strategii terapeutycznych.
Informacje dotyczące hodowli komórek C2C12
Komórki C2C12, szeroko znane ze swojej roli w badaniach nad biologią mięśni, wymagają specyficznych warunków dla optymalnego wzrostu i różnicowania. Oto kluczowe punkty, które należy wziąć pod uwagę podczas hodowli mioblastów C2C12:
Czas podwojenia: Czas podwojenia komórek C2C12 wynosi zazwyczaj od 12 do 24 godzin, co wskazuje na ich szybkie tempo proliferacji w idealnych warunkach.
Typ komórek: Te mioblasty są przylegające, co wymaga odpowiedniej powierzchni do przyczepienia i wzrostu.
Gęstość wysiewu: Idealna gęstość wysiewu dla komórek C2C12 wynosi około 1 x 10^4 komórek/cm^2. Przy tej gęstości komórki zwykle osiągają konfluencję w ciągu około 4 dni, co sprawia, że kluczowe jest monitorowanie konfluencji komórek, aby zapobiec nadmiernemu wzrostowi.
Pożywkahodowlana: Zalecaną pożywką do hodowli komórek C2C12 jest RPMI 1640, wzbogacona 10% płodową surowicą bydlęcą (FBS) i 2,1 mM L-glutaminy. Pożywka ta zaspokaja potrzeby żywieniowe komórek i promuje zdrową proliferację.
Warunki wzrostu: Hodowlę najlepiej prowadzić w temperaturze 37°C w nawilżonym inkubatorze z 5% CO2, tworząc środowisko naśladujące warunki fizjologiczne.
Przechowywanie: W celu długoterminowej konserwacji, komórki C2C12 są przechowywane w fazie gazowej ciekłego azotu lub w zamrażarkach o bardzo niskiej temperaturze, utrzymując temperaturę poniżej -150°C.
Zamrażanie i rozmrażanie: Przy użyciu pożywki CM-1 lub CM-ACF zaleca się powolne zamrażanie w celu stopniowego obniżania temperatury i zachowania żywotności komórek. Po rozmrożeniu komórki są delikatnie ponownie zawieszane w świeżej pożywce, odwirowywane w celu usunięcia pożywki zamrażającej, a następnie przenoszone do nowych kolb hodowlanych.
Bezpieczeństwo biologiczne: Hodowla komórek C2C12 wymaga ustawienia poziomu bezpieczeństwa biologicznego 1, zapewniającego bezpieczną obsługę i praktyki konserwacyjne w laboratorium.
Przestrzeganie tych parametrów hodowli zapewnia zdrowie i żywotność komórek C2C12, ułatwiając udane eksperymenty i wyniki badań w biologii mięśni i nie tylko.
Linia komórkowa C2C12: Zalety i ograniczenia
Linia komórkowa mysich mioblastów C2C12, pochodząca z tkanki mięśni szkieletowych, jest powszechnie uznawana w dziedzinie badań biomedycznych ze względu na swój unikalny zestaw zalet i ograniczeń.
Zalety
Dobrze scharakteryzowane: Komórki C2C12 zostały dogłębnie przebadane, zapewniając głębokie zrozumienie ich fizjologicznych i biologicznych właściwości, takich jak morfologia, potencjał różnicowania i odpowiedź na różne bodźce. Ta dokładna charakterystyka zapewnia wiarygodność i powtarzalność wyników badań.
Różnicowanie mięśni: Kluczową zaletą komórek C2C12 jest ich zdolność do różnicowania się w miotuby, naśladując rozwój komórek mięśniowych. To sprawia, że są one niezbędnym narzędziem do badania biologii mięśni, w tym tworzenia komórek mięśniowych, rozwoju i ekspresji białek kurczliwych, które są kluczowe dla funkcjonowania mięśni.
Wszechstronny model dla biologii komórki: Jako dobrze udokumentowany model, komórki C2C12 oferują wgląd w liczne procesy komórkowe, w tym reakcje na stres oksydacyjny, metabolizm glukozy, sygnalizację insulinową i mechanizmy leżące u podstaw insulinooporności. Ich zastosowanie ułatwia głębsze zrozumienie tych procesów zarówno na poziomie komórkowym, jak i molekularnym.
Ograniczenia
Różnice gatunkowe: Będąc linią komórkową pochodzącą od myszy, komórki C2C12 mogą nie odwzorowywać idealnie biologii ludzkich mięśni. Różnice w ekspresji genów, metabolizmie komórkowym i reakcjach fizjologicznych między myszami i ludźmi mogą ograniczać bezpośrednie zastosowanie wyników badań do warunków ludzkich.
Aspekty te podkreślają kluczową rolę komórek C2C12 w badaniach nad mięśniami, podkreślając jednocześnie znaczenie uwzględnienia ich ograniczeń, zwłaszcza podczas ekstrapolacji danych na biologię człowieka.
Podnieś poziom swoich badań dzięki komórkom C2C12
Zastosowania badawcze linii komórkowej C2C12
Poznaj różnorodne zastosowania badawcze mysiej linii komórkowej C2C12.
Badanie biologii mięśni: Komórki C2C12 służą jako solidny model in vitro do badań nad biologią mięśni, umożliwiając badania nad rozwojem, metabolizmem i różnicowaniem mięśni. Komórki te mogą różnicować się w komórki mięśniopodobne, zapewniając wgląd w tworzenie miotub i mechanizmy regeneracji mięśni. W jednym z badań podkreślono rolę TGF-β1 i mikroRNA-22 w funkcjonowaniu komórek C2C12, podkreślając ich regulacyjny wpływ na proliferację i różnicowanie komórek.
Badania przesiewowe leków i testy toksyczności: Linia komórkowa C2C12 odgrywa kluczową rolę w ocenie potencjalnych leków na zaburzenia mięśni. Oferuje ona platformę do oceny wpływu leków na metabolizm i różnicowanie komórek mięśniowych. Badania wykazały korzystny wpływ ekstraktu z li ściCnidoscolus aconitifolius na komórki C2C12, zwiększając utlenianie kwasów tłuszczowych i bioenergetykę mitochondriów, podczas gdy ekstrakt z liściMoringa oleifera chroni miotuby C2C12 przed stresem oksydacyjnym. Komórki C2c12 są nieocenione w badaniach przesiewowych leków epigenetycznych, które mogą wpływać na różnicowanie mięśni lub stężenie białek miofilamentowych. Model leków epigenetycznych pozwala badaczom obserwować ekspresję folistatyny i fosforylację smad1, kluczowych czynników w dojrzewaniu i regeneracji komórek macierzystych mięśni.
- konstrukcje tkankowe 3D i rozwój tkanki mięśni szkieletowych: Wykorzystując pożywkę do hodowli mioblastów c2c12, naukowcy z powodzeniem hodowali mioblasty i miotuby w wymiarowych kulturach komórkowych, które naśladują strukturę i funkcję tkanki mięśni szkieletowych. Te trójwymiarowe konstrukty tkankowe oferują szczegółowy model do badania tworzenia sarkomerów, podstawowej jednostki skurczu mięśni. Zapewniając trójwymiarowe ramy, takie konstrukty znacząco przyczyniają się do naszego zrozumienia miogenezy i rozwoju różnych fenotypów mięśni, rzucając światło na złożoną orkiestrację innych białek i zawartość białek kurczliwych podczas tworzenia mięśni.
Produkcja komórek mięśni szkieletowych: Ostatecznym celem pozostaje praktyczne zastosowanie tych badań do dojrzewania mięśni in vivo i produkcji komórek mięśni szkieletowych, mających na celu naprawę lub zastąpienie uszkodzonej tkanki w warunkach klinicznych. Hodowla komórek satelitarnych, w połączeniu z konwencjonalną hodowlą uzupełniającą surowicę, kładzie podwaliny pod rozwój terapii, które mogą zrewolucjonizować leczenie chorób związanych z mięśniami.
Tworzenie sarkomerówi funkcja kurczliwości: Tworzenie sarkomerów w miotubach pochodzących z komórek C2C12 jest głównym obszarem zainteresowania badaczy. Sarkomery są podstawowymi jednostkami kurczliwymi komórek mięśniowych, a ich prawidłowy montaż ma kluczowe znaczenie dla funkcjonowania mięśni. Badanie tych struktur dostarcza cennych informacji na temat zawartości białek kurczliwych i ogólnego stanu zdrowia mięśni, zwłaszcza gdy komórki C2C12 są poddawane różnym lekom, które mogą wpływać na te procesy.
Protokół transfekcji komórek C2C12
Potrzebne materiały:
Komórki mioblastów C2C12
Podłoże hodowlane: DMEM z 10-20% FBS
Odczynnik do transfekcji (np. Lipofectamine)
Plazmid DNA lub siRNA
Opti-MEM lub podobna pożywka bez surowicy
płytki 6-dołkowe lub szalki hodowlane
Inkubator ustawiony na 37°C z 5% CO2
Procedura:
Posiew komórek:
Jeden dzień przed transfekcją wysiej komórki C2C12 na 6-dołkową płytkę, aby zapewnić ich 70-80% konfluencję w czasie transfekcji.
Mieszanina odczynników DNA:
Rozcieńczyć plazmidowe DNA lub siRNA w Opti-MEM (bez surowicy) do końcowej objętości, która pozwoli uzyskać optymalny stosunek DNA do odczynnika.
Wymieszać odczynnik do transfekcji z Opti-MEM w oddzielnej probówce i inkubować w temperaturze pokojowej przez 5 minut.
Połączyć mieszaniny DNA i odczynnika i inkubować przez 20 minut w temperaturze pokojowej, aby umożliwić utworzenie kompleksu.
Transfekcja:
Usunąć pożywkę wzrostową z komórek i zastąpić ją kompleksem DNA-odczynnik w Opti-MEM.
Inkubować komórki z mieszaniną transfekcyjną przez 4-6 godzin w inkubatorze.
Wymiana pożywki:
Po inkubacji zastąpić mieszaninę transfekcyjną świeżą pożywką wzrostową i ponownie umieścić komórki w inkubatorze.
Analiza ekspresji:
Przeanalizuj skuteczność transfekcji po 24-48 godzinach, sprawdzając ekspresję transfekowanego genu lub wpływ siRNA.
Protokół różnicowania dla komórek C2C12
Potrzebne materiały:
Komórki mioblastów C2C12
Podłoże hodowlane: DMEM z 10-20% FBS
Podłoże do różnicowania: DMEM z 2% surowicą końską
płytki 6-dołkowe lub szalki hodowlane
Inkubator ustawiony na 37°C z 5% CO2
Procedura:
Posiew komórek:
Posiej komórki C2C12 na 6-dołkowej płytce lub szalce hodowlanej i hoduj je w pożywce wzrostowej, aż osiągną pełną konfluencję.
Indukcja różnicowania:
Gdy komórki osiągną konfluencję, odessać pożywkę wzrostową i zastąpić ją pożywką do różnicowania.
Niskie stężenie surowicy jest kluczowe dla zainicjowania różnicowania.
Konserwacja:
Codziennie zmieniaj podłoże do różnicowania, aby zapewnić świeże składniki odżywcze i usunąć resztki komórkowe.
Monitorowanie różnicowania:
Obserwuj komórki codziennie pod mikroskopem. W ciągu 1-2 dni mioblasty powinny się wyrównać i połączyć, tworząc miotuby.
Pełne różnicowanie i formowanie miotub zazwyczaj następuje w ciągu 3-5 dni.
Analiza:
Po 5-7 dniach zróżnicowane miotuby powinny być gotowe do dalszych zastosowań, takich jak immunofluorescencja lub analiza ekspresji białek.
Uwaga: Dokładne warunki transfekcji i różnicowania (takie jak stężenie odczynnika do transfekcji lub procent surowicy w pożywce do różnicowania) mogą się różnić i powinny być zoptymalizowane w oparciu o konkretne potrzeby eksperymentalne. Optymalne warunki należy zawsze sprawdzać w arkuszach danych produktu lub literaturze naukowej.
Zasoby dla linii komórkowej C2C12: Protokoły, filmy i nie tylko
Odkryj cenne zasoby dotyczące linii komórkowej C2C12:
Protokół transfekcji C2C12: Kompleksowy samouczek wideo szczegółowo opisujący transfekcję in vitro komórek C2C12.
Myoblasty C2C12: Ten przewodnik po protokole obejmuje podstawy pasażowania i transfekcji komórek mięśniowych C2C12.
Hodowla komórek C2C12: Zawiera kluczowe informacje na temat hodowli i różnicowania komórek C2C12.
Różnicowanie komórek C2C12: Ten dokument zawiera szczegółowy przewodnik dotyczący hodowli i różnicowania komórek C2C12 z zamrożonych kultur.
Komórki C2C12: Publikacje badawcze
Poniżej wyróżniono ważne publikacje dotyczące komórek C2C12:
Interleukina-6 indukuje różnicowanie miogeniczne poprzez sygnalizację JAK2-STAT3: Badanie opublikowane w 2019 roku w International Journal of Molecular Sciences bada rolę IL-6 w różnicowaniu miogenicznym komórek C2C12, rzucając światło na leżący u podstaw szlak sygnałowy JAK2/STAT3.
Wpływ ekstraktu z liści Rubus Anatolicus na metabolizm glukozy: Opublikowane w 2023 r. badanie to bada modulację metabolizmu glukozy przez Rubus An atolicus w C2C12 i innych liniach komórkowych, sugerując jego potencjał w zwiększaniu glikogenezy.
Zmniejszony wpływ miostatyny na różnicowanie komórek C2C12: W artykule 2020 Biomolecules omówiono, w jaki sposób różnicowanie komórek C2C12 znacznie zmniejsza wpływ miostatyny na sygnalizację wewnątrzkomórkową, zapewniając nowy wgląd w rozwój mięśni.
Wpływ genisteiny na geny związane ze szlakiem insulinowym: Badanie z 2018 r. w Folia Histochemica et Cytobiologica wykorzystujące zróżnicowane komórki C2C12 do oceny wpływu genisteiny na geny szlaku insulinowego.
Rola Moringa Oleifera w metabolizmie oksydacyjnym: To badanie Phytomedicine Plus (2021) zakłada, że ekstrakt z liści Moringa Oleifera promuje biogenezę mitochondriów w miotubach C2C12 poprzez szlak SIRT1-PPARα.
Często zadawane pytania dotyczące komórek C2C12
Piśmiennictwo
- Denes, L.T., et al., Culturing C2C12 myotubes on micromolded gelatin hydrogels accelerates myotube maturation. Mięśnie szkieletowe, 2019. 9(1): p. 1-10.
- Wong, C.Y., H. Al-Salami, and C.R. Dass, C2C12 cell model: its role in understanding of insulin resistance at the molecular level and pharmaceutical development at the preclinical stage. J Pharm Pharmacol, 2020. 72(12): p. 1667-1693.
- Wang, H., et al., miR-22 reguluje proliferację i różnicowanie mioblastów C2C12 poprzez ukierunkowanie na TGFBR1. European Journal of Cell Biology, 2018. 97(4): p. 257-268.
- Avila-Nava, A., et al., Ekstrakty z liści Chaya (Cnidoscolus aconitifolius (Mill.) IM Johnst) regulują bioenergetykę mitochondriów i utlenianie kwasów tłuszczowych w miotubach C2C12 i pierwotnych hepatocytach. Journal of Ethnopharmacology, 2023. 312: p. 116522.
- Ceci, R., et al., Ekstrakt z liści Moringa oleifera chroni miotuby C2C12 przed stresem oksydacyjnym wywołanym przez H2O2. Antioxidants, 2022. 11(8): p. 1435.