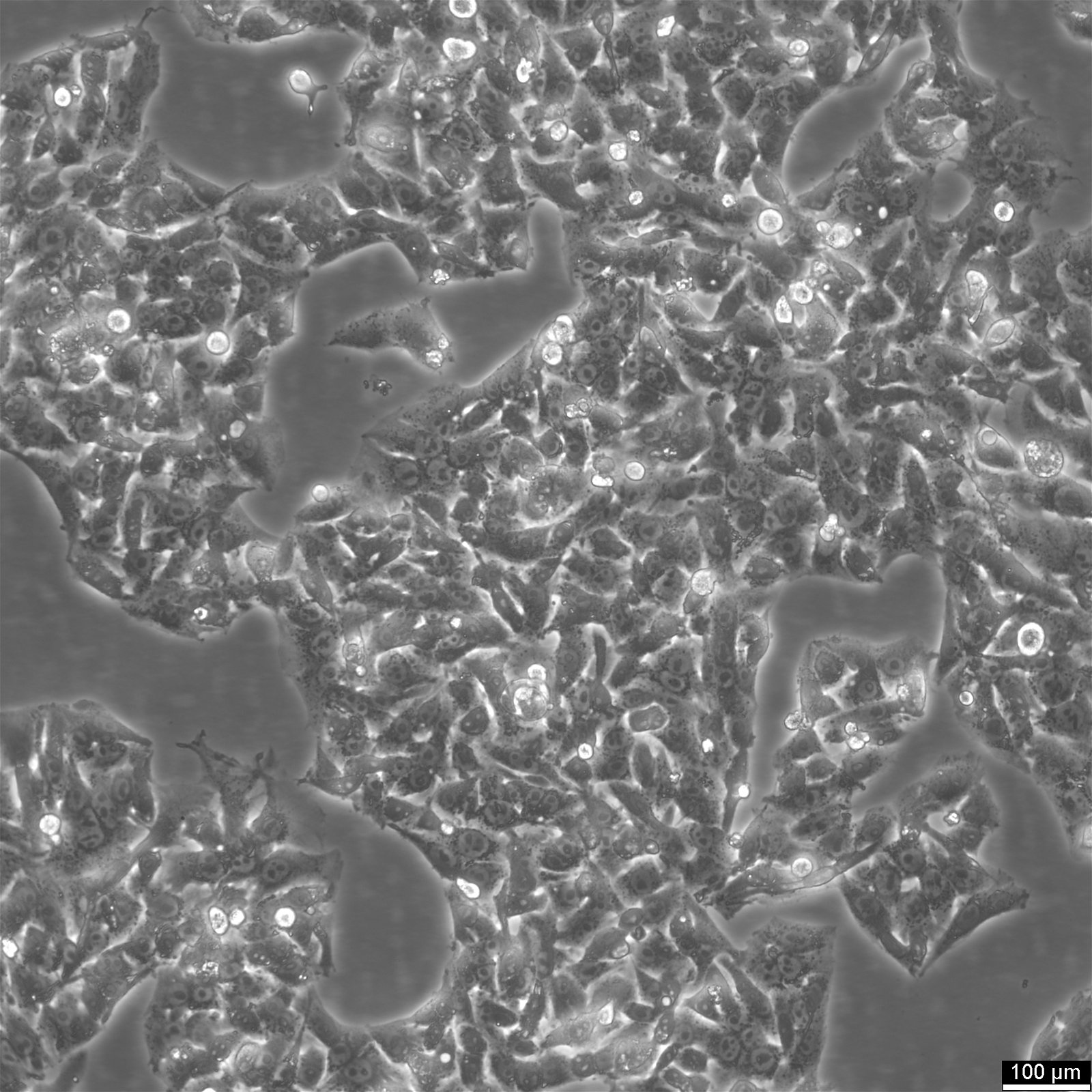
Komórki HepG2 - źródło badań nad rakiem wątroby
Hep-G2 to ludzka linia komórek raka wątroby pochodząca z tkanki wątroby 15-letniego mężczyzny rasy kaukaskiej z rakiem wątrobowokomórkowym. Komórki te są często wykorzystywane w badaniach metabolizmu leków i hepatotoksyczności. Chociaż komórki HepG2 charakteryzują się wysokim współczynnikiem proliferacji i wyglądem przypominającym nabłonek, są one nienowotworowe i pełnią różne zróżnicowane funkcje wątrobowe. W 1975 roku naukowcy uzyskali komórki HepG2 z raka wątrobowokomórkowego, co czyni je pierwszą linią komórek wątrobowych wykazującą krytyczne cechy hepatocytów. W przeciwieństwie do wcześniej ustalonej linii komórkowej SK-Hep1, w której brakuje istotnych markerów komórek wątroby, komórki HepG2 mogą wydzielać różne białka osocza i stanowią cenny model do badania wewnątrzkomórkowej dynamiki domen powierzchni komórek w ludzkich hepatocytach. Komórki te wykazują morfologię podobną do nabłonka, mają modalną liczbę chromosomów 55 i mogą być stymulowane ludzkim hormonem wzrostu
Charakterystyka HepG2
Typowy kształt pierwotnych hepatocytów jest sześcienny i zwykle zawiera dwa jądra. W przeciwieństwie do nich, komórki HepG2 mają morfologię podobną do nabłonka z pojedynczym jądrem i liczbą chromosomów wahającą się od 48 do 54 na komórkę. Chociaż komórki HepG2 mogą stanowić do 25% całkowitego białka komórkowego, ich rozmiar jest większy niż normalnych hepatocytów, stanowiąc około 10% całego białka w komórce. Białka komórkowe są kluczowymi aktorami w komórce, wykonującymi funkcje określone przez geny.
Komórki nowotworowe, w tym te z nieprawidłową liczbą chromosomów, często wykazują wzrost liczby jąder, do siedmiu na komórkę. Ze względu na ich wysoki stopień zróżnicowania in vitro, komórki HepG2 stanowią idealny model do badania wewnątrzkomórkowego ruchu i dynamiki kanałów żółciowych, sinusoidalnych białek błonowych i lipidów w ludzkich hepatocytach.
Średnia średnica komórki HepG2 wynosi około 10-20 µm, czyli jest mniejsza niż hepatocytu o średnicy 15 µm, ale podobna do komórek nowotworowych Hepatoblastoma (HB), których średnica wynosi od 10 do 20 µm.
Genetyka HepG2
Linia komórkowa Hep-G2 wykazuje kilka translokacji, w tym między krótkimi ramionami chromosomów 1 i 21, trisomie chromosomów 2, 16 i 17 oraz tetrasomię chromosomu 20. Obserwuje się również utratę regionu chromosomu 4q3, związaną z translokacją t(1;4) często obserwowaną w Hepatoblastoma (HB) i innymi nieprawidłowościami chromosomalnymi, takimi jak trisomie 2 i 20. Liczba chromosomów w komórkach HepG2 waha się od 50 do 60, co wskazuje na kariotyp hiperdiploidalny, podczas gdy niektóre przypadki wykazują ponad 100 chromosomów i charakteryzują się powiększeniem tetraploidalnym. Komórki HepG2 zawierają około 7,5 pg DNA, o 15% więcej niż przeciętna komórka somatyczna. Dla porównania, pierwotne hepatocyty mają sześcienny kształt i zazwyczaj zawierają dwa jądra [1].
Profil mutacyjny komórek HepG2
Linia komórkowa HepG2 jest nosicielem mutacji regionu promotora TERT C228T, obecnej również w raku wątrobowokomórkowym (HCC) i hepatoblastoma (HB). Mutacja ta przyczynia się do immortalizacji poprzez ochronę telomerów w komórkach nowotworowych. Dodatkowo, komórki HepG2 wykazują dziki typ TP53, genu o krytycznym znaczeniu dla tłumienia ludzkiego raka, ponieważ odgrywa on rolę w zatrzymaniu cyklu komórkowego, apoptozie i starzeniu. Mutacje w tym genie mogą promować proliferację komórek.
Komórki HepG2 uczestniczą w kilku szlakach, w tym w rozregulowaniu wzrostu komórek, szlakach przeżycia, takich jak płodowy i embrionalny HB, oraz szlaku Wnt/β-katenina. Ponadto linia komórkowa ma charakterystyczną delecję trzeciego eksonu genu CTNNB1, która jest identyczna z tą obserwowaną w nabłonkowym typie HB [2,3].
Przegląd komórek raka wątrobowokomórkowego HepG2 w badaniach nad wątrobą
Komórki HepG2, pochodzące z ludzkiego wątrobiaka, stały się nieocenionym narzędziem do badania funkcji i chorób wątroby, w tym raka wątrobowokomórkowego. Te wątrobowe linie komórkowe zapewniają wgląd w odpowiedzi komórkowe ludzkich hepatocytów w różnych warunkach eksperymentalnych. Zastosowanie plazmidów reporterowych lucyferazy w komórkach HepG2 było szczególnie skuteczne w śledzeniu ekspresji genów i transfekcji komórkowych, które mają fundamentalne znaczenie w badaniach metabolicznych, takich jak badanie wpływu etanolu na komórki wątroby
Badania nad infekcjami wirusowymi i chorobami wątroby z wykorzystaniem komórek HepG2
Immortalizowane linie komórek nowotworowych wątroby, takie jak HepG2 i Huh7, są niezbędne w badaniach nad infekcjami wirusowymi, wykazując pełną replikację cyklu komórkowego wirusa zapalenia wątroby typu D (HDV) i ekspresję wirusa zapalenia wątroby typu B (HBV) [5,6]. Równolegle, linie komórkowe HepaRG odgrywają kluczową rolę w wyjaśnianiu mechanizmów wnikania HBV [7]. Komórki HepG2 są również wykorzystywane do badania różnych ludzkich chorób wątroby, od chorób genetycznych, takich jak postępująca rodzinna cholestaza wewnątrzwątrobowa (PFIC) i zespół Dubina-Johnsona, po badania środowiskowe i dietetyczne związane z czynnikami cytotoksycznymi i genotoksycznymi, a także w badaniach nad lekami i hepatokarcynogenezą [8,9]. Ich zastosowanie rozciąga się na próby z urządzeniami sztucznej wątroby
Interakcje komórek HepG2 z biomateriałami w inżynierii tkankowej
Interakcja komórek HepG2 z różnymi biomateriałami ma kluczowe znaczenie w inżynierii tkankowej. Techniki takie jak sonda koloidalna pomagają zrozumieć te interakcje poprzez pomiar właściwości adhezyjnych komórek, które są niezbędne do określenia żywotności komórek w celu opracowania rusztowań i dokładnych modeli tkanek wątroby
Zachowanie komórek i innowacje w modelach opartych na HepG2
Badanie zachowania komórek w modelach opartych na HepG2 ma kluczowe znaczenie dla badań nad chorobami wątroby. Postępy w trójwymiarowych hodowlach komórek sferoidalnych doprowadziły do stworzenia sferoidów komórek HepG2, oferując bardziej fizjologiczny model, który ściśle odzwierciedla normalne hepatocyty. Te modele 3D, o zwiększonej aktywności metabolicznej, wskazują na potencjał komórek HepG2 jako modelu dla hepatoblastoma i są istotne w badaniach nad leczeniem raka, zwłaszcza w symulacji guzów wątroby i testowaniu nowych podejść terapeutycznych [10-12]
Porównanie i charakterystyka HepG2 wśród innych linii komórek nowotworowych
HepG2 jest jedną z najczęściej stosowanych linii komórkowych nowotworów wątroby, wybraną ze względu na jej szerokie zastosowanie w badaniach naukowych spośród około 40 dostępnych linii komórkowych nowotworów wątroby [13]. Pomimo słabej lub braku ekspresji niektórych enzymów cytochromu P450 w porównaniu z normalnymi hepatocytami, profil metaboliczny HepG2 spowodował wysiłki zmierzające do modyfikacji linii komórkowej w celu lepszego badania metabolizmu leków [13]. W porównaniu z nowotworowymi liniami komórkowymi, takimi jak MCF7, PC3, 143B i HEK293, komórki HepG2 wykazują unikalne profile zawartości aminokwasów, które znacząco wpływają na syntezę i wydzielanie białek, podkreślając ich unikalne szlaki metaboliczne [14]
Odkrywanie badań nad chorobami wątroby za pomocą HepG2
Podhodowla komórek HepG2
Oto pięć kroków usuwania przylegających komórek z kolb do hodowli komórkowych przy użyciu Accutase:
- Usuń pożywkę z kolby do hodowli komórkowej i przepłucz przylegające komórki używając PBS bez wapnia i magnezu. Użyj 3-5 ml PBS dla kolb T25 i 5-10 ml dla kolb T75.
- Dodaj Accutase do kolby hodowli komórkowej, używając 1-2 ml na kolbę T25 i 2,5 ml na kolbę T75. Upewnić się, że Accutase pokrywa cały arkusz komórek.
- Inkubować kolbę w temperaturze pokojowej przez 8-10 minut.
- Ostrożnie ponownie zawiesić komórki w pożywce, używając 10 ml świeżej pożywki.
- Wirować ponownie zawieszone komórki przez 5 minut z prędkością 300xg, ponownie zawiesić je w świeżej pożywce i przenieść do nowych kolb zawierających świeżą pożywkę.
Perspektywy na przyszłość dla komórek HepG2
Dążenie do uwolnienia pełnego potencjału linii komórkowej HepG2 jest kontynuowane dzięki przełomowym postępom w zwiększaniu ekspresji cytochromów. Naukowcy badają również możliwości trójwymiarowych kultur komórek sferoidalnych, które oferują bardziej fizjologiczny system. Aktywność metaboliczna, w tym cytochromów, jest znacznie wyższa w sferoidalnych modelach 3D HepG2 niż w komórkach 2D, co przybliża nas do stworzenia modelu odzwierciedlającego normalne hepatocyty. Dodatkowo, badanie dynamicznych procesów leżących u podstaw nieprawidłowej dystrybucji białek powierzchniowych komórek może utorować drogę do lepszego zrozumienia chorób wątroby
Komórki HepG2: Zrozumienie ich roli i różnic w badaniach biomedycznych - najczęściej zadawane pytania
Piśmiennictwo
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiation-induced chromosomal breakage and rejoining in interphase-metaphase chromosomes of human lymphocytes, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4 Inhibition: Nowa strategia terapeutyczna mająca na celu reaktywację P53 w Hepatoblastoma. Sci. Rep. 2021, 11, 2967.
- Hussain, S.P., Schwank, J., Staib, F., Wang, X.W., Harris, C.C. TP53 Mutations and hepatocellular Carcinoma: Insights into the Etiology and Pathogenesis of Liver Cancer. Oncogene 2004.
- Schicht, G., Seidemann, L., Haensel, R., Seehofer, D., Damm, G. Critical Investigation of the Usability of Hepatoma Cell Lines HepG2 and Huh7 as Models for the Metabolic Representation of Resectable Hepatocellular Carcinoma. Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Cell Culture Models for the Investigation of Hepatitis B and D Virus Infection. Viruses 2016, 8, 261.
- Verrier, E.R., Colpitts, C.C., Bach, C., Heydmann, L., Weiss, A., Renaud, M., Durand, S.C., Habersetzer, F., Durantel, D., AbouJaoudé, G., et al. A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Viruses. Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. Infection of a Human Hepatoma Cell Line by Hepatitis B Virus. Proc. Natl. Acad. Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann, V., Knasmüller, S., Wu, X.J., Darroudi, F., Kassie, F. Use of a human-derived liver cell line for the detection of cytoprotective, antigenotoxic and cogenotoxic agents. Toxicology. 2004; 198(1-3): 329-340.
- Fanelli, A. HepG2 (rak wątrobowokomórkowy wątroby): hodowla komórkowa. HepG2. Retrieved 3 December 2017.
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Development of HepG2-Derived Cells Expressing Cytochrome P450s for Assessing Metabolism-Associated Drug-Induced Liver Toxicity. Physiol. Behav. 2017, 176, 139-148.
- Ooka, M., Lynch, C., Xia, M. Application of in Vitro Metabolism Activation in High-Throughput Screening. Int. J. Mol. Sci. 2020, 21, 8182.
- Huang, L., Coughtrie, M.W.H., Hsu, H. Down-Regulation of Dehydroepiandrosterone Sulfotransferase Gene in Human Hepatocellular Carcinoma. Mol. Cell. Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Rakowe komórki macierzyste/progenitorowe są wysoce wzbogacone w populację CD133 + CD44 + w raku wątrobowokomórkowym. Int J Cancer. 2010; 126:2067-2078.
- Arbus, C., Benyamina, A., Llorca, P.-M., Baylé, F., Bromet, N., Massiere, F., Garay, R.P., Hameg, A. Characterization of human cytochrome P450 enzymes involved in the metabolism of cyamemazine. Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.