Linia komórkowa HCT116: Filar w badaniach nad rakiem jelita grubego
Linia komórkowa HCT116 służy jako kamień węgielny w badaniach nad rakiem jelita grubego, oferując nieoceniony wgląd w patogenezę choroby i potencjalne możliwości terapeutyczne. Znana ze swojej użyteczności w badaniach nad rakiem i ocenach farmakologicznych, HCT116 ułatwia kluczowe badania nad zachowaniem guza i skutecznością leków.
Pochodzenie i podstawowa charakterystyka komórek HCT116
Zrozumienie pochodzenia i podstawowych cech komórek HCT116, takich jak ich cechy morfologiczne, skład genetyczny i wymiary komórkowe, jest niezbędne dla naukowców rozpoczynających badania z wykorzystaniem tej linii komórkowej.
Pochodzenie i krajobraz genetyczny: Pochodzące z okrężnicy 48-letniego mężczyzny rasy kaukaskiej, u którego zdiagnozowano raka jelita grubego, komórki HCT116 wyróżniają się mutacją w kodonie 13 (G13D) genu KRAS, będącego częścią szlaku sygnałowego RAS/RAF/MEK/ERK. Ta konkretna mutacja jest kluczowa w onkogennej transformacji tych komórek, podkreślając ich znaczenie w badaniach nad rakiem.
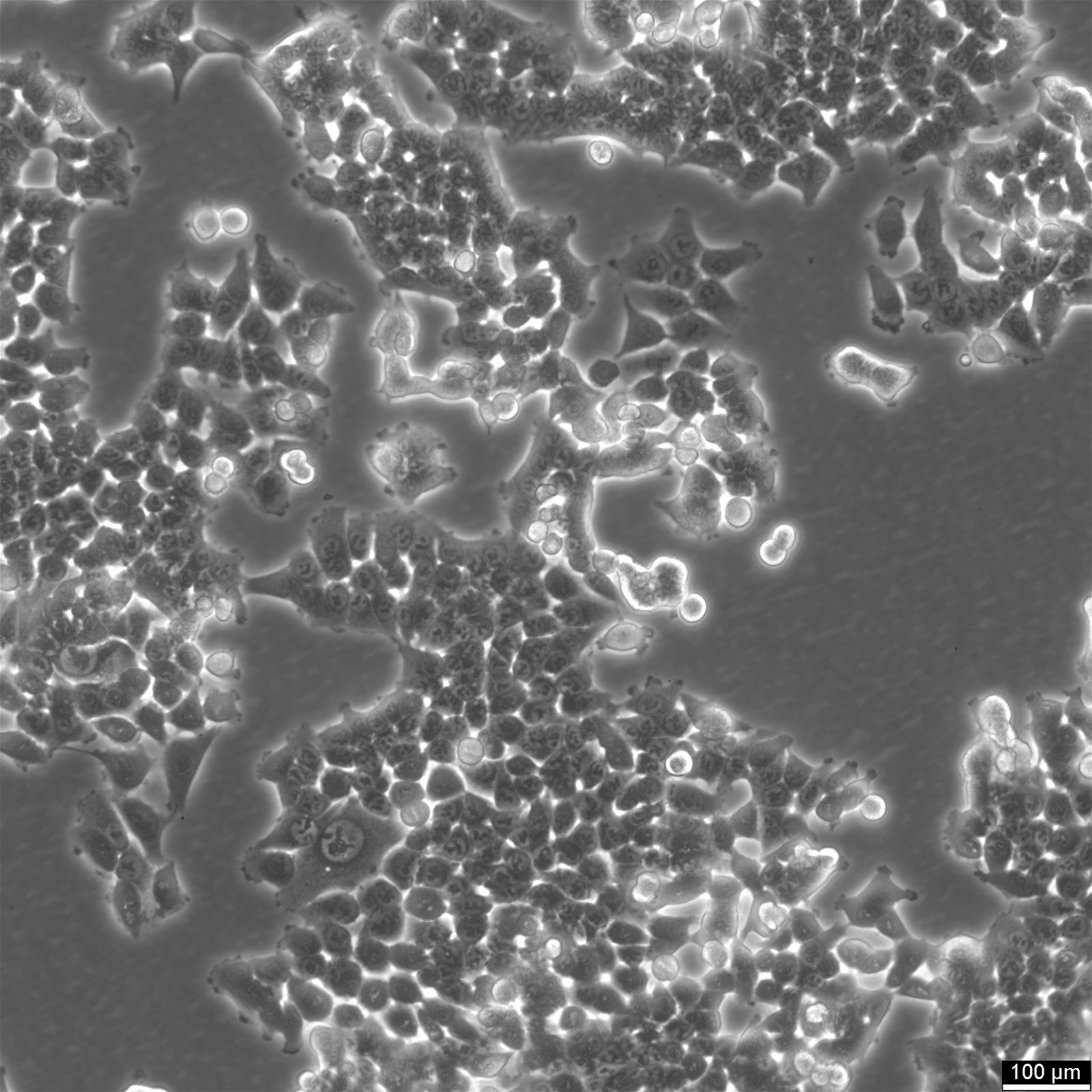
Morfologia i charakterystyka wzrostu: Wykazując morfologię podobną do nabłonka, komórki HCT116 zazwyczaj rosną w hodowlach jednowarstwowych, ale mogą również tworzyć sferoidy o średnicy 150-400 µm. Ta zdolność adaptacji wzorców wzrostu podkreśla ich wszechstronność w różnych konfiguracjach eksperymentalnych.
Profil chromosomalny: Skład chromosomalny komórek HCT116 jest prawie diploidalny, z około 70% populacji komórek zawierających 45 chromosomów. W szczególności występuje powtarzająca się amplifikacja w długich ramionach chromosomów 8, 10, 16 i 17, podczas gdy chromosom Y jest nieobecny, przyczyniając się do ich unikalnej sygnatury genomowej.
Analiza porównawcza: linie komórkowe HCT116 i HT29
Zestawiając HCT116 z HT29, inną linią komórkową ludzkiego raka jelita grubego, pojawiają się wyraźne różnice w ich potencjale onkogennym i zdolności różnicowania:
Agresywność onkogenna i różnicowanie: Komórki HCT116 charakteryzują się wysoką agresywnością onkogenną i ograniczonym potencjałem różnicowania, co czyni je modelem do badania agresywnych fenotypów nowotworów. W przeciwieństwie do nich, komórki HT29 wykazują zdolność do różnicowania się w linie podobne do enterocytów i produkujące mucynę, zapewniając kontrastowy model, który naśladuje różne aspekty biologii raka jelita grubego.
To porównawcze zrozumienie linii komórkowych HCT116 i HT29 wzbogaca zestaw narzędzi dostępnych dla naukowców, umożliwiając bardziej zniuansowane badania nad wieloaspektową naturą raka jelita grubego.
Obsługa komórek HCT116
|
Czas podwojenia: |
Czas podwojenia dla komórek nowotworowych HCT116 wynosi od 25 do 35 godzin. |
|
Przylegające lub w zawiesinie: |
Linia komórek raka okrężnicy HCT116 jest adherentna, a komórki rosną w monowarstwach. |
|
Gęstość wysiewu: |
Gęstość wysiewu 2 x104 komórek/cm2 jest zalecana dla hodowli komórek HCT116. W celu podhodowli komórki należy oddzielić za pomocą roztworu Accutase po przemyciu 1x PBS. Po odwirowaniu, osad komórek jest ponownie zawieszany w świeżej pożywce wzrostowej i przenoszony do nowej kolby. |
|
Pożywka wzrostowa: |
Pożywka McCoys 5a, uzupełniona 3,0 g/L L-glukozy, 1,5 mM L-glutaminy, 3,0 g/L NaHCO3 i 10% płodowej surowicy bydlęcej, jest optymalna do hodowli komórek HCT116. Zaleca się odnawianie pożywki 1 do 2 razy w tygodniu. |
|
Warunki wzrostu (temperatura,CO2): |
Hodowla odbywa się w nawilżanym inkubatorze w temperaturze 37°C w atmosferze 5%CO2. |
|
Przechowywanie: |
Komórki HCT116 mogą być przechowywane w temperaturze poniżej -150°C w parze lub w fazie ciekłej ciekłego azotu. |
|
Proces zamrażania i pożywka: |
Do kriokonserwacji należy używać pożywki CM-1 lub CM-ACF. Zalecana jest metoda zamrażania z kontrolowaną szybkością, pozwalająca na stopniowy spadek temperatury o 1°C na minutę, co pomaga utrzymać żywotność komórek. |
|
Proces rozmrażania: |
Rozmrozić komórki HCT116 w łaźni wodnej o temperaturze 37°C. Po dodaniu pożywki wzrostowej odwirować w celu usunięcia pozostałości pożywki zamrażającej. Ponownie zawiesić osad komórkowy w świeżej pożywce i hodować w nowych kolbach. |
|
Poziom bezpieczeństwa biologicznego: |
Poziom 1 |
Zalety linii komórkowej HCT116
Niniejsza sekcja poświęcona jest linii komórkowej HCT116, podkreślając jej kluczową rolę w badaniach nad rakiem, w szczególności w badaniach nad rakiem jelita grubego, oraz omawiając jej nieodłączne zalety.
Linia komórkowa HCT116 wyróżnia się w badaniach nad rakiem ze względu na kilka kluczowych zalet:
Model raka jelita grubego: Służy jako powszechnie uznany model in vitro raka jelita grubego, trzeciego najczęściej występującego nowotworu na świecie. Jego znaczenie w naśladowaniu ludzkiego raka jelita grubego czyni go nieocenionym dla zrozumienia biologii raka i testowania strategii terapeutycznych.
Jednorodność: Co ciekawe, około 70% komórek HCT116 wykazuje spójne profile genetyczne, oferując stosunkowo jednorodną populację. Ta jednorodność ma kluczowe znaczenie dla badań koncentrujących się na ekspresji genów, komórkowych szlakach sygnałowych i ocenie skuteczności leczenia farmakologicznego, ponieważ zapewnia spójność i wiarygodność wyników eksperymentalnych.
Wydajność transfekcji: Jedną z cech wyróżniających komórki HCT116 jest ich wysoka podatność na transfekcję, zwłaszcza wektorami wirusowymi. Cecha ta jest szczególnie korzystna w badaniach nad terapią genową, umożliwiając wprowadzenie materiału genetycznego z wydajnością i precyzją, ułatwiając w ten sposób zaawansowane manipulacje genetyczne i badania funkcjonalne.
Przyspiesz swoje odkrycia dzięki naszej uwierzytelnionej linii komórkowej HCT116
Zastosowania badawcze linii komórkowej HCT116
Linia komórkowa HCT116 ma szeroki zakres zastosowań w badaniach nad rakiem. Niektóre z nich to
Biologia raka
Linia komórkowa raka okrężnicy HCT116 jest wykorzystywana do badania progresji i rozwoju raka okrężnicy. Co więcej, pomaga ona zrozumieć podstawowe mechanizmy i szlaki sygnałowe zaangażowane w proliferację, migrację i inwazję nowotworów. W badaniu wykorzystano komórki HCT116 do badania genów zaangażowanych w rozwój oporności na leki. Naukowcy nadeksprymowali gen MDR1 w komórkach raka jelita grubego i zaobserwowali ekspresję izoform NOX (tlenku NADPH) i Nrf2. Badanie wykazało, że regulacja NOX2 i Nrf2 powoduje chemiooporność w komórkach nowotworowych; w związku z tym geny te mogą być ukierunkowane na przezwyciężenie rozwoju oporności podczas terapii przeciwnowotworowej [1]. Podobnie, badania przeprowadzone w 2021 r. wykazały, że szlak sygnałowy NF-κB jest zaangażowany w regulację proliferacji i migracji raka okrężnicy. W związku z tym można go wykorzystać do opracowania nowych i skutecznych środków terapeutycznych przeciwko rakowi jelita grubego [2].
W dziedzinie onkologii zrozumienie skomplikowanych procesów cyklu komórkowego, proliferacji i wzrostu oraz apoptozy ma fundamentalne znaczenie. Te funkcje biologiczne są kluczowe w badaniu ludzkich linii komórkowych, szczególnie tych pochodzących z komórek złośliwych, takich jak ludzkie komórki raka okrężnicy i modele raka trzustki. Na przykład linie komórkowe HCT116 i SW620 odgrywają kluczową rolę w badaniu mechanizmów leżących u podstaw odpowiednio raka okrężnicy i raka trzustki. Dzięki technikom takim jak cytometria przepływowa i testy klonogeniczne, naukowcy mogą wyjaśnić profile ekspresji genów i zachowanie niezależnych komórek w guzach, rzucając światło na sposób, w jaki rak komunikuje się w macierzy zewnątrzkomórkowej.
Rola apoptozy w progresji nowotworu
Apoptoza, czyli zaprogramowana śmierć komórki, odgrywa kluczową rolę w utrzymaniu homeostazy komórkowej i jest kluczowym obszarem badań w badaniach nad rakiem. Kluczowe znaczenie ma rozróżnienie między apoptozą niezwiązaną z nowotworem a apoptozą indukowaną specjalnie w kontekście raka, taką jak śmierć komórek raka okrężnicy. Proces ten nie polega jedynie na eliminacji komórek, ale obejmuje złożoną interakcję sygnałów, które mogą wpływać na wzrost guza i przerzuty. Badając apoptozę i śmierć komórek w połączeniu z supresorami przerzutów i aktywnością supresorów nowotworów, naukowcy mogą uzyskać wgląd w szlaki regulujące progresję raka i potencjał przerzutowy.
Przerzuty i markery molekularne w raku
Przerzuty pozostają jednym z najgroźniejszych aspektów raka, a przerzuty krwiotwórcze stanowią istotny problem w rozprzestrzenianiu się komórek złośliwych. Badanie przerzutów obejmuje badanie zdolności komórek nowotworowych do przemieszczania się i inwazji, czyli lokomocji komórek, oraz sposobu, w jaki komórki oddziałują z otoczeniem, w tym z macierzą zewnątrzkomórkową. Markery molekularne, takie jak ekspresja CD133 i receptor naskórkowego czynnika wzrostu, mają kluczowe znaczenie dla identyfikacji i zrozumienia zachowania pozytywnych komórek raka okrężnicy i innych typów nowotworów. Szlak SIRT6, na przykład, pojawił się jako obszar zainteresowania ze względu na jego potencjalną rolę w modulowaniu wzrostu guza i przerzutowego raka okrężnicy.
Toksykologia/rozwój leków
Linia komórkowa HCT116 jest wykorzystywana jako model przesiewowy dla nowych leków przeciwnowotworowych. Przeprowadzono szereg badań w celu oceny skuteczności i toksyczności leków przeciwnowotworowych, w tym produktów naturalnych i chemicznie syntetyzowanych nanocząstek. W związku z tym w badaniu oceniano cytotoksyczność zsyntetyzowanych nanocząstek srebra z ekstraktów leku ziołowego Caesalpinia pulcherrima w komórkach HCT116 [3]. W badaniu naukowcy wykorzystali linię komórek rakowych HCT116 do oceny potencjału przeciwnowotworowego wodnego ekstraktu z herbaty kakaowej. Stwierdzili, że ekstrakt z herbaty kakaowej zmniejsza proliferację raka okrężnicy i indukuje śmierć komórek [4]. Winnym badaniu wykorzystano komórki rakowe HCT116 i odkryto, że ekstrakty zziemniaka powietrznego, Dioscorea bulbifera, wykazują działanie proapoptotyczne w komórkach raka jelita grubego poprzez aktywację kaskady sygnałowej JNK i supresję genu ERK1/2 [5].
Wpływ metforminy na komórki nowotworowe, szczególnie w kontekście raka okrężnicy i trzustki, stanowi przykład tego, jak zrozumienie biologicznych funkcji komórek nowotworowych może prowadzić do potencjalnych strategii terapeutycznych. Badania nad przeżywalnością klonogenną lub zdolnością do tworzenia klonów komórek nowotworowych po leczeniu środkami takimi jak metformina lub ukierunkowanymi na określone szlaki, takie jak receptor naskórkowego czynnika wzrostu, mogą dostarczyć cennych informacji na temat skutecznych metod leczenia raka. Ponadto wykorzystanie klonów HCT116 i populacji komórek HCT116 w tych badaniach pozwala na lepsze zrozumienie, w jaki sposób komórki nowotworowe reagują na różne interwencje terapeutyczne, torując drogę do bardziej spersonalizowanego podejścia do leczenia raka.
Komórki HCT116: Publikacje badawcze
W tej sekcji omówimy kilka znaczących i najczęściej cytowanych ostatnich publikacji dotyczących linii komórkowej HCT116.
Badanie to zostało opublikowane w Journal of Photochemistry and Photobiology B: Biology (2017). Naukowcy wykorzystali linie komórkowe raka okrężnicy HCT116 i raka płuc A549 do oceny cytotoksycznego działania zsyntetyzowanych nanocząstek tlenku cyny z nasion piper nigrum.
Badania opublikowane w Cancer Letters (2018) sugerują, że lncRNA SNHG15 promuje migrację komórek raka okrężnicy w liniach komórkowych raka jelita grubego, w tym HCT116.
Nadekspresja długiego niekodującego RNA TUG1 promuje progresję raka jelita grubego
Artykuł ten został opublikowany w czasopiśmie Medical Science Monitor w 2016 roku. Badanie wykazało, że onkogenny LncRNA TUG1 promuje proliferację i migrację komórek raka okrężnicy HCT116.
Badanie opublikowane w czasopiśmie Biochemical Pharmacology (2018) sugeruje, że rozwój oporności na leki zwiększa poziom enzymów produkujących H2S w komórkach raka okrężnicy HCT116.
Ten artykuł badawczy w International Journal of Environmental Health Research (2023) sugeruje, że ekstrakt z Inula viscosa L. wywiera działanie przeciwnowotworowe na komórki raka jelita grubego HCT116 poprzez regulację mikroRNA.
Zasoby dotyczące komórek HCT116
Poniżej znajduje się kilka zasobów dotyczących komórek HCT116.
- Transfekcja HCT116: Ten film jest przewodnikiem krok po kroku dotyczącym transfekcji komórek nowotworowych HCT116.
- Hodowla linii komórkowej HCT116: Ten film przedstawia protokół subhodowli linii komórek raka okrężnicy HCT116.
- Subhodowla linii komórkowej HCT116: Ta strona internetowa zawiera wiele przydatnych informacji na temat podłoża hodowlanego HCT116. Ponadto zawiera procedury zamrażania, rozmrażania i subkulturowania komórek.
Często zadawane pytania dotyczące komórek HCT116
piśmiennictwo
- Waghela, B.N., F.U. Vaidya i C. Pathak: Regulacja w górę NOX-2 i Nrf-2 promuje oporność na 5-fluorouracyl w ludzkich komórkach raka okrężnicy (HCT-116). Biochemistry (Moskwa), 2021, 86, s. 262-274.
- Yang, M., et al., Astragalina hamuje proliferację i migrację ludzkich komórek raka okrężnicy HCT116 poprzez regulację szlaku sygnałowego NF-κB. Frontiers in Pharmacology, 2021, 12: s. 639256.
- Deepika, S., C.I. Selvaraj, and S.M. Roopan, Screening bioactivities of Caesalpinia pulcherrima L. swartz and cytotoxicity of extract synthesized silver nanoparticles on the HCT116 cell line. Materials Science and Engineering, C, 2020, 106, s. 110279.
- Gao, X., et al., Herbata kakaowa (Camellia ptilophylla) indukuje apoptozę zależną od mitochondriów w komórkach HCT116 poprzez generowanie ROS i szlak sygnałowy PI3K/Akt. Food Research International, 2020, 129, s. 108854.
- Hidayat, A.F.A., et al., Dioscorea bulbifera indukowała apoptozę poprzez hamowanie ERK 1/2 i aktywację szlaków sygnałowych JNK w ludzkich komórkach raka jelita grubego HCT116. Biomedicine & Pharmacotherapy, 2018. 104: p. 806-816.