후두암 연구에서의 간2 세포와 그 역할
간세포는 류마티스학, 암 연구, 면역학 등 생물의학 연구 분야에서 광범위하게 사용되는 중추적인 시험관 내 모델입니다. 후두암종에서 유래한 이 인간 세포는 후두 종양의 기원 조직과 특정 특성을 규명하는 데 필수적인 역할을 해왔습니다. 간세포의 중요성은 중개 암 연구에서 잘 알려져 있으며, 후두의 특성과 암의 기원에 대한 이해에 크게 기여하여 후두암 연구 논문에서 상당한 비중을 차지하고 있습니다[1].
2형 간염 세포의 기원과 일반적인 특성
세포주의 기원과 일반적인 특성은 연구에서의 적용 가능성을 결정합니다. 이 섹션에서는 Hep 2 세포의 기원과 몇 가지 두드러진 특징에 대해 알아볼 수 있습니다. 예를 들면 다음과 같습니다: HEp-2 세포주란 무엇인가요? 2형 간염 세포의 출처는 무엇인가요? 그리고 2형 간염의 형태는 무엇인가요?
- 불멸의 인간 상피 세포주인 Hep 2는 1954년 H.W. Toolan에 의해 후두암 세포로 처음 설명되었습니다. 그러나 최근에는 Hep 2 세포주가 자궁경부 선암 세포로 구성되어 있으며 헬라 세포주의 오염에서 비롯된 것으로 보고되고 있습니다[2].
- Hep 2 세포는 헬라 마커 염색체를 포함하고 있으며 면역 산화 효소 염색과 PCR을 통해 각각 케라틴 및 인유두종 바이러스 DNA 서열에 양성으로 확인되었습니다.
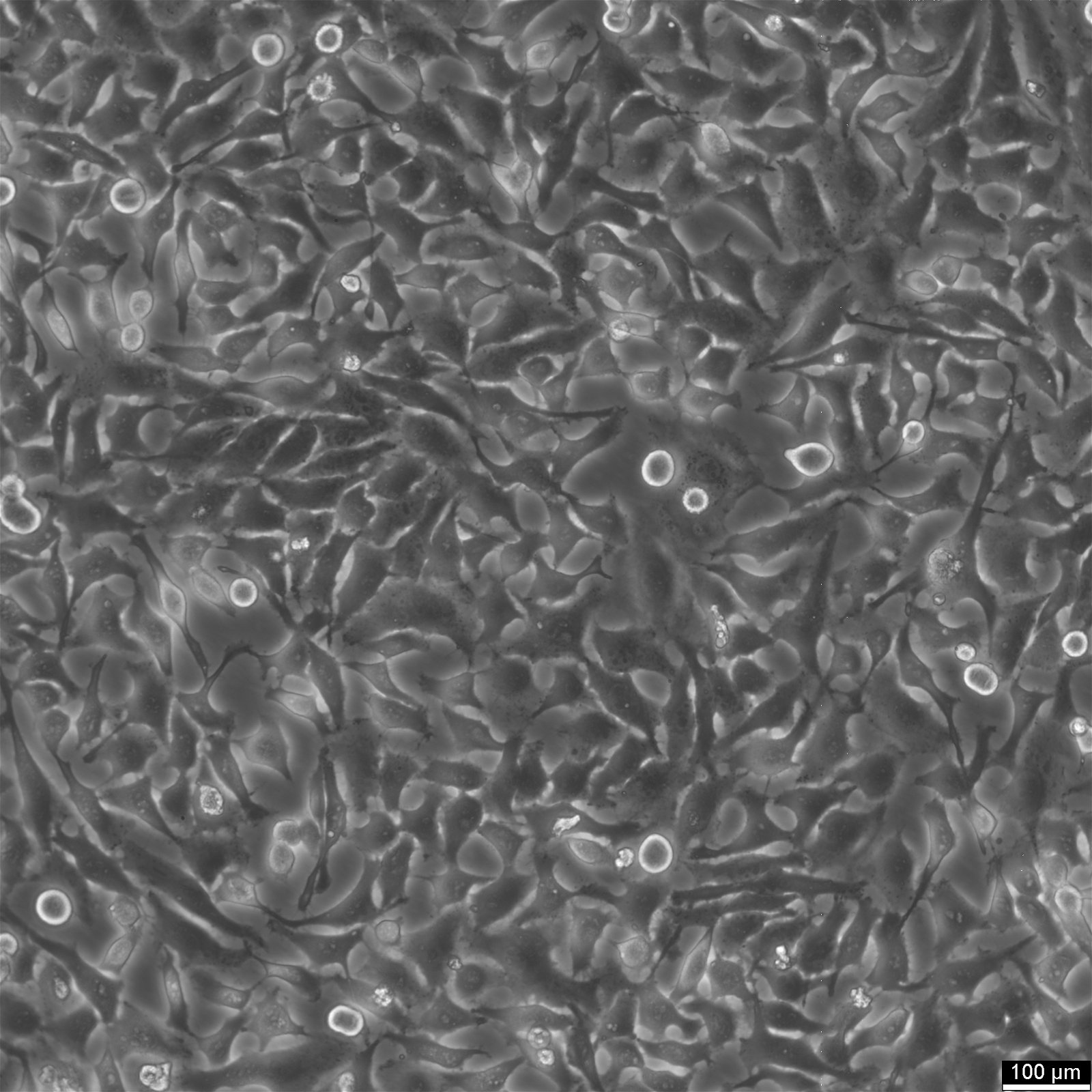
- 헬라 세포주 파생물 Hep 2는 상피세포와 유사한 형태를 가지고 있습니다.
- Hep 2 세포주는 거의 삼배체 핵형을 가진 구조적 및 수치적 염색체 결손을 모두 나타냅니다[3].
2형 간염 세포주: 배양 정보
세포주로 작업하기 전에 세포주 배양에 대한 다음 핵심 사항을 알아야 합니다. 이 정보는 세포주를 효과적으로 배양하고 유지하는 데 유용할 수 있습니다. 알아두어야 할 사항 HEp-2 세포의 배양 시간은 어떻게 되나요? Hep 2 세포는 부착성이 있나요? Hep2 세포의 시딩 밀도는 얼마인가요?
|
인구 배가 시간: |
Hep 2 세포에 대해 보고된 2배 증가 시간은 약 40시간입니다. |
|
부착 또는 정지 상태: |
Hep 2 세포는 부착되어 단층으로 성장합니다. |
|
시딩 밀도: |
1 x104 세포/cm2의 시딩 밀도는 Hep 2 세포 배양에 이상적입니다. 시딩을 위해 부착된 Hep 2 세포를 1 x PBS 용액으로 헹군 다음, Accutase 해리 용액으로 배양합니다. 실온에서 8~10분 배양 후 세포를 배지에 재부유하고 원심분리합니다. 그런 다음 수집된 세포를 새로운 배지에 분배하고 배양을 위해 새 플라스크에 붓습니다. |
|
성장 배지: |
Hep 2 세포 배양에는 EMEM 또는 Eagle의 최소 필수 배지를 사용합니다. 이 배지에는 이상적인 세포 성장을 위해 10% FBS, 1.0g/L 포도당, 2.2g/L NaHCO3, 2.0mM L-글루타민, 1% NEAA, 1mM 피루브산 나트륨이 보충되어 있습니다. 배지는 일주일에 2~3회 교체해야 합니다. |
|
성장 조건: |
다른 포유류 세포주와 마찬가지로 Hep 2도 37°C의 온도와 5%의 CO2가 지속적으로 공급되는 가습 인큐베이터에서 배양합니다. |
|
보관: |
Hep 2 세포는 초저온 전기 냉동고(-150°C 이하)에 보관하거나 액체 질소 증기상에 보관하여 장기 보관할 수 있습니다. |
|
동결 과정 및 매체: |
Hep 2 세포에 권장되는 냉동 매체는 CM-1 또는 CM-ACF입니다. 세포는 온도를 1°C씩 서서히 떨어뜨리고 세포 생존력을 보호할 수 있는 저속 냉동 프로세스를 사용하여 냉동해야 합니다. |
|
해동 과정: |
냉동된 세포 바이알을37°C의수조에서 작은 얼음 덩어리가 남을 때까지 교반하여 빠르게 해동합니다. 그런 다음 세포를 신선한 배지에 추가하고 원심분리하여 동결 배지 성분을 제거합니다. 그 후 세포 펠릿을 배지에 다시 부유시키고 세포를 배양 플라스크에 분배합니다. 세포가 부착하려면 거의 24시간 동안 휴식을 취해야 합니다. |
|
생물학적 안전 수준 |
2형 간염 세포 배양의 취급 및 유지 관리에는 생물안전 레벨 1 실험실을 권장합니다. |
2형 간염 세포의 장점과 한계
거의 모든 세포주는 연구 분야에서 사용되는 데 기여하는 장점과 한계가 고유하게 조합되어 있습니다. 이 섹션에서는 Hep 2 세포주와 관련된 몇 가지 주요 장단점을 설명합니다.
장점
Hep 2 세포주의 주요 장점은 다음과 같습니다:
- 인간 유래: Hep 2는 인간 상피 세포에서 유래하여 인간 질병 및 바이러스 감염을 연구하는 데 유용한 시험관 내 모델입니다
- ANA 검출: Hep 2 세포주는 수많은 항원을 나타내는 고유 단백질 배열을 보유하고 있어 항핵 항체(ANA) 검출에 탁월한 기질입니다. 이 기능을 통해 혈청 내 ANA를 특이적이고 매우 민감하게 스크리닝할 수 있으므로 결합 조직 질환을 식별하는 데 중요한 진단 도구로 사용할 수 있습니다
제한 사항
- 염색체 이상: 2형 간염 세포는 여러 가지 수치적 및 구조적 염색체 이상을 나타냅니다. 이러한 이상은 세포 행동에 영향을 미칠 수 있으며 특정 실험실 실험에서 적용 가능성을 제한할 수 있습니다
- 종양원성: 종양 유래 인간 상피 세포주인 Hep 2는 일반적으로 상피 세포에 없는 유전적 이상을 가지고 있을 수 있습니다. 따라서 정상적인 세포 생리학에 초점을 맞춘 특정 연구에서는 Hep 2 세포의 사용이 제한될 수 있습니다.
생의학 연구에서의 Hep 2 세포주 활용 확대
Hep 2 세포주는 생의학 연구의 다양한 응용 분야에서 모범적인 모델로 각광받고 있습니다. 다용도로 잘 알려진 이 세포는 수용체 분석부터 복잡한 질병 연구에 이르기까지 체외 실험에서 중요한 역할을 합니다.
간세포를 이용한 종양 유발 기전 및 치료 표적 탐색
간세포 2형 세포는 종양 생성 능력이 있어 복잡한 암 생물학을 탐구하는 데 중추적인 역할을 합니다. 간세포는 암 신호 전달 경로와 메커니즘 연구에 대한 인사이트를 제공하며, 항암제 선별 및 평가의 중심이 됩니다. 예를 들어, 한 통찰력 있는 연구에서는 Hep 2를 활용하여 miRNA-33a가 암세포 증식에 미치는 영향을 설명했습니다. 이 연구 결과는 알려진 발암 유전자인 PIM1과의 상호작용을 통해 miRNA-33a의 항증식 효과를 조명하여 새로운 치료 표적을 제시했습니다[4]. 또 다른 사례로, Hep 2는 마르스데니아 테나시시마 산화아연 나노입자의 치료 잠재력을 평가하는 데 사용되어 항증식 및 세포사멸 효능을 강조했습니다 [5].
2형 간염 세포 인사이트를 통한 바이러스학 연구 발전
다양한 인간 바이러스에 대한 간세포의 감수성으로 인해 간세포는 바이러스학 연구에서 매우 귀중한 자원이 되고 있습니다. 이 세포는 바이러스와 숙주 세포 메커니즘 사이의 복잡한 상호 작용을 밝히기 위해 SARS-CoV-2 바이러스 유전자의 발현에 효과적으로 사용되었습니다[6]. 이러한 응용은 코로나19와 같은 바이러스 감염을 이해하고 퇴치하는 것이 전 세계적으로 최우선 과제인 현시점에서 특히 중요합니다.
세포 기능 해독: 2형 간염 세포의 유전자 조작
유전자 조작에 대한 Hep 2 세포주의 적응성은 기계론적 연구에서 그 유용성을 강조합니다. 연구자들은 유전자 발현을 조절하고 세포 기능에서 특정 유전자의 역할을 규명하기 위해 이 기능을 활용합니다. 주목할 만한 연구로는 간 2형 세포에서 RNA 결합 단백질 RBM6의 과발현을 통해 종양 억제 가능성을 조사하여 암의 분자적 토대에 대한 귀중한 통찰력을 제공한 연구가 있습니다[7].
2형 간염 세포주 애플리케이션을 통한 질병 진단 강화
이러한 연구 분야 외에도 Hep 2 세포는 특히 전신성 홍반성 루푸스와 같은 자가면역질환 진단에 중요한 ANA를 검출하는 데 있어 진단 능력으로 호평을 받고 있습니다. 간2 세포가 ANA를 정확하게 검출할 수 있기 때문에 자가면역 병리에 대한 이해를 높이고 환자 치료를 개선하여 표적 치료의 진단과 개발을 지원합니다.
이러한 다양한 응용을 통해 간 2 세포는 중개 암 연구, 바이러스 감염 연구 및 세포 메커니즘 탐구의 발전에 크게 기여해 왔습니다. 임상 관련 데이터 생성에 대한 기여는 매우 중요하며, 실험실과 임상 모두에서 없어서는 안 될 필수적인 역할임을 확인시켜 줍니다. 연구가 계속 발전함에 따라 Hep 2 세포주는 새로운 치료법을 발견하고 인간의 건강과 질병에 대한 지식을 넓히는 데 도움을 주며 앞으로도 선두에 서게 될 것입니다.
지금 바로 HEp-2 세포주 확보하기
2형 간염 세포: 연구 출판물
다음은 간세포 2형에 관한 흥미롭고 가장 많이 인용된 연구 논문입니다.
- 후두암 세포(Hep-2)에서 세포 증식을 억제하고 세포 사멸을 유도하는 마스데니아 테나시시마의 산화아연 나노입자 합성
광화학 및 광생물학 저널 B: 생물학(2019)에 게재된 이 논문은 Hep 2 세포주에서 생합성된 마스데니아 테나시시마 산화아연 나노입자의 항암 잠재력을 탐구했습니다. - 생합성 헤스페리딘이 탑재된 PLGA 나노입자는 암세포의 미토콘드리아 매개 내재적 세포 사멸 경로에 대응합니다
이 논문은 2021년 무기 및 유기 금속 고분자 및 재료 저널에 게재되었습니다. 이 연구는 헤스페리딘이 함유된 바이오 제형 폴리(락틱-코-글리콜산)(PLGA) 나노입자의 항암 특성을 간세포 2형 세포에서 조사했습니다. - 호흡기 세포융합 바이러스 감염에 대한 로파더룸 그라실 에탄올 추출물의 항바이러스 활성
2019년 민족약리학 저널에 게재된 이 논문은 호흡기 세포융합 바이러스 감염을 연구하고 이에 대한 항바이러스 약물을 선별하기 위해 간2 세포를 사용했습니다. 이 연구에서는 호흡기 세포융합 바이러스 감염에 대한 약용 식물, 즉 로파더룸 그라실(Lophatherum gracile)의 에탄올 추출물의 유망한 항바이러스 잠재력을 보고했습니다. - 인간 HEp-2 상피 세포에 대한 칸디다 알비칸스 부착에 대한 4가지 방향성 식물의 수성 추출물 활성 평가
이 연구는 Gene Reports(2020)에 게재되었습니다. 이 연구는 네 가지 아로마 식물의 수성 추출물이 인간 간세포(Hep 2) 상피세포에 대한 칸디다 알비칸스의 부착을 억제하는 잠재력을 탐구한 연구입니다. - Wnt1 유도 신호 단백질 1은 YAP1/TEAD1/GLUT1 경로를 통해 후두 편평 세포 암종의 해당 작용과 화학 저항성을 조절합니다
이 연구는 2019년 세포 생리학 저널에 게재되었습니다. 이 연구에서는 Wnt1 유도 신호 단백질 1(WISP1)이 YAP1/TEAD1/GLUT1 경로와 상호작용하여 Hep 2 세포주에서 포도당 대사와 화학 저항성을 조절한다고 보고합니다.
Hep2 세포주에 대한 리소스: 프로토콜, 비디오 등
Hep 2는 잘 알려진 세포주입니다. Hep 2 세포주를 다루는 여러 리소스를 이용할 수 있습니다.
- Hep2 세포주 하위 배양: 이 동영상은 Hep 2 세포 하위 배양에 대한 단계별 가이드입니다.
- 2형 간염 세포 ANA 스크리닝: 이 동영상에서는 Hep 2 세포주를 사용한 항핵항체(ANA) 스크리닝에 대해 설명합니다.
- Hep 2 배양: 이 링크에는 Hep 2 세포에 대한 기본적인 세포 배양 정보가 포함되어 있습니다. 여기에는 세포 분할, 세포 동결 및 해동이 포함됩니다.
생물의학 연구에서 HEp-2 세포에 대해 자주 묻는 질문
참고 문헌
- 푸시, M. 및 S. 도티, HEp-2 세포주를 완전히 동물이 없는 배양 시스템에 적용하고 세포 성장의 실시간 분석. 생명 공학, 2021. 70(6): p. 319-326.
- 고르페, P., 후두암에 대한 중개 연구에서 Hep-2 세포주에 대한 포괄적인 검토. Am J Cancer Res, 2019. 9(4): p. 644-649.
- Wang, M., 외, 인간 HEp-2 확립 후두 이종 이식 종양에서 암 관련 섬유 아세포는 상피 간엽 전이를 통해 암 세포에서 유래하지 않으며 표현형 적으로 활성화되지만 핵형 적으로 정상입니다. PLoS One, 2015. 10(2): p. E0117405.
- 카라타스, O.F., PIM1 표적을 통한 후두암 Hep-2 세포에서 miR-33a의 항증식성 잠재력. Head Neck, 2018. 40(11): p. 2455-2461.
- 왕, Y., 외., 후두암 세포(Hep-2)에서 산화아연 나노입자의 합성은 세포 증식을 억제하고 세포 자멸사를 유도합니다(Marsdenia tenacissima에서 산화아연 나노입자의 합성). 광화학 및 광생물학 저널 B: 생물학, 2019. 201: p. 111624.
- Zhang, J., 외., SARS-CoV-2 단백질의 세포 내 국소화에 대한 체계적 및 분자적 연구. 신호 전달 표적 Ther, 2020. 5(1): p. 269.
- Wang, Q., 외., 종양 억제 유전자로서의 RNA 결합 단백질 RBM6는 후두암의 성장과 진행을 억제합니다. 유전자, 2019. 697: p. 26-34.