Hep2細胞と喉頭癌研究におけるその役割
Hep2細胞は、リウマチ学、癌研究、免疫学などの生物医学研究領域で広く使用されている重要なin vitroモデルである。喉頭癌に由来するこのヒト細胞は、喉頭新生物の発生組織や特異的形質を解明する上で不可欠である。その重要性は、トランスレーショナルな癌研究においてよく認識されており、喉頭癌の性質と癌の起源に関する我々の理解に大きく貢献しており、喉頭癌の研究発表においてかなりの存在感を示している[1]。
Hep 2細胞の起源と一般的特徴
細胞株の起源と一般的特徴は、研究への応用可能性を規定する。このセクションでは、Hep 2細胞の起源といくつかの顕著な特徴について知るのに役立ちます。例えばHEp-2細胞株とは何か?Hep 2細胞の供給源は?Hep 2の形態は?
- Hep 2は不死性のヒト上皮細胞株で、1954年にH.W. Toolanによって喉頭癌細胞として初めて報告された。しかし最近では、Hep 2細胞株は子宮頸部腺がん細胞から構成され、Hela細胞株の混入に由来することが報告されている[2]。
- Hep 2細胞はHelaマーカー染色体を含み、免疫ペルオキシダーゼ染色とPCRでそれぞれ確認されたケラチンとヒトパピローマウイルスのDNA配列に陽性であることが判明している。
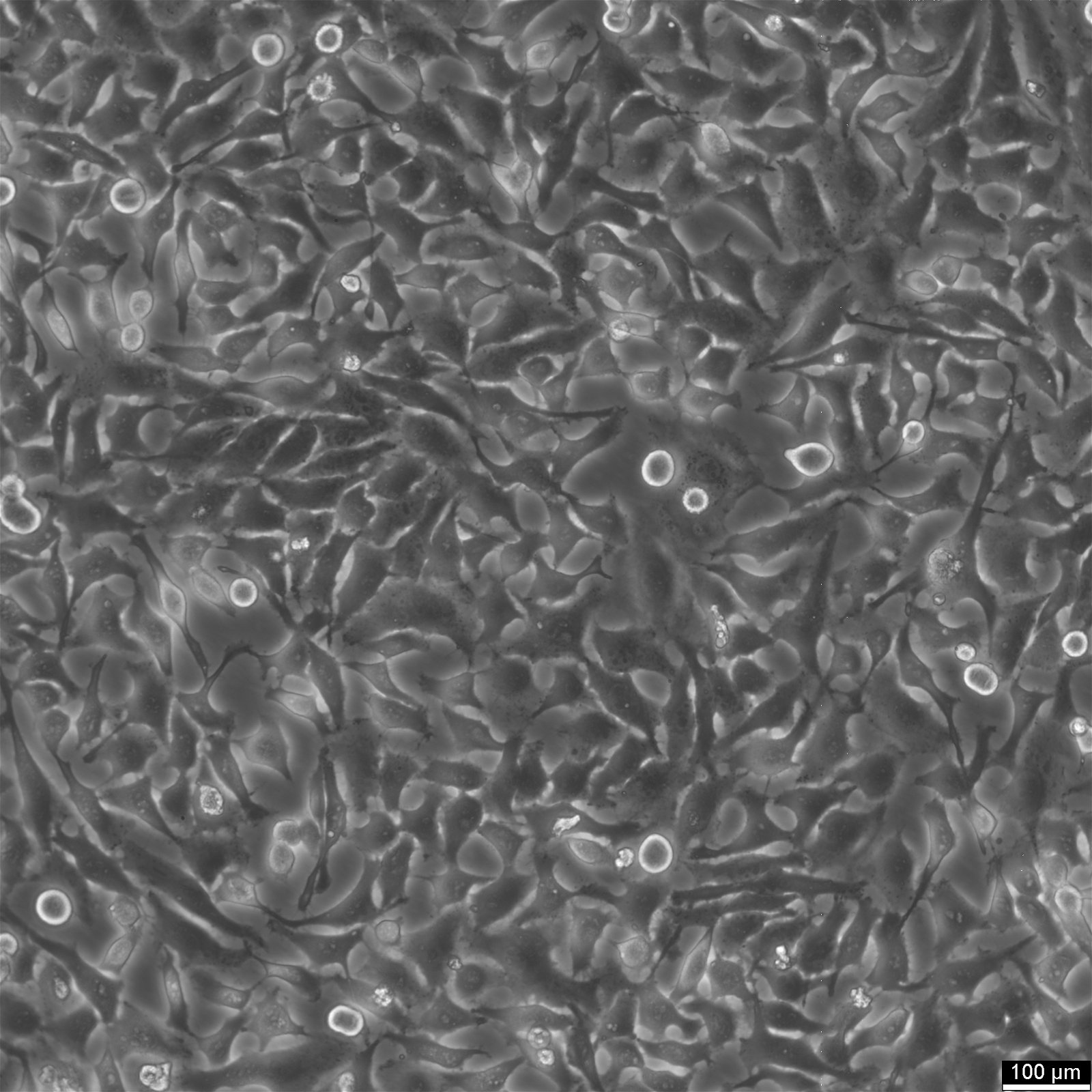
- Hela細胞株誘導体Hep 2は上皮様形態を有する。
- Hep 2細胞株は、ほぼ3倍体の核型を持つ構造的および数的染色体擦過傷を示す[3]。
Hep 2 細胞株培養に関する情報
細胞株を使用する前に、その培養に関する以下の要点を 知っておく必要がある。この情報は、細胞株を効果的に培養し、維持するために有用である。知っておくべきことHEp-2細胞の倍加時間は?Hep 2細胞は接着するか?Hep2細胞の播種密度はどのくらいですか?
|
細胞倍加時間: |
Hep 2細胞で報告されている倍加時間は約40時間です。 |
|
接着性か懸濁状態か: |
Hep 2細胞は接着性で、単層に増殖する。 |
|
播種密度: |
Hep 2細胞の培養には、1 x104 cells/cm2の播種密度が理想的である。播種には、接着したHep 2細胞を1 x PBS溶液でリンスし、続いてAccutase解離液でインキュベートします。周囲温度で8~10分間インキュベートした後、細胞を培地に懸濁し、遠心分離する。回収した細胞は新鮮な培地に分注し、培養用の新しいフラスコに流し込む。 |
|
増殖培地: |
Hep 2細胞の培養にはEMEMまたはEagle's minimal essential mediumを用いる。この培地には、理想的な細胞増殖のために、10% FBS、1.0 g/Lグルコース、2.2 g/L NaHCO3、2.0 mM L-グルタミン、1% NEAA、および1 mM ピルビン酸ナトリウムが添加されている。培地は週に2~3回更新する。 |
|
増殖条件: |
他の哺乳類細胞株と同様、Hep 2も37℃、5%CO2を連続供給する加湿インキュベーター内で培養する。 |
|
保存: |
Hep 2細胞は、超低温電気冷凍庫(-150℃以下)または液体窒素気相中で長期保存が可能である。 |
|
凍結プロセスと培地 |
Hep 2細胞に推奨される凍結培地はCM-1またはCM-ACFである。細胞は、徐々に1℃ずつ温度を下げ、細胞の生存性を保てるような緩慢な凍結プロセスを用いて凍結させる。 |
|
解凍プロセス: |
凍結した細胞バイアルを、37℃のウォーターバスで撹拌しながら、小さな氷の塊が残るまで速やかに融解する。その後、細胞を新鮮な培地に加え、遠心分離して凍結培地成分を除去する。その後、細胞ペレットを培地に再懸濁し、培養フラスコに分注する。細胞を接着させるには、ほぼ24時間休ませる必要がある。 |
|
バイオセーフティーレベル |
Hep 2細胞培養の取り扱いと維持管理には、バイオセーフティレベル1の実験室が推奨される。 |
Hep 2細胞の利点と限界
ほとんど全ての細胞株は、研究分野での使用に寄与する長所と短所のユニークな組み合わせを示す。このセクションでは、Hep 2細胞株に関連するいくつかの主な長所と短所について述べる。
長所
Hep 2細胞株の主な長所は以下の通りである:
- ヒト由来:Hep 2はヒト上皮細胞由来であるため、ヒトの疾患やウイルス感染を研究するための貴重なin vitroモデルである。
- ANA検出:Hep 2細胞株は、多数の抗原を提示するネイティブなタンパク質アレイを有しており、抗核抗体(ANA)を検出するための優れた基質となっている。この特徴により、血清中のANAを特異的かつ高感度にスクリーニングすることができ、結合組織疾患を同定するための重要な診断ツールとなる。
制限事項
- 染色体異常:Hep 2細胞は、複数の数値的および構造的な染色体異常を示す。これらの異常は細胞の挙動に影響を与える可能性があり、特定の実験室での実験には適用できない可能性がある。
- 腫瘍原性:腫瘍由来のヒト上皮細胞株であるHep 2は、上皮細胞には通常見られない遺伝子異常を持っている可能性がある。その結果、正常な細胞生理に焦点を当てた特定の研究においては、Hep 2細胞の使用が制限される可能性がある。
生物医学研究におけるHep 2細胞株の応用拡大
Hep 2細胞株は、生物医学研究における多くの応用のための模範的モデルとして際立っている。汎用性の高さで知られるこの細胞は、受容体の解析から複雑な疾患の研究に至るまで、in vitro実験において重要な役割を果たしている。
Hep 2細胞を用いた腫瘍形成メカニズムと治療標的の探索
Hep 2細胞は腫瘍原性であるため、がん生物学の複雑さを掘り下げる上で極めて重要である。Hep 2細胞は、がんのシグナル伝達経路やメカニズムに関する洞察を提供し、抗がん剤のスクリーニングや評価における主役である。例えば、がん細胞の増殖に対するmiRNA-33aの影響を明らかにするためにHep 2を利用した洞察に満ちた研究がある。その結果、癌遺伝子として知られるPIM1との相互作用を通じてmiRNA-33aの抗増殖作用が明らかになり、新たな治療標的が示唆された[4]。別の例では、マースデニア・テナシッシマ酸化亜鉛ナノ粒子の治療可能性を評価するためにHep 2が使用され、その抗増殖およびアポトーシス効果を強調した [5]。
Hep 2細胞の知見によるウイルス学研究の進展
Hep 2細胞は様々なヒトウイルスに感受性があるため、ウイルス学研究において貴重なリソースとなっている。Hep 2細胞はSARS-CoV-2ウイルス遺伝子の発現に効果的に利用され、ウイルスと宿主細胞メカニズムの複雑な相互作用を解明している[6]。この応用は、COVID-19のようなウイルス感染症の理解と対策が世界的な優先課題となっている現代において、特に重要である。
細胞機能の解読:Hep 2細胞における遺伝子操作
Hep 2細胞株の遺伝子操作に対する適応性は、メカニズム研究におけるその有用性を強調している。研究者はこの特徴を利用して遺伝子発現を調節し、細胞機能における特定の遺伝子の役割を解明している。注目すべき研究では、RNA結合タンパク質RBM6をHep 2細胞で過剰発現させることで、そのがん抑制能を調べ、がんの分子基盤に関する貴重な知見を提供した [7]。
Hep 2細胞株の応用による疾患診断の強化
これらの研究領域を超えて、Hep 2細胞はその診断能力、特に全身性エリテマトーデスのような自己免疫疾患の診断に重要なANAの検出で高く評価されている。Hep 2細胞がANAを正確に提示できることは、診断や標的治療の開発をサポートし、自己免疫病態の理解を深め、患者のケアを向上させる。
こうした多様な応用を通じて、Hep2細胞は、トランスレーショナルな癌研究、ウイルス感染研究、細胞メカニズムの探求の進歩に大きく貢献してきた。臨床に関連したデータの生成に対するHep2細胞の貢献は非常に貴重であり、研究室と臨床の両方におけるHep2細胞の不可欠な役割を裏付けている。研究が進化し続ける中、Hep2細胞株は最前線に立ち続け、新たな治療法の発見を助け、ヒトの健康と病気に関する知識を広げていくに違いない。
今すぐHEp-2細胞株を確保
Hep 2細胞研究発表
以下は、Hep 2細胞に関する興味深い研究発表で、最も引用されているものです。
- マースデニア・テナシッシマからの酸化亜鉛ナノ粒子の合成は、喉頭癌細胞(Hep-2)の細胞増殖を阻害し、アポトーシスを誘導する
Journal of Photochemistry and Photobiology B: Biology (2019)に掲載されたこの論文は、Hep 2細胞株において、生合成されたマースデニア・テナシッシマ酸化亜鉛ナノ粒子の抗がんポテンシャルを探索した。 - バイオフォーミュレートされたヘスペリジン担持PLGAナノ粒子は、がん細胞におけるミトコンドリア媒介内在性アポトーシス経路に対抗する
この論文は2021年にJournal of Inorganic and Organometallic Polymers and Materialsに掲載された。本研究は、ヘスペリジンを担持したポリ乳酸(PLGA)ナノ粒子のHep 2細胞における抗がん作用を検討した。 - 呼吸器合胞体ウイルス感染に対するLophatherum gracileのエタノール抽出物の抗ウイルス活性
2019年のJournal of Ethnopharmacology誌に掲載されたこの論文は、Hep 2細胞を用いて呼吸器合胞体ウイルス感染を研究し、それに対する抗ウイルス薬をスクリーニングした。この研究は、呼吸器合胞体ウイルス感染に対する薬用植物すなわちLophatherum gracileのエタノール抽出物の有望な抗ウイルス性を報告した。 - ヒトHEp-2上皮細胞へのカンジダ・アルビカンス付着に対する4種の芳香植物水性エキスの活性評価
この研究はGene Reports誌(2020年)に掲載された。本研究は、ヒトHep2上皮細胞へのカンジダ・アルビカンスの接着に対する4種の芳香植物の水性抽出物の阻害能を探索した。 - Wnt1誘導性シグナルタンパク質1がYAP1/TEAD1/GLUT1経路を介して喉頭扁平上皮がんの解糖と化学療法抵抗性を制御する
この研究は、2019年のJournal of Cellular Physiology誌に掲載された。この研究は、Wnt1-inducible signalling protein 1(WISP1)がYAP1/TEAD1/GLUT1経路と相互作用し、Hep 2細胞株における糖代謝と化学療法抵抗性を制御することを報告している。
Hep2細胞株のリソース:プロトコル、ビデオ、その他
Hep 2はよく知られた細胞株である。Hep 2細胞株を特集した利用可能なリソースがいくつかあります。
- Hep2細胞株のサブカルチャー: このビデオはHep 2細胞のサブカルチャーをステップバイステップで説明しています。
- Hep 2細胞のANAスクリーニング: Hep 2細胞株を用いた抗核抗体(ANA)スクリーニングについて説明したビデオです。
- Hep 2の培養 このリンクには、Hep 2細胞に関する基本的な細胞培養情報が含まれています。細胞分割、細胞凍結、解凍が含まれます。
生物医学研究におけるHEp-2細胞に関するよくある質問
参考文献
- Fusi, M. and S. Dotti, HEp-2細胞株の完全非動物性培養系への適応と細胞増殖のリアルタイム解析。Biotechniques, 2021.70(6): p. 319-326.
- Gorphe, P., A comprehensive review of Hep-2 cell line in translational research for laryngeal cancer.Am J Cancer Res, 2019.9(4): p. 644-649.
- Wang, M., et al., ヒトHEp-2樹立喉頭異種移植腫瘍における癌関連線維芽細胞は、上皮間葉転換を経た癌細胞由来ではなく、表現型的には活性化されているが核型的には正常である。PLoS One, 2015.10(2): p. e0117405.
- Karatas, O.F., PIM1を標的とした喉頭がんHep-2細胞におけるmiR-33aの抗増殖能。Head Neck, 2018.40(11): p. 2455-2461.
- Wang, Y., et al., Synthesis of Zinc oxide nanoparticles from Marsdenia tenacissima inhibits the cell proliferation and induces apoptosis in laryngeal cancer cells (Hep-2).Journal of Photochemistry and Photobiology B: Biology, 2019.201: p. 111624.
- Zhang, J., et al., A systemic and molecular study of subcellular localization of SARS-CoV-2 proteins.Signal Transduct Target Ther, 2020.5(1): p. 269.
- Wang, Q., et al., RNA結合タンパク質RBM6は、喉頭癌の増殖と進行を抑制する癌抑制遺伝子である。Gene, 2019.697: p. 26-34.