U2OS-CRISPR-SNAPf-SEH1 细胞
一般信息
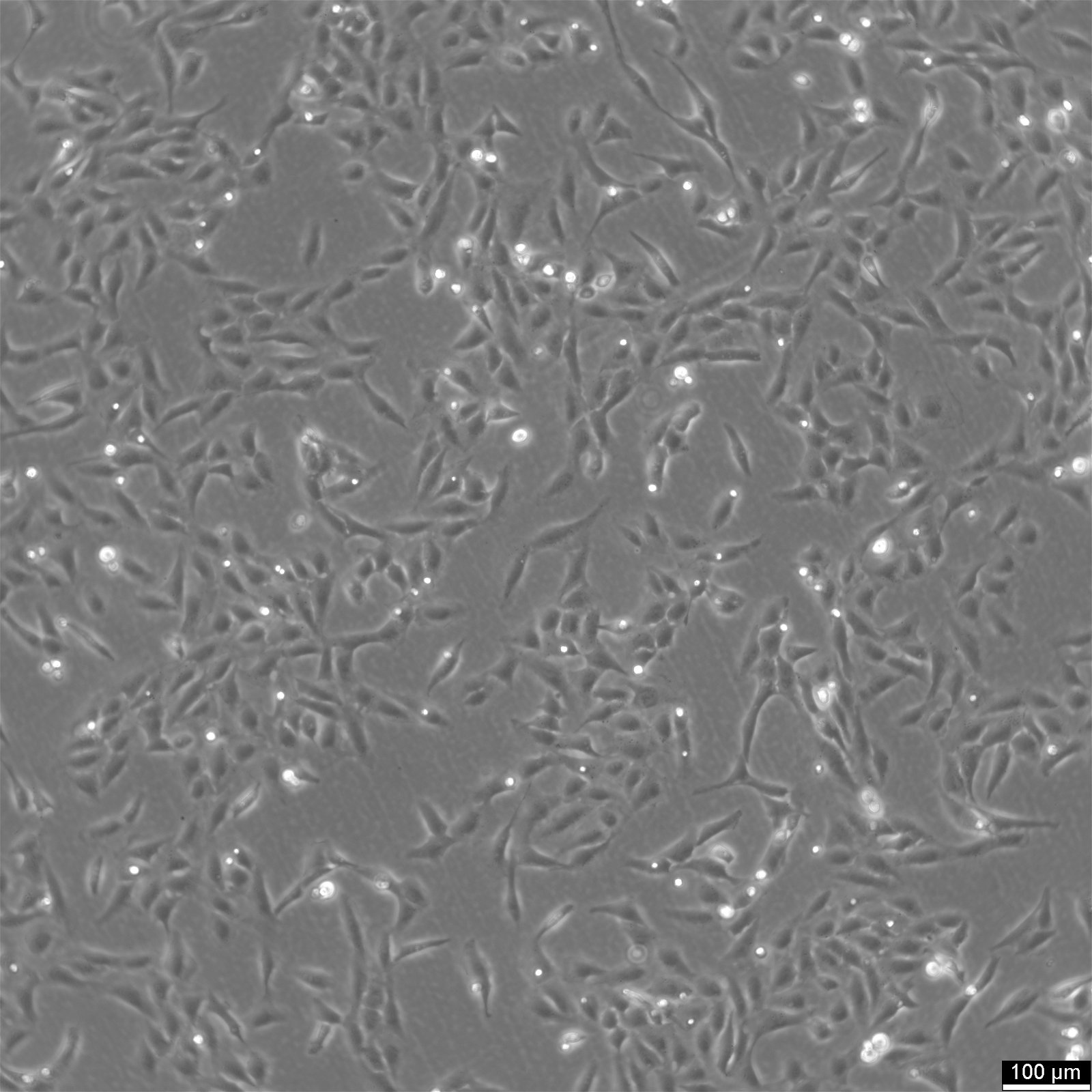
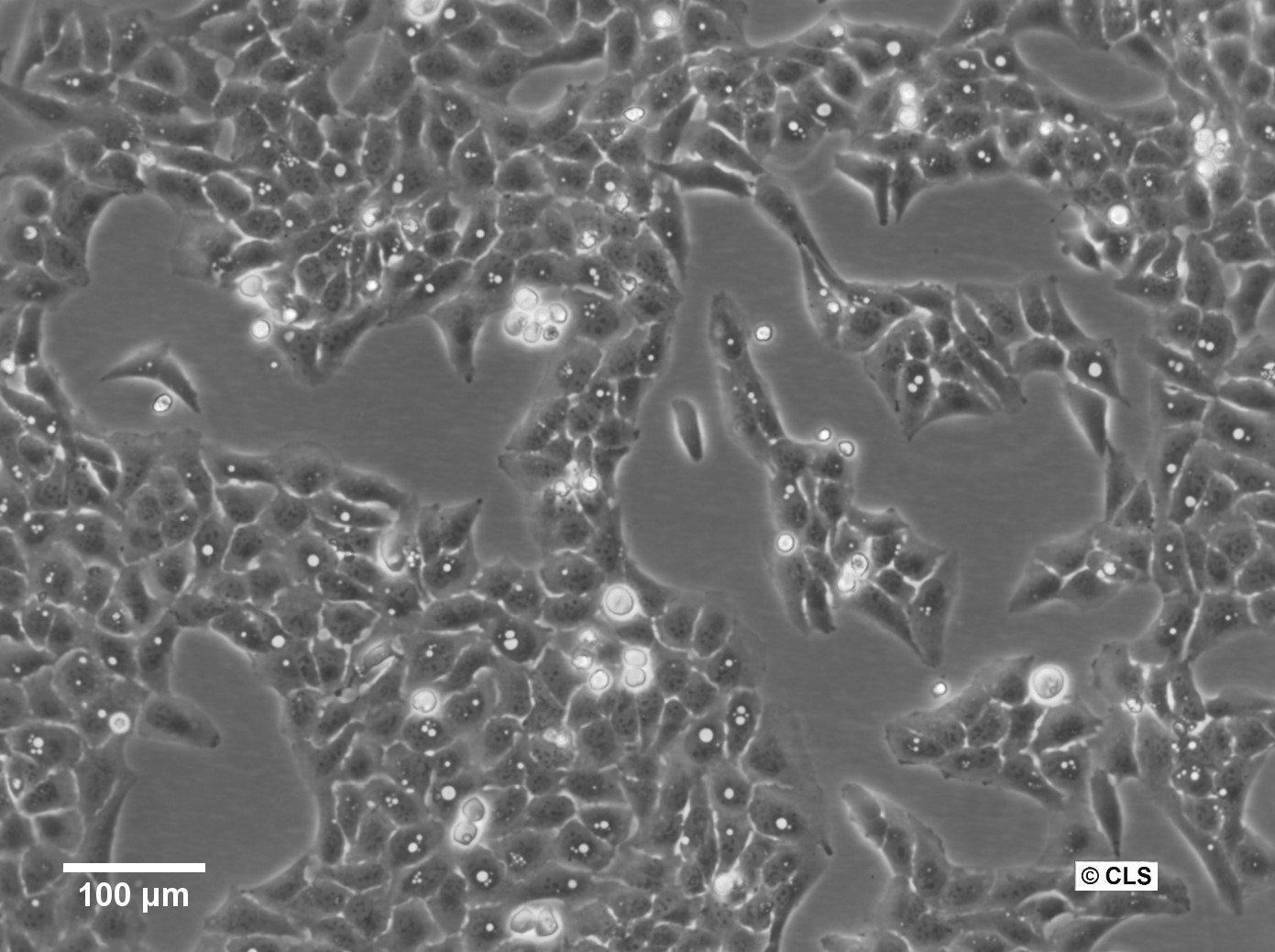
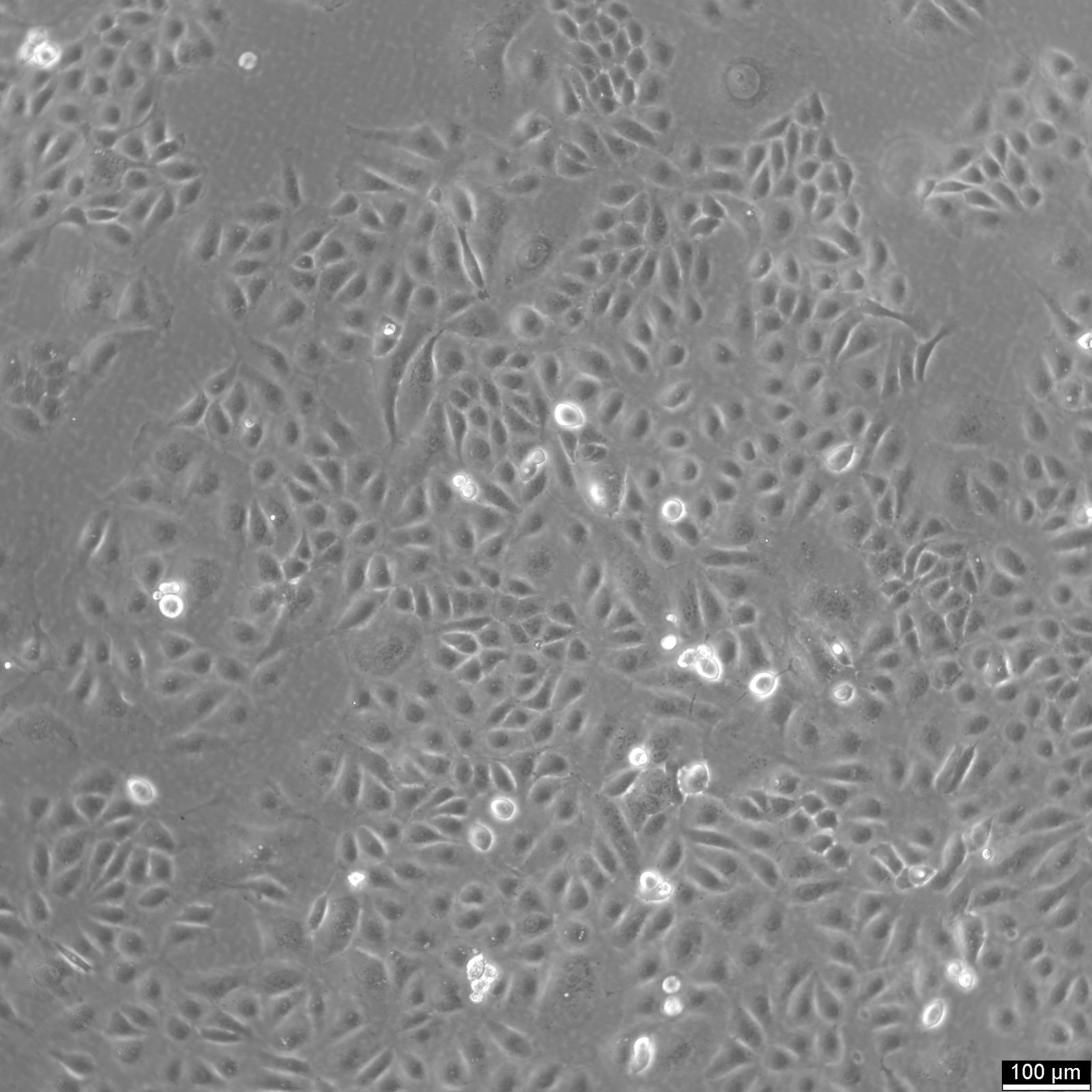
| 说明 | U2OS-CRISPR-SNAPf-SEH1是一种基因组编辑的人类骨肉瘤细胞系,源自U2OS细胞。该细胞系通过CRISPR/Cas9技术对内源性SEH1L(SEH1)基因进行修饰,使其编码一个同框SNAPf标签。 SEH1是Y复合体(又称NUP107-160复合体)的组成部分,该复合体作为核孔复合体(NPC)的核心结构单元,参与孔架组装与稳定性维持。通过在内源性基因座插入SNAPf编码序列,标记的SEH1蛋白在天然调控机制下表达,既保持生理表达水平又最大限度减少对核孔组成的干扰。 SNAPf标签是经工程改造的SNAP标签快速反应变体,可共价结合苄基鸟嘌呤偶联底物,实现活细胞或固定细胞中选择性稳定的荧光标记。在U2OS-CRISPR-SNAPf-SEH1细胞中,融合蛋白以NPC分布特有的点状模式定位于核膜。 由于标记发生在内源性蛋白水平,该系统特别适用于定量荧光显微镜、超分辨成像及单粒子追踪分析,可深入解析核孔复合体的组织结构与化学计量比。U2OS细胞扁平形态与大核特性进一步促进了核膜结构的高分辨率可视化。 SEH1参与核孔复合体生物合成,并被证实与有丝分裂期间着丝粒相关过程有关。因此,该细胞系为研究细胞周期依赖性核孔复合体组装与解聚、孔架结构内Y复合体的空间组织、以及SEH1在核膜与有丝分裂着丝粒上的潜在双重作用提供了可靠平台。 U2OS-CRISPR-SNAPf-SEH1细胞系可在生理相关表达条件下,实现核孔结构与动态机制的研究。 |
|---|---|
| 有机体 | 人类 |
| 组织 | 骨质 |
| 疾病 | 骨肉瘤 |
特点
| 年龄 | 15 年 |
|---|---|
| 性别 | 女性 |
| 种族 | 高加索人 |
| 形态学 | 上皮样 |
| 生长特性 | 附着物 |
监管数据
| 引用 | U2OS-CRISPR-SNAPf-SEH1(Cytion 目录号 300664) |
|---|---|
| 生物安全等级 | 1 |
| NCBI_TaxID | 9606 |
| 存款人 | 艾伦伯格实验室(EMBL) |
| 转基因生物现状 | GMO-S1:这种人类骨肉瘤细胞系(U2OS-CRISPR-SNAPf-SEH1)含有 CRISPR 介导的 SNAPf-SEH1 融合,可对 SEH1 核蛋白进行选择性标记。这种修饰是稳定存在的。本分类仅适用于德国国内,其他地区可能有所不同。 |
生物分子数据
| 蛋白质表达 | SEH1、SNAPf 标记 |
|---|
处理
| 培养基 | McCoys 5a,w:3.0 克/升葡萄糖,w:稳定谷氨酰胺,w:2.0 毫摩尔丙酮酸钠,w:2.2 克/升 NaHCO3(Cytion 文章编号 820200a)。 |
|---|---|
| 补充剂 | 在培养基中添加 10% FBS、3.0 g/L 葡萄糖、稳定的谷氨酰胺、2.0 mM 丙酮酸钠、2.2 g/L NaHCO3、1% NEAA |
| 解离试剂 | Accutase |
| 亚培养 | 去除粘附细胞上的旧培养基,用不含钙和镁的 PBS 冲洗。T25 烧瓶用 3-5 毫升 PBS,T75 烧瓶用 5-10 毫升。然后用 Accutase 完全覆盖细胞,T25 烧瓶用 1-2 毫升,T75 烧瓶用 2.5 毫升。让细胞在室温下孵育 8-10 分钟,使其分离。孵育后,用 10 毫升培养基轻轻混合细胞使其重悬,然后用 300xg 离心 3 分钟。弃去上清液,用新鲜培养基重悬细胞,并将其转移到已装有新鲜培养基的新烧瓶中。 |
| 冷冻介质 | 我们使用完全生长培养基(包括 FBS)+10% DMSO 或 CM-1(Cytion 商品目录编号 800100)作为冷冻保存培养基,以获得足够的解冻后存活率,CM-1(Cytion 商品目录编号 800100)含有优化的渗透保护剂和代谢稳定剂,可提高恢复能力并减少冷冻引起的应激。 |
| 解冻和培养细胞 |
|
| 培养氛围 | 37°C, 5%CO2, 加湿环境。 |
| 烧瓶涂层 | 无 |
| 冷冻程序 | 冷冻保存的细胞系用干冰装运,并用经过验证的隔热包装和足够的制冷剂包装,以便在整个运输过程中保持约 -78 °C 的温度。收到货后,应立即检查容器,并立即将小瓶转移到适当的储藏室。 |
| 运输条件 | 冷冻保存的细胞系用干冰装运,并用经过验证的隔热包装和足够的制冷剂包装,以便在整个运输过程中保持约 -78 °C 的温度。收到货后,应立即检查容器,并立即将小瓶转移到适当的储藏室。 |
| 储存条件 | 如需长期保存,可将样品瓶放入气相液氮中,温度约为 -150 至 -196 ℃。在-80 °C下保存只能作为转入液氮前的短暂过渡。 |
质量控制/基因图谱/HLA
| 无菌 | 使用基于 PCR 的检测方法和基于发光的支原体检测方法排除支原体污染。 为确保没有细菌、真菌或酵母菌污染,每天都要对细胞培养物进行目视检查。 |
|---|
第三方协议
请注意,标准 Cytion MTA 无法提供该细胞系,因为需要第三方协议和/或与原始许可人协商。-
所需产品
所需产品
冷冻培养基 CM-1 - 50 毫升冷冻保存介质变体: 50 毫升Cytion 的冷冻培养基 CM-1 是一种先进的冷冻培养基,旨在确保细胞在解冻后具有最高水平的活力和功能。这种多功能培养基适用于包括人类和动物细胞在内的多种细胞类型,是各种研究应用的必备工具。Freeze Medium CM-1 精心平衡了冷冻保护剂和必需营养素的组合,在冷冻过程中最大程度地减少了冰晶的形成和细胞应激,从而保护了细胞的完整性。
冷冻培养基 CM-1 的主要特点包括
广泛的兼容性:适用于多种类型的细胞,包括原代细胞、干细胞和成熟的细胞系。
高活力:经过优化,可最大限度地提高冻存后细胞的恢复能力和存活率,确保可靠的实验结果。
即用型:方便制备和灭菌,可立即使用,减少了制备时间和污染风险。
稳定性更强:在标准低温保存条件下保持稳定的性能,确保结果的可重复性。
保存期长:CM-1 是一种含血清的即用型冷冻保存培养基,可在冰箱中保存长达一年。
使用 CM-1 冷冻细胞
要使用 CM-1 冷冻粘附细胞和悬浮细胞,请按照以下步骤操作:
对于粘附细胞,清洗并使其与培养基质分离。对于悬浮细胞,直接进入下一步。
清点细胞,确保细胞浓度合适。
离心细胞使其沉淀,然后用 CM-1 冷冻培养基重悬。
将重新悬浮的细胞转移到冷冻瓶中。
在将细胞转移到长期储存器之前,采用缓慢冷冻的方法。
方法
说明
步骤
❄️
手动冷冻
逐步降低温度以确保细胞活力的方法。
1️⃣ 将细胞放入冷冻培养基中,在 4°C 的冰箱中冷冻 40 分钟。
2️⃣转移到-80°C冷冻室24小时。
3️⃣将细胞保存在液氮中,以便长期保存。
❄️
使用冰冻先生
无需电力即可控制冷冻速率的便捷设备。
1️⃣用冷冻培养基在低温瓶中准备细胞。
2️⃣ 将冷冻瓶放入 Mr.
3️⃣ 在-80°C下保存24小时,然后转移到液氮中。
❄️
可控速率冷冻箱
赛默飞或其他制造商生产的用于控制温度降低的高精度冷冻机。
1️⃣对设备进行编程,使温度逐渐降低。
2️⃣ 将准备好的细胞放入冷冻室。
3️⃣冷冻周期结束后,将细胞转移到液氮中。
将冷冻瓶保存在-130°C以下的温度或液氮中,以便长期保存。
成分
含 FBS、DMSO、葡萄糖、盐类
缓冲能力:pH = 7.2 至 7.6
Cytion 的冻存培养基 CM-1 为低温保存提供了可靠的解决方案,可确保细胞在解冻后的高存活率和高功能性,适用于广泛的研究应用。€59.00*麦考伊斯 5A 培养基(改良),w:3.0 克/升葡萄糖,w:稳定谷氨酰胺,w:2.0 毫摩尔丙酮酸钠,w:2.2 克/升 NaHCO3麦考伊5A培养基是一种备受推崇的专用培养基,专为促进病毒在原代细胞培养中的生长和复制而设计。其在各类生物研究应用中表现卓越,已获得广泛认可。 该培养基在人类结肠癌细胞系培养中的应用尤为突出,特别是用于研究富含亮氨酸重复序列的G蛋白偶联受体(LGR5)及其在结肠癌转移中的作用。 该培养基在多种结肠癌细胞系(包括HCT116、RKO、FET、CBS、HCT116b及TENN)的培养中表现优异,助力科研人员深入解析结肠癌转移的机制。 除癌症研究外,麦考伊5A培养基在成骨细胞研究中亦不可或缺。研究人员利用该培养基培养成骨细胞,以探究标准细胞培养基中钙缺失羟基磷灰石的离子反应性。此应用促进了对成骨细胞与钙缺失羟基磷灰石相互作用的深入理解,推动了骨研究领域的进展。 麦考伊5A培养基通过改良基础Eagle培养基中的氨基酸成分精心配制而成,为肝肿瘤细胞提供最优支持。这种富集配方使其适用于多种已建立细胞系及原代细胞,进一步增强了其在各类研究场景中的多功能性和适用性。 麦考伊5A培养基的生化与生理效应不仅限于肝肿瘤细胞。该培养基已成功应用于支持骨髓、皮肤、牙龈、肾脏、大网膜、肾上腺、肺、脾脏、大鼠胚胎及其他细胞类型的原代培养生长。如此广泛的应用范围,充分证明了麦考伊5A培养基在支持各类细胞生长与维持方面的多功能性,为综合性生物研究提供了有力保障。 配方 本改良版麦考伊5A培养基含3.0 g/L葡萄糖、稳定型谷氨酰胺、2.0 mM丙酮酸钠及2.2 g/L碳酸氢钠。 质量控制 pH值=7.2±0.02(20-25°C)。 每批产品均经过无菌、无支原体和无细菌的检测。 保存 请置于+2°C至+8°C的避光环境中冷藏保存。冷冻及升温至+37°C会显著降低产品品质。 请勿将培养基加热至37°C以上,或使用不可控热源(如微波设备)。 若需使用部分培养基,请从瓶中取出所需量并在室温下加热。 除基础培养基外,所有培养基开封后保质期为6至8周。 成分 成分 毫克/升 无机盐氯化钙·2水合物132.00 硫酸镁97.67 氯化钾400.00 氯化钠6,460.00 磷酸氢二钠(无水)504.00 其他成分D(+)-葡萄糖(无水)3,000.00 还原型谷胱甘肽0.50 肉水解物600.00 酚红钠盐11.00 氨基酸L-丙氨酸13.36 L-精氨酸 x 盐酸盐42.14 L-天冬酰胺 x 水45.03 L-天冬氨酸19.97 L-半胱氨酸 x 盐酸 x 水31.75 L-谷氨酰胺(稳定)219.15 L-谷氨酸22.07 甘氨酸7.51 L-组氨酸 x 盐酸 x 水20.96 L-羟脯氨酸19.67 L-异亮氨酸39.36 L-亮氨酸39.36 L-赖氨酸 x 盐酸盐36.54 L-蛋氨酸14.92 L-苯丙氨酸16.52 L-脯氨酸17.27 L-丝氨酸26.28 L-苏氨酸17.87 L-色氨酸3.06 L-酪氨酸二钠盐26.10 L-缬氨酸17.57 维生素对氨基苯甲酸1.00 抗坏血酸0.56 D(+)-生物素0.20 D-泛酸钙0.20 氯化胆碱5.00 叶酸10.00 肌醇36.00 烟酰胺0.50 烟酸0.50 盐酸吡哆醛0.50 盐酸吡哆醇0.50 核黄素0.20 硫胺素盐酸盐0.20 维生素B122.00€30.00*Accutase 细胞脱附液 - 100 毫升变体: 100 毫升含EDTA和酚红的Accutase细胞脱附液 – 100 毫升
Accutase 是一种即用型、经无菌过滤的细胞脱附液,旨在作为胰蛋白酶/EDTA 的温和替代品,用于将贴壁哺乳动物细胞从标准组织培养塑料器皿和粘附涂层表面上分离。该产品将蛋白水解酶和胶原酶活性结合在平衡盐溶液中,可实现有效且可控的细胞分离,同时保留细胞表面蛋白,并支持高传代存活率及快速再附着。
Accutase 的配方以杜尔贝科磷酸盐缓冲盐水(DPBS)为基础,并添加了 EDTA 及作为视觉 pH 指示剂的酚红。 该酶制剂源自非哺乳动物且非细菌来源,因此Accutase特别适用于干细胞研究、疫苗工作流程,以及任何必须最大限度减少动物或微生物来源污染的应用场景。该溶液在37 °C下会自动失活,因此脱附后无需使用中和试剂或含血清培养基——细胞可直接转移至新鲜培养基中。
主要特点
即用型 1x 无菌过滤液——无需稀释或复溶
兼具蛋白水解和胶原蛋白水解酶活性,实现温和分离
每批产品均标准化至特定解离活性,确保批次间一致性
酶源为非哺乳动物及非细菌来源
在 37 °C 时自动失活——无需中和溶液
以含EDTA的杜尔贝科PBS配制
内含酚红作为视觉pH指示剂
pH 6.8 – 7.8
典型应用
Accutase 可温和地分离各种粘附性和敏感性细胞类型,包括人类胚胎干细胞 (hESCs)、人类诱导多能干细胞 (iPSCs)、神经干细胞、原代神经元以及常规培养的粘附性细胞系,如 HeLa、HEK 293、CHO、MDCK、Vero、NIH/3T3、BHK-21 和 A549。 典型应用包括:
哺乳动物贴壁细胞的常规传代与分培养
hESCs、iPSCs及其他敏感细胞系的温和单细胞分离
流式细胞术和FACS分析的样本制备
对表位完整性至关重要的细胞表面标志物分析
细胞迁移、增殖和凋亡检测
通过血清饥饿法进行的静止期检测及致癌基因转染研究
肿瘤细胞和神经嵴细胞迁移检测
生物反应器工作流程中的生产规模放大
常规操作中,每75 cm²培养表面使用约10 ml Accutase,室温孵育5–10分钟。应针对每种细胞系确定最佳孵育时间,且不应超过一小时。添加前,请用不含钙镁的盐溶液(如无钙无镁DPBS)冲洗细胞层,以去除残留血清和二价阳离子。
操作与储存
未开封的瓶装产品应冷冻保存于-15 °C或更低温度。可在室温下或于+2 °C至+8 °C环境中过夜解冻。请勿在37 °C水浴中解冻Accutase,因高温会降低酶活性。解冻后,溶液可在+2 °C至+8 °C条件下保存最长2个月;请勿在室温下保存。 使用前请勿将试剂预热至37 °C——应在室温下直接加入已洗涤的细胞中。为延长保质期,建议分装为单次用量,以避免反复解冻。操作时务必在无菌条件下进行。
质量
本品在严格的质量标准下生产。每批Accutase均经过无菌过滤,并经过无菌性、pH值、外观及解离活性的检测,以确保批次间性能的一致性和可重复性。
产品规格
规格
详情
产品类型细胞脱附/分离试剂
规格经无菌过滤的液体,即用型
容量100 毫升
工作浓度1×(即用型)
酶活性兼具蛋白水解和胶原蛋白水解活性
酶源非哺乳动物和非细菌
缓冲体系含EDTA的杜尔贝科PBS
pH指示剂酚红
pH 范围6.8 – 7.8
外观透明、淡红至橙色溶液
储存温度-15 °C 或更低
解冻后的稳定性在 +2 °C 至 +8 °C 条件下可保存长达 2 个月
建议使用量每 75 cm² 培养表面约 10 ml
典型孵育时间室温下 5 – 10 分钟
运输条件干冰冷冻
预期用途仅限研究用途及后续生产
配方(每升成分)
组分
浓度(mg/L)
无机盐
氯化钠 (NaCl)8000.00
磷酸氢二钠 (Na2HPO4)1150.00
氯化钾 (KCl)200.00
磷酸二氢钾 (KH₂PO₄)200.00
其他组分
EDTA·4Na(四钠乙二胺四乙酸)220.00
酚红3.00
专有酶混合物(具有蛋白水解和胶原蛋白水解活性)1x
Accutase 是 Innovative Cell Technologies, Inc. 的注册商标。€75.00*抗生素/抗真菌溶液(100 倍)产品概述
容量:100 毫升 储存:≤-15°C 无菌:无菌过滤
抗生素/抗真菌溶液(100 倍)是一种无菌、即用型浓缩液,旨在降低细胞培养和相关实验室应用中的微生物污染风险。这种 100x 溶液含有青霉素、链霉素和两性霉素 B 的成熟组合,对革兰氏阳性和革兰氏阴性细菌、酵母菌和丝状真菌具有广谱抗菌活性。该制剂适用于真核细胞培养、细菌培养基和其他对污染敏感的系统,支持清洁、一致的实验室操作。
应用和优点 该溶液针对常规研究方案进行了优化,广泛用于维持细胞培养工作流程中的无菌条件。它能在污染敏感环境中提供可靠的性能,帮助研究人员降低微生物过度生长的风险,同时不影响细胞健康或实验重现性。无菌过滤配方无需额外的溶解步骤,可简化培养基制备过程,减少日常实验过程中的变异性。
使用方法与兼容性 要达到标准的工作浓度,可将溶液按 1:100 的比例稀释到完整的培养基中。该产品与多种哺乳动物细胞系和基础培养基兼容。由于有稳定的库存,研究人员可从可靠的供应连续性和简化的物流规划中获益。溶液应储存在 ≤ -15 °C 的环境中,避免反复冻融以保持稳定。 仅供研究使用。不得用于诊断或治疗程序。不得用于人类或动物。€45.00*公共广播事业磷酸盐缓冲盐水 (PBS) 溶液
磷酸盐缓冲盐水(PBS)是生物和化学研究中广泛使用的缓冲溶液。在组织处理和细胞培养等各种实验过程中,它在维持 pH 值平衡和渗透压方面发挥着至关重要的作用。我们的 PBS 溶液由高纯度成分精心配制而成,可确保每次实验的稳定性和可靠性。我们的 PBS 溶液的渗透压和离子浓度接近人体渗透压和离子浓度,因此等渗且对大多数细胞无毒。
我们的 PBS 溶液的成分
我们的 PBS 溶液是一种经过 pH 值调整的超纯级磷酸盐缓冲液和生理盐水混合溶液。在 1 倍工作浓度下,它包含
8000 毫克/升氯化钠(NaCl)
200 毫克/升 氯化钾(KCl)
1150 毫克/升 无水磷酸氢二钠(Na2HPO4)
200 毫克/升 无水磷酸二氢钾(KH2PO4)
这种成分可确保最佳的 pH 值和离子平衡,适用于广泛的生物应用。
我们的 PBS 溶液的应用
我们的 PBS 溶液非常适合生物研究中的各种应用。它具有等渗和无毒的特性,适用于物质稀释和细胞容器冲洗。含有 EDTA 的 PBS 溶液可有效分离附着和凝集的细胞。不过,PBS 中不应添加锌等二价金属,否则会导致沉淀。在这种情况下,建议使用 Good's 缓冲液。此外,我们的 PBS 溶液也可作为病毒运输培养基的替代品,用于运输和储存包括 SARS-CoV-2 在内的 RNA 病毒。
质量控制
无菌过滤
储存和保质期
储存于 +2°C 至 +25°C,避光保存。
开封后,储存于 2°C 至 25°C,并在 24 个月内使用。
运输条件
环境温度
保养
避光冷藏,温度保持在 +2°C 至 +8°C。避免冷冻和频繁加温至 +37°C,否则会降低产品质量。
不要将培养基加热到 37°C 以上或使用微波炉等不受控制的热源。
如果只需使用部分培养基,请取出所需用量并加热至室温后再使用。
成分
类别
成分
浓度(毫克/升)
盐类
氯化钾
200
无水磷酸一钾
200
氯化钠
8000
无水磷酸氢二钠
1150€20.00* -
相关产品
相关产品