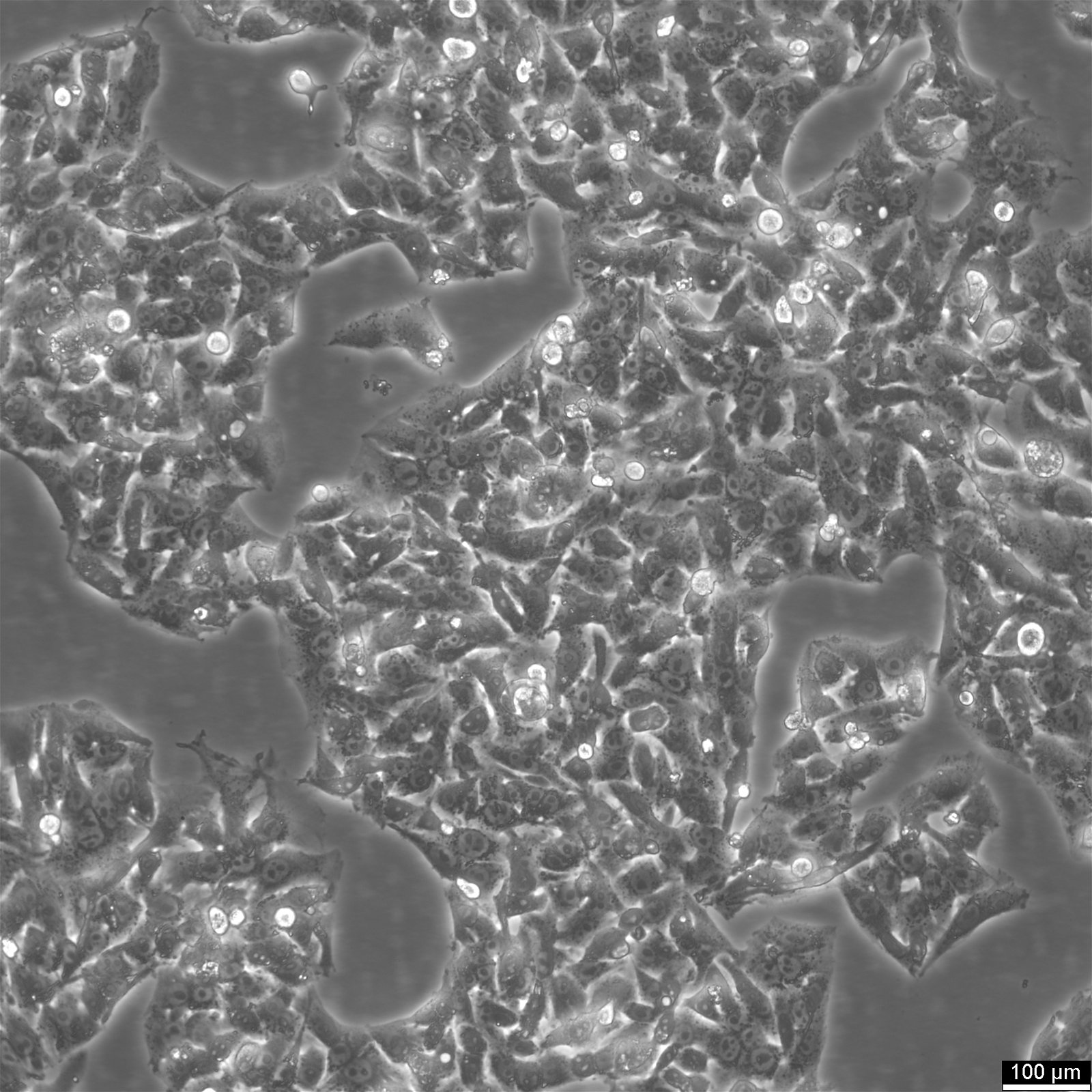
HepG2細胞 - 肝癌研究リソース
Hep-G2は、肝細胞癌を患った15歳の白人男性の肝組織に由来するヒト肝癌細胞株である。この細胞は薬物代謝や肝毒性研究で頻繁に利用されている。HepG2細胞は高い増殖率と上皮様の外観を持つが、腫瘍性はなく、様々な分化肝機能を発揮する。1975年、研究者らは肝細胞癌からHepG2細胞を誘導し、肝細胞の重要な特徴を示す最初の肝細胞株とした。肝細胞の必須マーカーを欠く先に確立されたSK-Hep1細胞株とは対照的に、HepG2細胞は様々な血漿タンパク質を分泌することができ、ヒト肝細胞における細胞表面ドメインの細胞内動態を研究するための貴重なモデルとなる。これらの細胞は上皮様形態を示し、モード染色体数は55で、ヒト成長ホルモンで刺激することができる。
HepG2の特徴
初代肝細胞の典型的な形状は立方体で、通常2つの核を持つ。対照的に、HepG2細胞は上皮様形態を有し、核は1個で、染色体数は1細胞当たり48~54本である。HepG2細胞は全細胞タンパク質の最大25%を占めるが、そのサイズは正常肝細胞よりも大きく、細胞内の全タンパク質の約10%を占める。細胞タンパク質は細胞内で重要な働きをし、遺伝子によって指定された機能を実行する。
染色体の数に異常があるものを含む腫瘍細胞は、しばしば核の数が増加し、1細胞あたり7個まで増加する。試験管内で高度に分化するため、HepG2細胞はヒト肝細胞における胆管、類洞膜タンパク質、脂質の細胞内輸送と動態を研究するための理想的なモデルとなる。
HepG2細胞の平均直径は約10-20μmであり、直径15μmの肝細胞よりは小さいが、10-20μmである肝芽腫(HB)の腫瘍細胞と同様である。
HepG2の遺伝学
Hep-G2細胞株は、1番と21番染色体の短腕間の転座、2番、16番、17番染色体のトリソミー、20番染色体のテトラソミーなど、いくつかの転座を示す。また、肝芽腫(HB)でしばしば見られる転座t(1;4)や、2番や20番のトリソミーなどの染色体異常と関連して、4q3領域の欠損も観察される。HepG2細胞の染色体数は50〜60本で、超2倍体の核型を示すが、100本以上の染色体を示す症例もあり、4倍体の肥大が特徴である。HepG2細胞のDNA量は約7.5pgで、平均的な体細胞より15%多い。比較すると、初代肝細胞は立方体の細胞形状をしており、通常2つの核を含んでいる[1]。
HepG2細胞の変異プロファイル
HepG2細胞株は、肝細胞癌(HCC)や肝芽腫(HB)にも存在するTERTプロモーター領域変異C228Tを持っている。この変異は癌細胞のテロメアを保護することによって不死化に寄与する。さらに、HepG2細胞は野生型TP53を示す。TP53は細胞周期の停止、アポトーシス、老化に関与するため、ヒトの癌を抑制するために重要な遺伝子である。この遺伝子に変異があると細胞増殖が促進される。
HepG2細胞は、細胞増殖の調節異常、胎児性・胚性HBなどの生存経路、Wnt/β-カテニン経路など、いくつかの経路に関与している。さらに、この細胞株はCTNNB1遺伝子の第3エクソンに特徴的な欠失があり、これは上皮型HBで見られるものと同じである[2,3]。
肝研究におけるHepG2肝細胞癌細胞の概要
ヒト肝腫瘍由来のHepG2細胞は、肝細胞癌を含む肝機能や疾患の研究において非常に貴重なツールとなっている。これらの肝細胞株は、様々な実験条件下におけるヒト肝細胞の細胞応答についての洞察を与えてくれる。HepG2細胞におけるルシフェラーゼレポータープラスミドの使用は、肝細胞に対するエタノールの影響の研究など、代謝研究の基礎となる遺伝子発現や細胞トランスフェクションの追跡に特に効果的である。
HepG2細胞を用いたウイルス感染および肝疾患研究
HepG2やHuh7のような不死化肝腫瘍細胞株は、D型肝炎(HDV)の完全な細胞周期複製やB型肝炎(HBV)の発現を示し、ウイルス感染の研究に不可欠である[5,6]。これと並行して、HepaRG細胞株はHBV侵入メカニズムの解明において重要な役割を果たしている[7]。HepG2細胞はまた、進行性家族性肝内胆汁うっ滞症(PFIC)やDubin-Johnson症候群のような遺伝的疾患から、細胞毒性薬剤や遺伝毒性薬剤に関連する環境および食餌の研究、さらには薬剤標的化や肝発癌の研究に至るまで、様々なヒト肝疾患の研究にも使用されている [8,9]。その利用は、バイオ人工肝臓装置の試験にも及んでいる。
組織工学におけるHepG2細胞と生体材料の相互作用
HepG2細胞と様々な生体材料との相互作用は、組織工学において極めて重要である。コロイドプローブ技術のような技術は、細胞接着特性を測定することにより、これらの相互作用を理解するのに役立ち、これは足場や正確な肝組織モデルの開発における細胞生存率の決定に不可欠である。
HepG2ベースのモデルにおける細胞挙動とイノベーション
HepG2ベースのモデルにおける細胞挙動の研究は、肝疾患研究にとって極めて重要である。三次元スフェロイド細胞培養の進歩により、HepG2細胞スフェロイドが作製され、正常な肝細胞に近い、より生理学的に適切なモデルが提供されるようになった。代謝活性が向上したこれらの3次元モデルは、HepG2細胞が肝芽腫のモデルとして機能する可能性を示しており、特に肝腫瘍のシミュレーションや新規治療アプローチの試験など、がん治療研究において重要な意味を持つ[10-12]。
他の腫瘍細胞株との比較とHepG2の特徴
HepG2は最も広く使用されている肝腫瘍細胞株の一つであり、利用可能な約40種類の肝腫瘍細胞株の中から、科学研究への幅広い応用のために選択された[13]。正常肝細胞と比較して、特定のチトクロームP450酵素の発現が弱いか、あるいは発現がないにもかかわらず、HepG2の代謝プロファイルは、より優れた薬物代謝研究のために細胞株を改変する努力を促してきた [13] 。MCF7、PC3、143B、HEK293のような腫瘍細胞株と比較して、HepG2細胞は、タンパク質合成と分泌に大きく影響するユニークなアミノ酸含量プロファイルを示し、そのユニークな代謝経路を強調している [14]。
HepG2で肝疾患研究を探る
HepG2細胞の部分培養
アキュターゼを用いて細胞培養フラスコから付着細胞を除去する5つのステップを以下に示す:
- 細胞培養フラスコから培地を除去し、カルシウムとマグネシウムを除いたPBSで付着細胞をすすぐ。T25フラスコには3~5ml、T75フラスコには5~10mlのPBSを使用する。
- 細胞培養フラスコにアキュターゼを、T25フラスコ当たり1-2mL、 T75フラスコ当たり2.5mL加える。アキュターゼが細胞シート全体を覆うようにする。
- フラスコを室温で8~10分間インキュベートする。
- 新鮮なメデュームを10ml使用し、細胞をメデュームで注意深く再懸濁する。
- 再懸濁した細胞を300xgで5分間遠心し、新鮮な培地に再懸濁し、新鮮な培地の入った新しいフラスコに分注する。
HepG2細胞の今後の展望
HepG2細胞株の可能性を最大限に引き出す探求は、チトクロムの発現を増加させる画期的な進歩とともに続いている。研究者たちはまた、より生理学的に適切な系を提供する三次元スフェロイド細胞培養の可能性を模索している。シトクロムを含む代謝活性は、2次元細胞よりも3次元スフェロイドHepG2モデルの方が著しく高く、正常な肝細胞を反映したモデルの作成に近づいている。さらに、細胞表面タンパク質の不正確な分布の根底にある動的プロセスを探求することで、肝疾患のより良い理解への道を開くことができる。
HepG2細胞:生物医学研究におけるその役割と特徴を理解する - FAQs
参考文献
- Vyas, R.C., Darroudi, F., Natarajan, A.T. Radiation-induced chromosomal breakage and rejoining in interphase-metaphase chromosomes of human lymphocytes, Mutat Res, 1991; 249(1):29-35.
- Woodfield, S.E., Shi, Y., Patel, R.H., Chen, Z., Shah, A.P., Srivastava, R.K., Whitlock, R.S., Ibarra, A.M., Larson, S.R., Sarabia, S.F., et al. MDM4阻害:肝芽腫におけるP53を再活性化する新規治療戦略。Sci. Rep. 2021, 11, 2967.
- Hussain、S.P.、Schwank、J.、Staib、F.、Wang、X.W.、Harris、C.C. TP53変異と肝細胞癌:肝癌の病因と病態への洞察。Oncogene 2004年
- Schicht、G.、Seidemann、L.、Haensel、R.、Seehofer、D.、Damm、G. 切除可能な肝細胞癌の代謝表現モデルとしての肝細胞腫細胞株HepG2およびHuh7の有用性の批判的調査。Cancers 2022, 14(17), 4227.
- Verrier, E.R., Colpitts, C.C., Schuster, C., Zeisel, M.B., Baumert, T.F. Cell Culture Models for Investigation of Hepatitis B and D Virus Infection.Viruses 2016, 8, 261.
- Verrier,E.R.、Colpitts,C.C.、Bach,C.、Heydmann,L.、Weiss,A.、Renaud,M.、Durand,S.C.、Habersetzer,F.、Durantel,D.、AbouJaoudé,G.、他。 A Targeted Functional RNA Interference screen Uncovers Glypican 5 as an Entry Factor for Hepatitis B and D Viruses.Hepatology 2016, 63, 35-48.
- Gripon, P., Rumin, S., Urban, S., Le Seyec, J., Glaise, D., Cannie, I., Guyomard, C., Lucas, J., Trepo, C., Guguen-Guillouzo, C. B型肝炎ウイルスによるヒト肝腫細胞株の感染。Proc.Natl. Acad.Sci. USA 2002, 99, 15655-15660.
- Mersch-Sundermann、V.、Knasmüller、S.、Wu、X.J.、Darroudi、F.、Kassie、F. 細胞保護剤、抗原毒性剤、遺伝毒性剤の検出におけるヒト由来肝細胞株の使用。毒性学。2004; 198(1-3):329-340.
- HepG2(肝細胞癌):細胞培養。HepG2.2017年12月3日取得。
- Xuan, J., Chen, S., Ning, B., Tolleson, W.H., Guo, L. Development of HepG2-Derived Cells Expressing Cytochrome P450s for Assessing Metabolism-Associated Drug-Induced Liver Toxicity.Physiol. Behav.2017, 176, 139-148.
- 高スループットスクリーニングにおけるin vitro代謝活性化の応用。Int.J. Mol.科学, 2020, 21, 8182.
- ヒト肝細胞癌におけるデヒドロエピアンドロステロン硫酸転移酵素遺伝子のダウンレギュレーション。Mol.Cell.Endocrinol.
- Zhu, Z., Hao, X., Yan, M., et al. Cancer stem/progenitor cells are highly enriched in CD133 + CD44 + population in hepatocellular carcinoma.Int J Cancer.2010; 126:2067-2078.
- シアメマジンの代謝に関与するヒトのチトクロームP450酵素の特性。Eur J Pharm Sci. 2007 Dec;32(4-5):357-66.