HCT116細胞株:大腸癌研究の柱
HCT116細胞株は 、大腸癌の研究において礎石としての役割を果たしており、この疾患の病態や潜在的な治療法に関する貴重な洞察を提供している。がん研究や薬理学的評価における有用性で知られるHCT116は、腫瘍の挙動や薬剤の有効性に関する極めて重要な研究を促進する。
HCT116細胞の起源と基本的特徴
HCT116細胞の形態学的特徴、遺伝子構成、細胞の大きさなどのルーツと基本的特徴を理解することは、この細胞株を用いた研究に着手する研究者にとって不可欠である。
起源と遺伝的背景大腸がんと診断された48歳の白人男性の大腸から採取されたHCT116細胞は、RAS/RAF/MEK/ERKシグナル伝達経路の一部であるKRAS遺伝子のコドン13(G13D)に変異があることが特徴である。この特定の変異は、これらの細胞のがん化に極めて重要であり、がん研究における重要性を強調している。
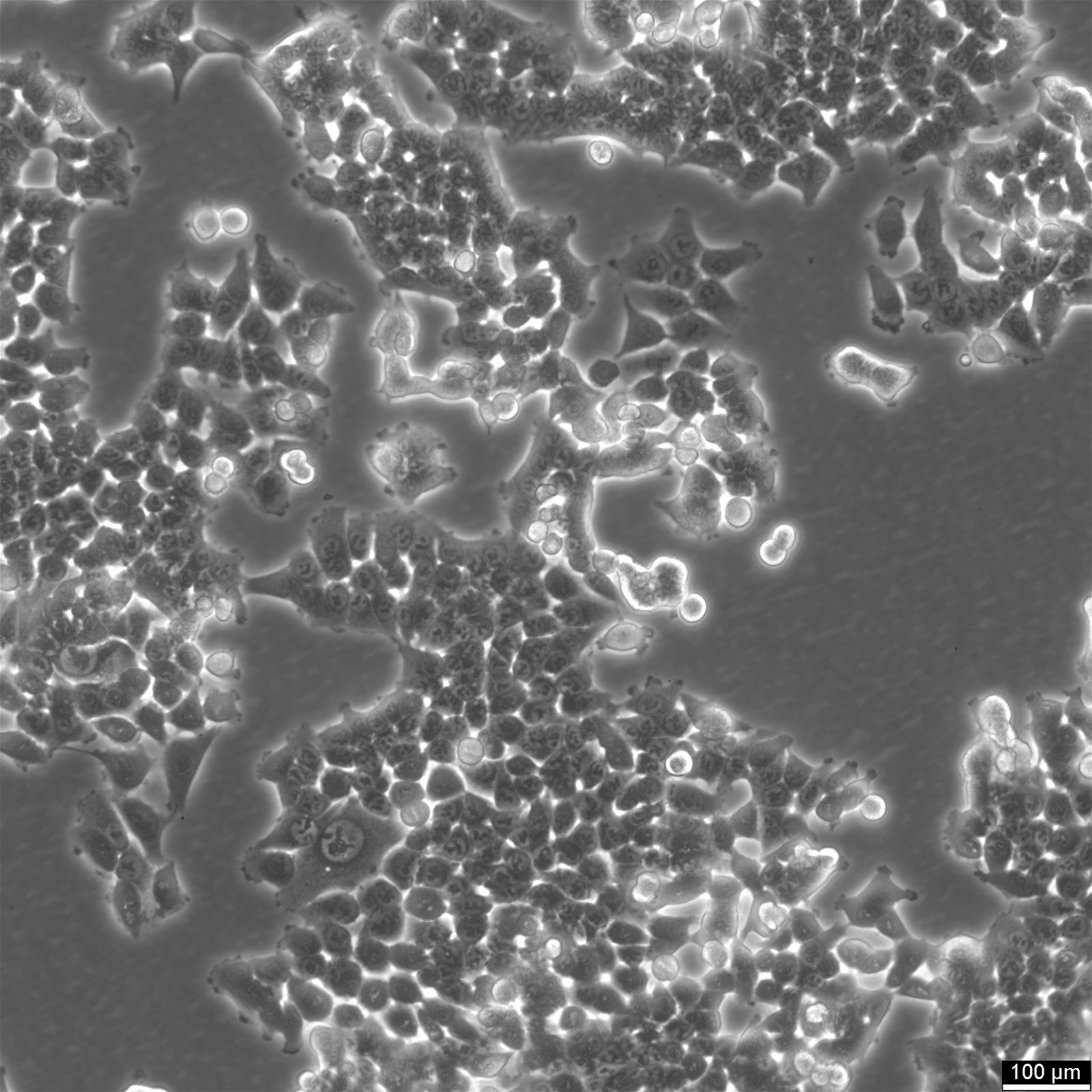
形態と増殖特性:上皮様形態を示すHCT116細胞は、通常単層培養で増殖するが、直径150-400μmのスフェロイドを形成することもできる。このような増殖パターンの適応性は、様々な実験セットアップにおけるHCT116細胞の多用途性を強調している。
染色体プロフィール:HCT116細胞の染色体構成はほぼ2倍体であり、細胞集団の約70%が45本の染色体を保有している。注目すべきは、8番、10番、16番、17番の長腕に再発性の増幅が見られるのに対し、Y染色体は存在しないことであり、これがHCT116細胞のユニークなゲノムの特徴となっている。
比較解析:HCT116とHT29細胞株との比較
HCT116をもう一つのヒト大腸癌細胞株であるHT29と並べると、発癌能と分化能に明確な違いが現れる:
がん原性攻撃性と分化能である:がん原性攻撃性と分化能:HCT116細胞は、高いがん原性攻撃性と限られた分化能を特徴とし、攻撃的な腫瘍表現型を研究するモデルとなっている。対照的に、HT29細胞は腸細胞様系とムチン産生系への分化能を示し、大腸癌生物学の多様な側面を模倣する対照的モデルを提供する。
HCT116細胞株とHT29細胞株のこのような比較理解は、研究者が利用できるツールキットを充実させ、大腸癌の多面的性質についてのより微妙な研究を可能にする。
HCT116細胞の取り扱い
|
倍加時間: |
HCT116癌細胞の倍加時間は25~35時間である。 |
|
接着または懸濁状態: |
HCT116結腸癌細胞株は接着性で、細胞は単層で増殖する。 |
|
播種密度: |
HCT116細胞培養には2 x104 cells/cm2の播種密度が推奨される。再培養には、1x PBS洗浄後、Accutase溶液を用いて細胞を剥離する。遠心後、細胞ペレットを新鮮な増殖培地に再懸濁し、新しいフラスコに移す。 |
|
増殖培地: |
3.0g/LのL-グルコース、1.5mMのL-グルタミン、3.0g/LのNaHCO3、および10%のウシ胎児血清を添加したMcCoys 5a培地がHCT116細胞の培養に最適である。培地は週に1~2回更新することが望ましい。 |
|
増殖条件(温度、CO2): |
培養は37℃、5%CO2雰囲気の加湿インキュベーター内で行う。 |
|
保存: |
HCT116細胞は液体窒素の気相または液相で-150℃以下で保存できる。 |
|
凍結プロセスと培地: |
凍結保存にはCM-1またはCM-ACF培地を用いる。細胞の生存率を維持するために、1分間に1℃ずつ徐々に温度を下げられるよう、速度を制御した凍結方法が推奨される。 |
|
融解プロセス: |
HCT116細胞を37℃のウォーターバスで融解する。増殖培地を加えた後、遠心して凍結培地残渣を除去する。細胞ペレットを新しい培地に懸濁し、新しいフラスコで培養する。 |
|
バイオセーフティーレベル |
レベル1 |
HCT116細胞株の利点
このセクションではHCT116細胞株について掘り下げ、癌研究、特に大腸癌の研究において極めて重要な役割を担っていることを強調し、その固有の利点について述べる。
HCT116細胞株は、いくつかの重要な利点により、癌研究において際立っている:
大腸癌モデル:大腸癌モデル:世界的に3番目に多い癌である大腸癌のin vitroモデルとして広く認知されている。ヒトの大腸がんを模倣したその関連性は、がんの生物学を理解し、治療戦略を検証する上で非常に貴重である。
均質性:驚くべきことに、HCT116細胞の約70%は一貫した遺伝子プロファイルを示し、比較的均質な集団である。この均一性は、実験結果の一貫性と信頼性を保証するため、遺伝子発現、細胞シグナル伝達経路、薬物治療の有効性評価に焦点を当てた研究にとって極めて重要である。
トランスフェクション効率:HCT116細胞の際立った特徴の一つは、特にウイルスベクターによるトランスフェクションに対する高い適合性である。この特性は遺伝子治療研究において特に有益であり、効率的かつ正確に遺伝物質を導入できるため、高度な遺伝子操作や機能研究が容易になる。
認証されたHCT116細胞株で あなたの発見を前進させる
HCT116細胞株の研究応用
HCT116細胞株は癌研究において幅広い応用が可能である。いくつかの顕著な応用例は以下の通りである:
癌生物学
HCT116結腸癌細胞株は結腸癌の進行と発生の研究に用いられる。さらに、癌の増殖、遊走、浸潤に関与する根本的なメカニズムやシグナル伝達経路の解明にも役立っている。ある研究では、薬剤耐性発現に関与する遺伝子の研究にHCT116細胞を用いた。研究者らは、結腸がん細胞でMDR1遺伝子を過剰発現させ、NOX(NADPH酸化物)アイソフォームとNrf2の発現を観察した。同様に、2021年に行われた研究では、NF-κBシグナル伝達経路が結腸癌の増殖と遊走の制御に関与していることが報告された。したがって、NF-κBシグナル伝達経路を標的とすることで、大腸癌に対する新規で効果的な治療薬を開発することができる [2]。
腫瘍学の領域では、細胞周期、増殖と成長、アポトーシスの複雑なプロセスを理解することが基本である。これらの生物学的機能は、ヒト細胞株、特にヒト結腸癌細胞や膵臓癌モデルのような悪性細胞に由来する細胞株の研究において極めて重要である。例えば、HCT116細胞株とSW620細胞株は、それぞれ結腸がんと膵臓がんの根底にあるメカニズムを探求するのに役立っている。フローサイトメトリーやクローン形成アッセイなどの技術により、研究者は腫瘍内の独立した細胞の遺伝子発現プロファイルや挙動を解明し、がんが細胞外マトリックス内でどのようにコミュニケーションしているかに光を当てることができる。
癌の進行におけるアポトーシスの役割
アポトーシス、すなわちプログラムされた細胞死は、細胞の恒常性を維持する上で重要な役割を果たしており、癌研究における重要な研究分野である。がんと無関係なアポトーシスと、大腸がん細胞死などがんに特異的に誘導されるアポトーシスとの区別は極めて重要である。このプロセスは、単に細胞を除去するだけではなく、腫瘍の増殖や転移に影響を与えるシグナルが複雑に絡み合っている。アポトーシスと細胞死を転移抑制因子や癌抑制因子活性と合わせて調べることにより、科学者は癌の進行と転移能を制御する経路についての洞察を得ることができる。
癌の転移と分子マーカー
転移は依然として癌の最も厄介な側面の一つであり、悪性細胞の拡散において血行性転移は重要な関心事である。転移の研究においては、がん細胞の移動と浸潤能力、すなわち細胞運動と、細胞が細胞外マトリックスを含む周囲の環境とどのように相互作用するかを研究する必要がある。CD133発現や上皮成長因子受容体のような分子マーカーは、陽性の結腸癌細胞や他のタイプの癌の挙動を同定し理解する上で極めて重要である。例えば、SIRT6経路は、腫瘍増殖と転移性結腸癌の調節におけるその潜在的役割のために、関心のある分野として浮上している。
毒性学/薬剤開発
HCT116細胞株は新しい抗癌剤のスクリーニングモデルとして用いられている。天然物や化学的に合成されたナノ粒子を含む抗がん剤の有効性と毒性を評価するために、いくつかの研究が行われてきた。この研究では、生薬であるCaesalpinia pulcherrimaの 抽出物から合成した銀ナノ粒子のHCT116細胞における細胞毒性を評価した[3]。研究者らは、HCT116がん細胞株を用いて、カカオ茶水抽出物の抗がん作用を評価した。 別の研究では、HCT116がん細胞を用い、エアーポテト( Dioscorea bulbifera) 抽出物が、JNKシグナル伝達カスケードの活性化とERK1/2遺伝子の抑制を介して、大腸がん細胞のアポトーシス活性を示すことを発見した [5]。
メトホルミンのがん細胞、特に結腸がんや膵臓がんに対する作用は、がん細胞の生物学的機能を理解することがいかに潜在的な治療戦略につながるかを例証している。メトホルミンのような薬剤による治療や、上皮成長因子受容体のような特定の経路を標的とした治療による、がん細胞のクローン形成生存、すなわちクローン形成能に関する研究は、効果的ながん治療法に関する貴重な知見を提供することができる。さらに、これらの研究でHCT116クローンやHCT116細胞集団を使用することで、がん細胞がさまざまな治療介入にどのように反応するかについての微妙な理解が可能となり、がん治療に対するより個別化されたアプローチへの道が開かれる。
HCT116細胞研究発表
このセクションでは、HCT116細胞株を取り上げた重要で最も引用された最近の出版物をいくつか紹介する。
この研究はJournal of Photochemistry and Photobiology B: Biology(2017年)に掲載された。研究者らは、HCT116結腸がん細胞株とA549肺がん細胞株を用いて、ピペル・ニグラム種子を介した合成酸化スズナノ粒子の細胞毒性効果を評価した。
ロングノンコーディングRNA SNHG15は転写因子Slugと相互作用して安定化し、結腸がんの進行を促進する
Cancer Letters(2018年)に掲載されたこの研究は、HCT116を含む大腸癌細胞株において、lncRNA SNHG15が大腸癌細胞の移動を促進することを提唱している。
ロングノンコーディングRNA TUG1の過剰発現は結腸癌の進行を促進する
この論文は2016年にMedical Science Monitor誌に掲載された。この研究では、がん原性LncRNA TUG1がHCT116結腸がん細胞の増殖と遊走を促進することを発見した。
薬剤耐性はHCT116結腸癌細胞におけるH2S産生酵素のアップレギュレーションを誘導する
Biochemical Pharmacology誌(2018年)に掲載されたこの研究は、薬剤耐性の発現がHCT116結腸癌細胞におけるH2S産生酵素のレベルを上昇させることを提唱している。
Inula viscosa L.水抽出物のHCT116細胞株に対するmicroRnas発現におけるアポトーシスおよび抗増殖効果:in vitro試験
この論文は、International Journal of Environmental Health Research (2023)に掲載され、イヌラ・ビスコサ・L.エキスがマイクロRNAの制御を介してHCT116大腸がん細胞に対して抗がん作用を発揮することを提唱している。
HCT116細胞に関するリソース
以下はHCT116細胞に関するいくつかのリソースである。
- HCT116のトランスフェクションこのビデオはHCT116癌細胞のトランスフェクションのステップバイステップガイドです。
- HCT116細胞株の培養:この動画はHCT116結腸癌細胞株の部分培養プロトコールを示しています。
- HCT116細胞株のサブカルチャー:このウェブサイトには、HCT116の培地に関する多くの有用な情報が掲載されている。さらに、細胞の凍結、融解、亜培養の手順も掲載されている。
HCT116細胞についてよくある質問
参考文献
- Waghela, B.N., F.U. Vaidya, and C. Pathak:Upregulation of NOX-2 and Nrf-2 promotes 5-fluorouracil resistance in human colon carcinoma (HCT-116) cells.Biochemistry (Moscow), 2021,86, p. 262-274.
- Yang, M., et al.,アストラガリンはNF-κBシグナル伝達経路を調節することによりヒト結腸癌HCT116細胞の増殖と移動を抑制する.Frontiers in Pharmacology, 2021,12: p. 639256.
- Deepika, S., C.I. Selvaraj, and S.M. Roopan,「Caesalpinia pulcherrima L. swartzの生物活性スクリーニングおよび合成銀ナノ粒子抽出物のHCT116細胞株に対する細胞毒性」.Materials Science and Engineering, C, 2020,106, p. 110279.
- Gao, X. 他,ココア茶(Camellia ptilophylla)は活性酸素種生成とPI3K/Aktシグナル経路を介してHCT116細胞にミトコンドリア依存性アポトーシスを誘導する.食品研究国際誌, 2020,129, p. 108854.
- Hidayat, A.F.A. 他,Dioscorea bulbifera は HCT116 ヒト結腸直腸癌細胞において ERK 1/2 の阻害と JNK シグナル伝達経路の活性化を介してアポトーシスを誘導した.バイオメディシン&ファーマコセラピー, 2018.104: p. 806-816.