AGS細胞 - 癌研究における胃腺癌AGS細胞の探索
AGS細胞はヒト胃腺癌細胞株であり、生物医学研究に広く用いられている。特に、腫瘍の成長、発生、進行、治療介入を含む胃癌の生物学を研究するために使用されている。さらに、宿主と病原体の相互作用の研究にも用いられている。
本稿では、胃上皮AGS細胞の基礎について述べる。特に以下の点を取り上げる:
1.AGS細胞の一般的特徴と由来
細胞株の起源と一般的特徴について知っておくことは、その細胞株を使い始める前に必要です。このセクションでは、以下について説明します:AGS細胞とは何か?AGS細胞の起源は?AGS癌細胞株の形態は?
- AGS細胞株は、胃腺癌を患った54歳の白人女性の胃組織に由来する。1979年に単離された[1]。
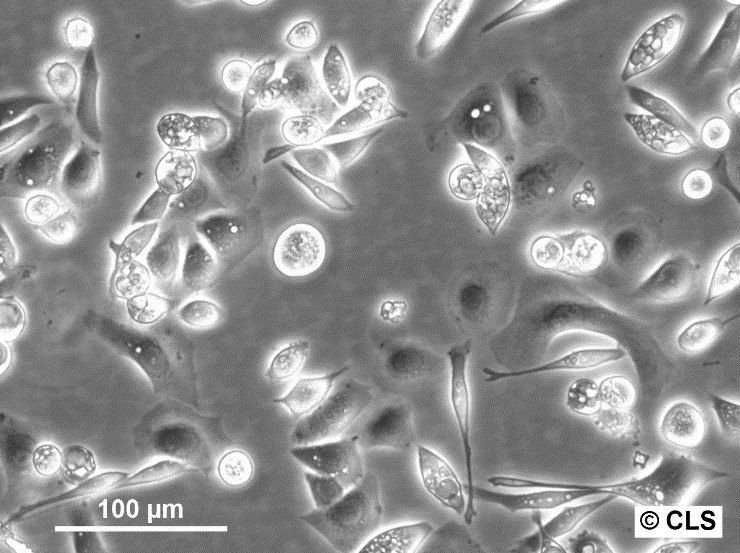
- AGS細胞は上皮様形態を有する。
- 胃上皮AGS細胞は2倍体である。AGS細胞の最頻染色体数は49であり、ほぼ60%の細胞に見られる。また、倍数体は細胞の約3.6%に見られる。
2.AGS細胞株に関する培養情報
細胞株を適切に取り扱い、管理するためには、基本的な培養の概念を知っておく必要があります。特に、以下のことを学ぶ必要があります:AGS細胞の倍加時間とは?AGS細胞培地とは何ですか?AGS細胞はどのようにサブカルチャーするのですか?胃上皮AGS細胞に使用される凍結培地は?
AGS細胞培養のポイント
|
倍加時間: |
AGS細胞の倍加時間は24~48時間です。 |
|
接着か懸濁か: |
AGS細胞は接着性である。単層に増殖する。 |
|
播種密度 |
AGS細胞は1 x104 cells/cm2の細胞密度で播種される。細胞はこの密度で3~5日でコンフルエントな単層になる。古い培地を除去した後、細胞を1×PBSで洗浄し、アキュターゼ解離液でインキュベートする。剥離した細胞を培地に再懸濁し、遠心分離した。細胞ペレットを再度懸濁し、AGS細胞計数後、新しいフラスコに分注して増殖させる。 |
|
増殖培地: |
AGS細胞の培養には、10%FBS、4mM L-グルタミン、4.5g/Lグルコース、1.5g/L NaHCO3、1.0mMピルビン酸ナトリウムを含むDMEM培地を用いる。培地は週に2~3回交換する。 |
|
増殖条件: |
AGS細胞は、加湿インキュベーター(37℃、5%CO2供給)で培養する。 |
|
保存: |
凍結したAGS細胞は、-150℃以下の電気冷凍庫、または液体窒素の気相中で長期間保存する。 |
|
凍結プロセスと培地 |
AGS細胞の凍結にはCM-1またはCM-ACF培地が使用される。細胞の凍結は、1分間に1℃しか温度が下がらないような緩慢な凍結プロセスで行われ、細胞の生存能力を保護する。 |
|
解凍プロセス: |
凍結した胃上皮細胞を37℃のウォーターバスで40~60秒間急速に攪拌する。解凍した細胞を新鮮な培地に再懸濁し、新しいフラスコに流し込んで増殖させる。24時間培養後、培地を新しくして凍結培地成分を除去する。これとは逆に、解凍した細胞を遠心分離し、凍結培地成分を除去する。その後、採取した細胞を再び懸濁し、培地の入ったフラスコに分注する。 |
|
バイオセーフティレベル |
AGS細胞培養には、バイオセーフティーレベル2の実験室環境が不可欠である。 |
3.AGS細胞株:利点と限界
このセクションでは、AGS細胞に関連する主な利点と限界について説明する。
利点
胃上皮AGS細胞の主な利点は以下の通りである:
|
培養が容易 |
AGS胃癌細胞株は細胞培養研究室で容易に維持できる。複雑で煩わしい細胞培養の必要はない。さらに、良好な増殖特性を示し、胃癌生物学の研究に理想的な選択である。 |
|
胃癌との関連性 |
AGS細胞はヒト胃腺がん由来であり、胃がんの生物学的研究および治療介入に広く用いられている。 |
限界
AGS細胞株に関する限界は以下の通りである:
|
In vitro細胞モデル |
AGS細胞は生物医学研究所で人工的な条件下で培養されている。そのため、in vivoでの胃がんの微小環境やその他の細胞・分子間相互作用を完全に再現できない可能性がある。 |
4.AGS細胞の応用
AGS細胞は特に胃がんの生物学的研究に用いられる。AGS細胞は、バイオメディカル分野で他にも多くの有望な応用がある。AGS細胞の興味深い研究応用例をいくつか挙げる:
- 胃癌研究: 胃がんの研究:AGS細胞は、胃がんの増殖、転移、浸潤の根底にある細胞や分子のメカニズムを調べるための優れた研究ツールである。研究者はまた、胃がん発生におけるさまざまな細胞プロセス、遺伝子変異、シグナル伝達経路を研究するために胃上皮AGS細胞を用いている。Oncology Reports(2019年)の研究によると、マイクロRNA-183-5p.1はBcl 2/P53シグナル伝達カスケードを阻害することにより、腫瘍細胞の増殖、遊走、浸潤を促進する。さらに、これらの効果を発揮するためにTPM1遺伝子をダウンレギュレートする。従って、microRNAとTPM1の両方が、抗胃癌剤の標的治療を開発するための効果的な分子標的であることが示唆されている[2]。
- 薬剤スクリーニング: AGS細胞は、新規で効果的な抗胃癌剤のスクリーニングによく用いられている。研究者らは、AGS細胞株を用いて潜在的薬剤の細胞毒性と有効性を評価している。また、新しい分子標的を同定し、胃癌に対抗する新しい標的療法を開発する研究も行われている。2021年に行われた研究では、AGS胃がん細胞を利用し、パクリタキセル薬の治療効果を研究した。その結果、パクリタキセルはAGS細胞においてアポトーシスや細胞死の不可欠なメカニズムである分裂カタストロフィーを誘導することが明らかになった。さらに、パクリタキセルは胃がん細胞のオートファジーも促進した [3]。
- 宿主と病原体の相互作用: AGSがん細胞株は、宿主と病原体の相互作用も研究している。これは、研究者が感染に関与する細胞メカニズムや反応を理解するのに役立つ。例えば、2020年に行われた研究では、ヘリコバクター・ピロリの 外膜小胞に存在する低分子ノンコーディングRNAが、ヒトAGS細胞におけるインターロイキン8の分泌を減少させることが観察された [4]。
5.AGS細胞株に関する研究発表
このセクションでは、AGS細胞を取り上げた興味深い研究論文や最も引用された研究論文をいくつか取り上げる。
サリドロシドはPI3K/Akt/mTOR経路を介してヒト胃癌AGS細胞にアポトーシスと保護的オートファジーを誘導する
Biomedicine & Pharmacotherapy誌(2020年)に掲載されたこの研究は、天然化合物であるサリドロシドが、PI3K/Akt/mTORシグナル伝達経路の調節を介して、胃上皮AGS細胞において保護的オートファジーと細胞死を誘導することを提唱した。
ハトムギ多糖体は、AKTシグナル伝達経路を阻害することにより、胃がんAGS細胞におけるアパチニブの抗腫瘍効果を増強した
この研究はBiomedicine & Pharmacotherapy(2018年)に掲載された。AGS細胞におけるハトムギ多糖体とアパチニブ製剤の相乗的な抗がん作用を探索したものである。研究の結果、ハトムギはAKTシグナルの抑制を介してアパチニブの抗腫瘍効果を増強することが明らかになった。
クルクゼドアライドはアポトーシス誘導を介してヒト胃癌AGS細胞に対するクルクマ・ゼドアリア根茎の細胞毒性に寄与する。
Journal of Ethnopharmacology誌(2018年)に掲載されたこの研究は、Curcuma zedoaria Roscoe植物由来の天然化合物であるクルクゼドアライドが、AGS細胞に対する細胞毒性能に寄与していることを提唱した。
FOXA1の過剰発現はヒト胃癌AGS細胞の細胞増殖とEMTを阻害する
Gene (2018)に掲載されたこの論文は、FOXA1のアップレギュレーションがAGS胃腺がん細胞の増殖と上皮間葉転換(EMT)および浸潤を抑制することを提唱した。
ヘリコバクター・ピロリ菌外膜小胞によってパッケージ化されたsncRNAはヒト細胞におけるIL-8分泌を抑制する
この研究論文は、2020年にInternational Journal of Medical Microbiologyに掲載された。この研究では、宿主と病原体の相互作用を研究するためにAGS細胞が用いられた。その結果、ヘリコバクター・ピロリ菌の外膜小胞には、AGS細胞のIL-8レベルに影響を与えるノンコーディングRNAが含まれていることが明らかになった。
6.AGS細胞株のリソースプロトコール、ビデオ、その他
以下はAGS細胞に関するいくつかのリソースである。
- AGS細胞トランスフェクション・プロトコール: このビデオは、胃上皮AGS細胞のトランスフェクション・プロトコルを学ぶための段階的ガイドである。
以下のリンクにAGS細胞培養プロトコールがある。
- AGS細胞培養プロトコール このウェブサイトには、AGS細胞培地と細胞培養プロトコールに関する有用な情報が掲載されている。簡単に説明すると、胃上皮AGS細胞のサブカルチャー、増殖および凍結保存したAGS培養物の取り扱いに関するプロトコールが記載されています。
- AGS細胞のサブカルチャーこのサイトでは、AGS細胞のサブカルチャー手順について詳しく説明する。
参考文献
- Phuc, B.H., et al.,2つのベトナム産ヘリコバクター・ピロリ株(非噴門部胃癌患者由来CHC155株および十二指腸潰瘍患者由来VN1291株)の比較ゲノム解析。Scientific Reports, 2023.13(1): p. 8869.
- Lin,J.、他、miRNA-183-5p.1は、TPM1を標的とすることで、胃がんAGS細胞の遊走と浸潤を促進する Corrigendum in/10.3892/or. 2020.7902.オンコロジーレポート, 2019.42(6): p. 2371-2381.
- Khing、T.M.、他、AGS細胞におけるアポトーシス、オートファジーおよび有糸分裂カタストロフィーに対するパクリタキセルの効果。Scientific Reports, 2021.11(1): p. 23490.
- ヘリコバクター・ピロリ菌の外膜小胞によってパッケージされたsncRNAは、ヒト細胞におけるIL-8の分泌を抑制する。International Journal of Medical Microbiology, 2020.310(1): p. 151356.