U87MG 细胞 - 使用 U87MG 进行胶质母细胞瘤研究及其对脑癌研究的影响
人类原代胶质母细胞瘤细胞系U-87 MG 被广泛应用于生物学研究。特别是在神经科学和免疫肿瘤学领域。
U-87 MG 细胞系的一般特征和起源
本节将介绍 U87 细胞系的起源和一般特征。您将了解什么是 U-87 MG 细胞?U87 细胞来自哪里?U-87 MG 的全称是什么?U87 细胞有多大?U87 细胞系的形态是怎样的?
- U87 细胞系是一种胶质母细胞瘤、星形细胞瘤细胞系。它于 1966 年在乌普萨拉大学建立。细胞取自一名患有胶质母细胞瘤的 44 岁高加索男性。该细胞系正式名称为 U 87 MG,代表乌普萨拉 87 恶性胶质瘤。
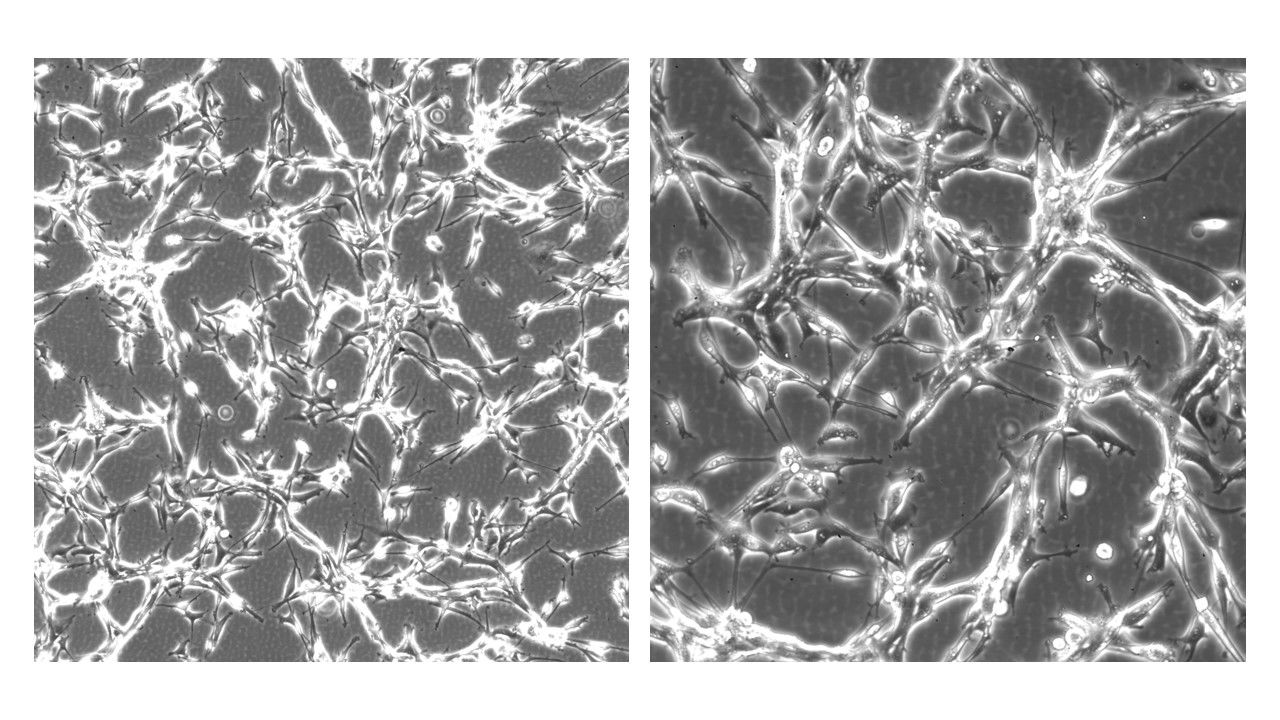
- U 87 MG 细胞具有上皮细胞样形态。
- U 87 MG 细胞的直径在 12 到 14 微米之间。
- 这种人类胶质母细胞瘤细胞系为低二倍体,约 48% 的细胞群中染色体数为 44。不过,在 5.9% 的细胞群中也存在更高的倍数。
U-87 MG 细胞培养信息
在使用 U-87 MG 细胞之前,您应该了解培养这些胶质母细胞瘤细胞的以下要点。特别是要知道U 87 MG 细胞的群体倍增时间是多少?培养 U87 细胞使用什么培养基?U 87 MG 细胞系的播种密度是多少?
培养 U-87 MG 细胞的要点
|
群体倍增时间: |
U 87 MG 细胞的群体倍增时间为 18-38 小时。 |
|
粘附或悬浮: |
U 87 MG 是一种粘附细胞系。细胞形状细长,以单层形式生长。 |
|
接种密度: |
胶质母细胞瘤细胞系 U 87 MG 建议以 1 x104 cells/cm2 的细胞密度播种。用 1 x PBS 冲洗粘附的 U87 细胞,并用 Accutase 溶液孵育。然后,离心并回收解离的细胞。仔细重悬细胞并将其加入装有生长培养基的新烧瓶中。 |
|
生长培养基: |
U 87 MG 细胞系在 EMEM(Eagle's minimal essential medium)培养基中培养,该培养基添加了 1.0 g/L L-葡萄糖、2.0 mM L-谷氨酰胺、2.2 g/L NaHCO3、1% NEAA、1 mM 丙酮酸钠和 10% FBS 溶液。培养基应每 2 至 3 天更新一次。 |
|
生长条件: |
U-87 MG 细胞需要在温度为 37°C 的 37% CO2 加湿培养箱中才能获得最佳生长条件。 |
|
储存: |
将 U87 细胞保存在液氮气相或低于 -150°C 的温度下,以保持胶质母细胞瘤细胞的最大活力。 |
|
冷冻过程和培养基: |
CM-1 或 CM-ACF 冷冻培养基适用于冷冻 U 87 MG 细胞。建议采用缓慢的冷冻过程,以防止细胞受到任何冲击并保护细胞活力。 |
|
解冻过程: |
在 37°C 水浴中解冻冷冻的 U-87 MG 细胞系小瓶。细胞加入生长培养基,重新悬浮,然后分装到新的培养瓶中培养。与此相反,U87 细胞可离心去除冷冻培养基,然后进行培养。 |
|
生物安全等级: |
处理 U87 MG 细胞培养物需要生物安全 1 级。 |
U-87 MG 细胞的优缺点
提到细胞系,我们首先想到的是:使用 U-87 MG 细胞有什么优势?U87 细胞有什么缺点?
优点
U 87 MG 细胞系被广泛用于研究。与这种细胞系相关的几个优点如下:
优点
- 易于生长:U 87 MG 细胞易于培养。它们不需要挑剔或复杂的细胞培养要求。
- 均质性:U-87 MG 是一种均质细胞系。群体中的大多数细胞具有相同的基因构成,因此具有相似的特征。这些细胞可用于研究细胞过程、药物筛选和测试。
- 特征明显:这种胶质母细胞瘤细胞系在生长特性、形态和基因表达方面特征明显,是一种有价值的研究工具。
缺点
- 适用性有限:U 87 MG 是一种胶质母细胞瘤细胞系,因此其应用主要局限于研究胶质母细胞瘤及其潜在的分子机制。它可能不适合研究其他癌症类型。
U-87 MG 细胞的研究应用
U87MG 胶质母细胞瘤细胞系被广泛用于癌症研究,尤其是胶质母细胞瘤研究。U 87 MG 细胞的一些研究应用包括
- 癌症生物学研究: U87 细胞系用于研究癌症的生长和发展、潜在的分子机制、信号通路和肿瘤微环境。2020 年发表的一项研究利用胶质母细胞瘤体外模型--U-87 MG 细胞系--研究作为治疗靶点的 BMAL1(Basic Helix-Loop-Helix ARNT Like 1)基因。研究结果表明,BMAL1基因通过抑制细胞周期蛋白B1、金属蛋白酶-9和磷酸化-AKT基因的表达,抑制胶质母细胞瘤细胞的增殖、迁移和侵袭[1]。2019年开展的另一项研究利用U87细胞系,研究了下调脂多糖诱导的肿瘤坏死因子-α因子(LITAF)转录因子表达可通过上调FOXO-1通路增强胶质瘤细胞的放射敏感性。LITAF 又称 p53 诱导基因 7(PIG7)[2]。
- 药物发现与开发: U-87 MG 细胞可用于药物筛选和测试,使研究人员能够确定新的潜在抗癌药物并评估其疗效和毒性。有研究利用 U-87 MG 胶质母细胞瘤细胞系来评估 Inula helenium(L.)提取物的抗癌和抗氧化潜力[3]。同样,另一篇出版物提到使用 U87 细胞系测试植物提取物的细胞毒性和凋亡效应[4]。此外,2018 年发表的研究报告研究了从 Nuphar 植物中提取的倍半萜生物碱对敏感和耐药 U 87 MG 细胞系的细胞毒性作用[5]。
立即订购您的 U87 MG 胶质瘤细胞系
U-87 MG 细胞系研究论文
以下是一些关于 U-87 MG 细胞系的著名研究论文。
缺氧通过PI3K/Akt/mTOR/HIF-1α通路增强人胶质母细胞瘤U87细胞的迁移和侵袭
这篇发表在《Neuroreport 2018》上的文章提出,缺氧可通过调节PI3K/Akt/mTOR/HIF-1α信号通路增加人胶质母细胞瘤细胞的迁移和侵袭。
桉叶油醇通过PI3K/Akt/NF-κB信号通路抑制胶质瘤细胞的增殖、转移并诱导其凋亡
这项研究发表在 2020 年的《药理学前沿》(Frontiers in Pharmacology)杂志上。研究结果表明,一种黄酮类化合物 Eriodictyol 能对 U87 细胞系产生抗癌作用,抑制细胞增殖和转移。该化合物通过调节PI3K/Akt/NF-κB通路介导其抗肿瘤特性。
西黄丸通过靶向 ROS 介导的 Akt/mTOR/FOXO1 通路诱导人胶质母细胞瘤 U-87 MG 细胞凋亡
这项发表在《循证补充与替代医学》(Evidence-Based Complementary and Alternative Medicine)(2018年)上的研究表明,一种名为西黄丸的中药配方可以通过靶向ROS激活的Akt/mTOR/FOXO1级联诱导U87细胞凋亡。
这篇研究论文发表在2019年的《细胞与分子神经生物学》(Cellular and Molecular Neurobiology)杂志上。研究提出,转录因子LITAF通过调节FOXO-1信号通路下调并增强胶质瘤细胞的放射敏感性。
制备姜黄素负载的PLGA纳米颗粒并研究其对人胶质母细胞瘤U87MG细胞的细胞毒性作用
本文发表于《应用化学生物界面研究》(2019年)。研究人员使用U 87 MG细胞研究姜黄素负载的PLGA纳米颗粒的细胞毒性作用。
有关 U-87 MG 细胞的资源:方案、视频及更多
许多癌症研究实验室都使用 U87MG 胶质母细胞瘤细胞系。以下是有关该细胞系的一些资源:
- 转染 U87 细胞系:本文档将向您介绍 U87 MG 细胞的转染方案。
- U 87 MG 细胞系转染:该视频是一步步解释 U87 细胞转染方案的教程。
U87 细胞的细胞培养方案资源如下:
- U87 MG 细胞:该链接包含有关 U87 MG 细胞系的基本信息。其中包括简要的细胞分裂、冷冻和细胞解冻方案。
深入了解 U87 MG 胶质瘤研究:常见问题
参考文献
- Gwon, D.H., et al.,《BMAL1通过下调细胞周期蛋白B1、磷酸化-AKT和金属蛋白酶-9抑制U87MG细胞的增殖、迁移和侵袭》(BMAL1 Suppresses Proliferation, Migration, and Invasion of U87MG Cells by Downregulating Cyclin B1, Phospho-AKT, and Metalloproteinase-9.Int J Mol Sci, 2020.21(7).
- Huang, C., et al.,LITAF Enhances Radiosensitivity of Human Glioma Cells via the FoxO1 Pathway.Cell Mol Neurobiol, 2019.39(6): p. 871-882.
- Koc, K., et al.,Inula helenium(L.)提取物在人U-87 MG胶质母细胞瘤细胞系中的抗氧化和抗癌活性。J Cancer Res Ther, 2018.14(3): p. 658-661.
- Rezadoost, M.H., H.H. Kumleh, and A. Ghasempour,植物提取物在乳腺癌、皮肤癌和胶质母细胞瘤细胞中的细胞毒性和凋亡诱导作用。Mol Biol Rep, 2019.46(5): p. 5131-5142.
- Fukaya, M., et al.,Cytotoxicity of sesquiterpene alkaloids from Nuphar plants toward sensitive and drug-resistant cell lines.Food Funct, 2018.9(12): p. 6279-6286.