เซลล์ต้นกำเนิดชนิดมีเซนไคม์ของมนุษย์ - ไขกระดูก (HMSC-BM)

























ข้อมูลทั่วไป
| คำอธิบาย | เซลล์ต้นกำเนิดชนิดมีเซนไคม์จากไขกระดูก (HMSC-BM) เป็นเครื่องมือที่แข็งแกร่งและหลากหลายสำหรับการวิจัยในหลอดทดลอง เซลล์ต้นกำเนิดชนิดมีเซนไคม์สโตรมา (MSCs) ที่มีศักยภาพในการเปลี่ยนแปลงเป็นเซลล์ชนิดต่าง ๆ ได้เหล่านี้มีความสามารถพิเศษในการฟื้นฟูตัวเองและเปลี่ยนแปลงเป็นเซลล์ชนิดต่าง ๆ ได้หลากหลาย รวมถึงเซลล์ไขมัน (adipocytes), เซลล์สร้างกระดูก (osteoblasts), และเซลล์สร้างกระดูกอ่อน (chondrocytes) ศักยภาพของ HMSC-BM ในการแยกตัวเป็นสามสายพันธุ์หลักได้รับการบันทึกไว้อย่างดี ทำให้มีคุณค่าอย่างยิ่งสำหรับการศึกษาที่มุ่งเน้นด้านการแพทย์ฟื้นฟู วิศวกรรมเนื้อเยื่อ และเส้นทางการแยกตัวของเซลล์ MSC เหล่านี้ถูกเพาะเลี้ยงภายใต้เงื่อนไขที่เข้มงวด เพื่อให้มั่นใจในความสามารถในการแยกตัวได้หลายรูปแบบและความมีชีวิตสูงหลังการละลาย หนึ่งในลักษณะเด่นของ HMSC-BM เมื่อเปรียบเทียบกับ MSCs ที่ได้มาจากแหล่งอื่น เช่น เนื้อเยื่อไขมันหรือสายสะดือ คือความสามารถในการเปลี่ยนแปลงเป็นเซลล์กระดูกที่เหนือกว่า ซึ่งทำให้มีประโยชน์อย่างยิ่งในด้านชีววิทยาของกระดูกและการวิจัยด้านออร์โธปิดิกส์ ที่ซึ่งการเข้าใจกลไกโมเลกุลที่ควบคุมการสร้างและการซ่อมแซมกระดูกเป็นสิ่งสำคัญ นอกจากนี้ HMSC-BM ยังแสดงโปรไฟล์การปรับภูมิคุ้มกันที่แข็งแกร่ง ซึ่งทำให้เป็นแบบจำลองที่ยอดเยี่ยมสำหรับการศึกษาปฏิสัมพันธ์ของภูมิคุ้มกันและการตอบสนองต่อการอักเสบ คุณลักษณะเฉพาะเหล่านี้ยังทำให้ HMSC-BM เป็นตัวเลือกที่ได้รับความนิยมสำหรับการศึกษาทางพรีคลินิกที่สำรวจสภาพแวดล้อมจุลภาคของไขกระดูก การสร้างเม็ดเลือด และพยาธิสรีรวิทยาของโรคที่เกี่ยวข้องกับไขกระดูก แต่ละหลอดแช่แข็งของ HMSC-BM ประกอบด้วยเซลล์อย่างน้อย 1 x 106 เซลล์ โดยมีอัตราการมีชีวิตอยู่ระหว่าง 92% ถึง 95% ตามการทดสอบการคัดกรองด้วยสีย้อม Trypan Blue เซลล์เหล่านี้ได้มาจากไขกระดูกที่เก็บรวบรวมจากผู้บริจาคผู้ใหญ่ที่มีสุขภาพดี ซึ่งทุกคนได้ให้ความยินยอมอย่างรอบรู้แล้ว เพื่อให้ได้มาตรฐานสูงสุด แต่ละชุดจะต้องผ่านการทดสอบควบคุมคุณภาพอย่างเข้มงวดเพื่อประเมินการระบุเซลล์ ความบริสุทธิ์ ความแรง และความมีชีวิต การทดสอบอย่างละเอียดนี้รับประกันว่าเซลล์ต้นกำเนิดชนิดมัลติโพเทนต์ (MSCs) จะตรงตามเกณฑ์ที่เข้มงวด ทำให้เหมาะสมสำหรับการใช้งานวิจัยที่หลากหลาย รวมถึงการศึกษาชีววิทยาของเซลล์ การค้นคว้ายา และการตรวจสอบการตอบสนองของเซลล์ต่อสิ่งกระตุ้นต่างๆ เซลล์เหล่านี้ไม่ได้มีวัตถุประสงค์เพื่อใช้ในทางการรักษาหรือในร่างกาย และการใช้จะถูกจำกัดไว้เพียงการวิจัยในสภาพแวดล้อมห้องปฏิบัติการที่ควบคุมเท่านั้น |
|---|---|
| สิ่งมีชีวิต | มนุษย์ |
| เนื้อเยื่อ | ไขกระดูก |
| การประยุกต์ใช้ | การทดสอบยา, การแพทย์ฟื้นฟู, การวิจัยโรค |
ลักษณะ
| อายุ | กรุณาสอบถาม |
|---|---|
| เพศ | กรุณาสอบถาม |
| เชื้อชาติ | คอเคเชียน |
| สัณฐานวิทยา | ลักษณะรูปร่างคล้ายแกนหมุนที่กระจายตัวดีและมีลักษณะคล้ายไฟโบรบลาสต์อย่างน้อยภายใน 5 ครั้งของการผ่านเซลล์ผ่านสื่อเลี้ยงเซลล์ พบเซลล์ที่มีลักษณะคล้ายไมโอไฟโบรบลาสต์โดยธรรมชาติน้อยกว่า 2% ในแต่ละครั้งของการผ่านเซลล์ |
| ชนิดของเซลล์ | เซลล์ต้นกำเนิด |
| คุณสมบัติการเติบโต | ยึดติด |
ข้อมูลด้านกฎระเบียบ
| การอ้างอิง | เซลล์ต้นกำเนิดชนิดมีเซนไคม์ของมนุษย์, ไขกระดูก (HMSC-BM) (หมายเลขแคตตาล็อก Cytion 300665) |
|---|---|
| ระดับความปลอดภัยทางชีวภาพ | 1 |
| NCBI TaxID | 9606 |
ข้อมูลชีวโมเลกุล
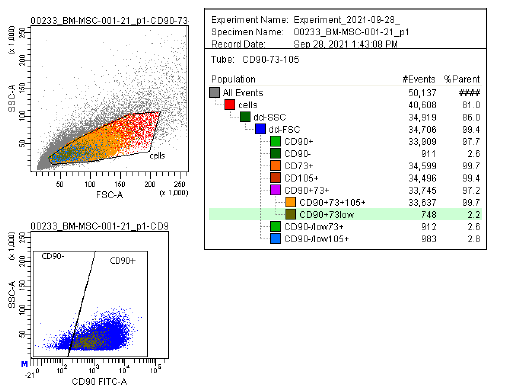
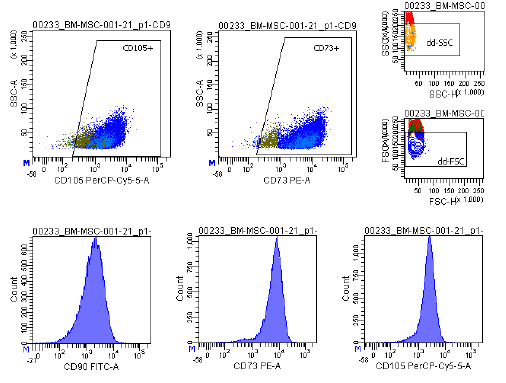
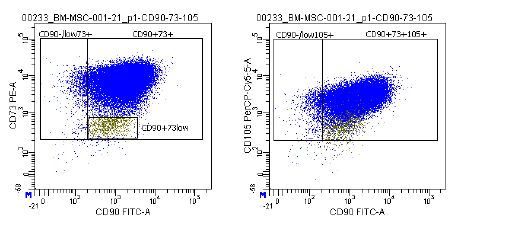
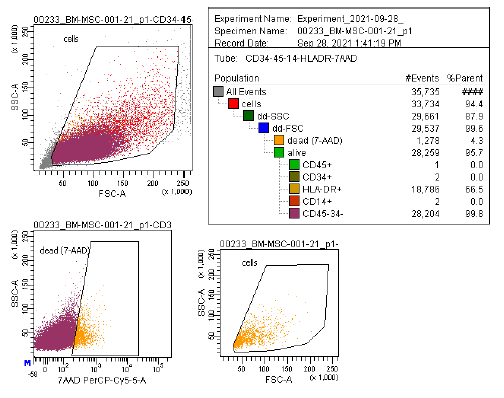
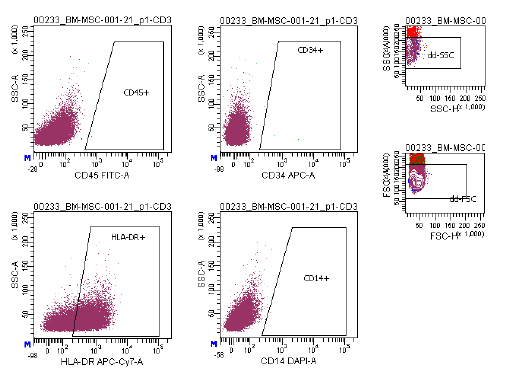
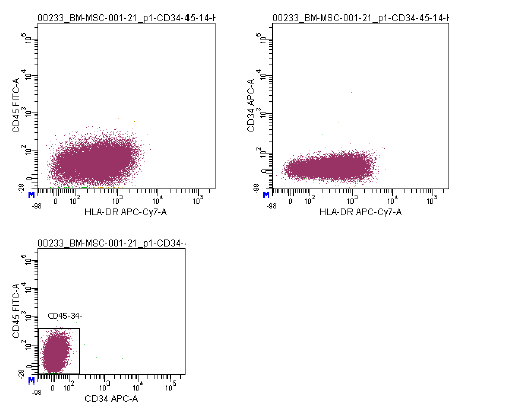
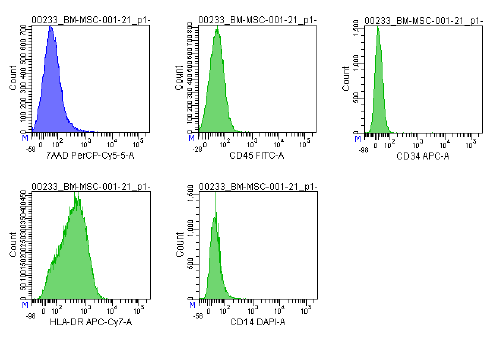
| การแสดงออกของแอนติเจน | ชุดตัวบ่งชี้ที่ครอบคลุม ซึ่งรวมถึง CD73/CD90/CD105 (บวก) และ CD14/CD34/CD45/HLA-DR (ลบ) ถูกใช้ในการวิเคราะห์ด้วยโฟลไซโตเมทรีเพื่อระบุเซลล์ต้นกำเนิดจากไขกระดูก (MSCs) ที่เพาะเลี้ยง (P2-P3) ก่อนการแช่แข็ง ตัวบ่งชี้เหล่านี้ได้รับการแนะนำโดยคณะกรรมการ ISCT MSC |
|---|---|
| ไวรัส | ผู้บริจาคมีผลลบสำหรับ HBV (PCR), Treponema pallidum (PCR), และ HIV-1/2 (IFA) เซลล์ไม่พบเชื้อ HBV, HCV, HSV1, HSV2, CMV, EBV, HHV6, Toxoplasma gondii, Treponema pallidum, Chlamydia trachomatis, Ureaplasma urealyticum และ Ureaplasma parvum |
การจัดการ
| อาหารเลี้ยงเชื้อ | Alpha MEM, w: กลูตามีนเสถียร 2.0 มิลลิโมลาร์, w/o: ไรโบนิวคลีโอไซด์, w/o: เดโซออกซีไรโบนิวคลีโอไซด์, w: โซเดียมไพรูเวต 1.0 มิลลิโมลาร์, w: NaHCO3 2.2 กรัม/ลิตร |
|---|---|
| อาหารเสริม | เติมอาหารเลี้ยงเชื้อด้วย FBS 10%, bFGF 2 นาโนกรัมต่อมิลลิลิตร |
| สารละลายตัวแยก | ทริปซิน-เอดทีเอ |
| การเพาะเลี้ยงเชื้อแบบแยกส่วน | สำหรับการเพาะเลี้ยงเซลล์ที่เกาะติดแบบปกติ: ดูดสกัดน้ำเลี้ยงเก่าออกจากเซลล์ที่เกาะติด และล้างเซลล์ด้วย PBS เพื่อกำจัดน้ำเลี้ยงที่เหลืออยู่หลังจากดูด PBS ออกแล้ว ให้เติมสารละลาย Trypsin/EDTA ในปริมาณที่เหมาะสมตามขนาดของภาชนะเพาะเลี้ยง (เช่น 1 มล. สำหรับขวด T25, 3 มล. สำหรับขวด T75) และทำการบ่มที่อุณหภูมิห้องหรือ 37°C จนเซลล์หลุดออกจากผนัง (ประมาณ 5-10 นาที)สังเกตการหลุดของเซลล์ภายใต้กล้องจุลทรรศน์ และเคาะภาชนะเบา ๆ หากจำเป็นเพื่อปล่อยเซลล์ เมื่อเซลล์หลุดออกแล้ว ให้เติมอาหารเลี้ยงเซลล์แบบครบถ้วนเพื่อหยุดการทำงานของ Trypsin/EDTA คนเซลล์ให้กระจายตัวอย่างเบามือ แล้วแบ่งตัวอย่างเซลล์ที่แขวนลอยใส่ลงในภาชนะเพาะเลี้ยงใหม่ที่มีอาหารเลี้ยงเซลล์สด วางภาชนะในตู้อบที่ตั้งอุณหภูมิไว้ที่ 37°Cพร้อมก๊าซคาร์บอนไดออกไซด์ 5% และเปลี่ยนอาหารเลี้ยงเซลล์ทุก 2-3 วัน |
| ความหนาแน่นของการหว่านเมล็ด | 1 ถึง 3 x 104 เซลล์/เซนติเมตร² |
| การฟื้นฟูของเหลว | เปลี่ยนของเหลวครั้งแรกหลังจาก 24 ชั่วโมง จากนั้นทุก 2 ถึง 3 วัน |
| สื่อเลี้ยงเซลล์แบบแช่แข็ง | ในฐานะที่เป็นสารอาหารสำหรับการแช่แข็ง เราใช้ FBS 80% + สารอาหารพื้นฐาน 10% + DMSO 10% เพื่อรักษาความมีชีวิต หรือ CM-1 (หมายเลขแคตตาล็อก Cytion 800100) สำหรับการป้องกันความเสียหายจากการแช่แข็งที่เหนือกว่า ป้องกันการเปลี่ยนแปลงที่ไม่ต้องการในขณะที่รักษาความสามารถในการเปลี่ยนแปลงเป็นเซลล์ต้นกำเนิดหลายชนิด |
| การละลายและการเพาะเลี้ยงเซลล์ |
|
| บรรยากาศการบ่มเพาะ | 37°C, 5%CO2, บรรยากาศชื้น |
| การเคลือบขวด | สำหรับการยึดเกาะและการมีชีวิตที่ดีที่สุดหลังการละลาย เราแนะนำให้ใช้ขวดหรือจานเคลือบคอลลาเจน |
| ขั้นตอนการแช่แข็ง | เซลล์ไลน์ที่แช่แข็งในไนโตรเจนเหลวจะถูกจัดส่งในบรรจุภัณฑ์ที่ผ่านการตรวจสอบแล้วและมีการเก็บรักษาความเย็นด้วยน้ำแข็งแห้ง พร้อมสารทำความเย็นที่เพียงพอเพื่อรักษาอุณหภูมิประมาณ −78 °C ตลอดการขนส่ง เมื่อได้รับสินค้า ให้ตรวจสอบภาชนะทันทีและถ่ายโอนหลอดทดลองไปยังที่เก็บที่เหมาะสมโดยไม่ล่าช้า |
| เงื่อนไขการจัดส่ง | เซลล์ไลน์ที่แช่แข็งในไนโตรเจนเหลวจะถูกจัดส่งในบรรจุภัณฑ์ที่ผ่านการตรวจสอบแล้วและมีการเก็บรักษาความเย็นด้วยน้ำแข็งแห้ง พร้อมสารทำความเย็นที่เพียงพอเพื่อรักษาอุณหภูมิประมาณ −78 °C ตลอดการขนส่ง เมื่อได้รับสินค้า ให้ตรวจสอบภาชนะทันทีและถ่ายโอนหลอดทดลองไปยังที่เก็บที่เหมาะสมโดยไม่ล่าช้า |
| เงื่อนไขการเก็บรักษา | สำหรับการเก็บรักษาในระยะยาว ให้วางหลอดบรรจุในไนโตรเจนเหลวในสถานะไอที่อุณหภูมิประมาณ −150 ถึง −196 °C การเก็บรักษาที่อุณหภูมิ −80 °C สามารถใช้ได้เฉพาะในระยะสั้นก่อนการย้ายไปยังไนโตรเจนเหลวเท่านั้น |
การควบคุมคุณภาพ / โปรไฟล์ทางพันธุกรรม / HLA
| ความปราศจากเชื้อ | การปนเปื้อนของไมโคพลาสมาถูกตัดออกโดยใช้ทั้งการทดสอบแบบ PCR และการตรวจหาไมโคพลาสมาโดยใช้วิธีการเรืองแสง เพื่อให้แน่ใจว่าไม่มีการปนเปื้อนของแบคทีเรีย เชื้อรา หรือยีสต์ การเพาะเลี้ยงเซลล์จะถูกตรวจสอบด้วยสายตาทุกวัน |
|---|
ใบรับรองการวิเคราะห์ (CoA)
| หมายเลขล็อต | ประเภทใบรับรอง | วันที่ | หมายเลขแคตตาล็อก |
|---|---|---|---|
| 300665-240423P1 | ใบรับรองการวิเคราะห์ | 26. Mar. 2026 | 300665 |
ข้อตกลงการโอนวัสดุ
หากคุณมีความประสงค์จะใช้สายเซลล์ Cytion เฉพาะสำหรับการวิจัยภายในองค์กร ณ สถานที่วิจัยเพียงแห่งเดียวเท่านั้น กรุณากรอกและลงนามในข้อตกลงการโอนวัสดุ (MTA) ของเราให้ครบถ้วน และส่งพร้อมใบสั่งซื้อของคุณ
สำหรับการใช้งานเชิงพาณิชย์ใด ๆ - รวมถึงแต่ไม่จำกัดเพียง งานบริการที่มีค่าธรรมเนียม การทดสอบควบคุมคุณภาพ การปล่อยผลิตภัณฑ์ การใช้งานเพื่อการวินิจฉัย หรือการศึกษากฎระเบียบ - กรุณากรอกแบบฟอร์มการใช้งานที่ตั้งใจไว้ เพื่อให้เราสามารถจัดเตรียมข้อตกลงที่เหมาะสมกับโครงการของคุณได้
โปรดทราบ: MTA ใช้ได้เฉพาะกับสายเซลล์บางชนิดเท่านั้น หากประกาศนี้และเอกสาร MTA ปรากฏบนหน้าผลิตภัณฑ์ ข้อตกลงนี้จะมีผลบังคับใช้ สำหรับสายเซลล์ที่ไม่ครอบคลุมโดย MTA จะไม่มีการอ้างอิงถึงข้อตกลงนี้ MTA ไม่มีผลบังคับใช้กับลูกค้าในอเมริกา จีน หรือไต้หวัน โปรดติดต่อหน่วยงานของเราในสหรัฐอเมริกาเพื่อรับข้อตกลงที่เหมาะสม
